- 您的位置:
- 标准下载网 >>
- 标准分类 >>
- 国家标准(GB) >>
- GB/T 4789.38-2008 食品卫生微生物学检验 大肠杆菌计数
标准号:
GB/T 4789.38-2008
标准名称:
食品卫生微生物学检验 大肠杆菌计数
标准类别:
国家标准(GB)
标准状态:
现行-
发布日期:
2008-11-21 -
实施日期:
2009-03-01 出版语种:
简体中文下载格式:
.rar.pdf下载大小:
750.35 KB
标准ICS号:
数学、自然科学>>微生物学>>07.100.30中标分类号:
医药、卫生、劳动保护>>卫生>>C53食品卫生
点击下载
标准简介:
标准下载解压密码:www.bzxz.net
本标准规定了食品中大肠杆菌计数的方法。本标准适用于各类食品中大肠杆菌的计数,其中第二法不适用于贝类产品。 GB/T 4789.38-2008 食品卫生微生物学检验 大肠杆菌计数 GB/T4789.38-2008
部分标准内容:
ICS 07.100.30
中华人民共和国国家标准
GB/T4789.382008
食品卫生微生物学检验
大肠杆菌计数
Microbiological examination of food hygiene-Fnumeration of Escherichia coli2008-11-21发布
中华人民共和国卫生部
中国国家标准化管理委员会
2009-03-01实施
中华人民共利国
国家标准
食品卫生微生物学检验
大肠杆菌计数
GR/T 4789,38- 2008
中国标准出版社出版发行
北京复兴门外三里河北街16号
邮致编码:100045
网址 spc. net. cn
电话:6852394668517548
中国标准出版社秦皇岛印刷厂印刷各地新华书店经销
开本880×12301/16
印张 1字数 24千宁
2009年3月第一版
2009年3月第一次印刷
书号:155066·1-36115定价16.00元由本社发行中心调换
如有印装差错
版校专有
傻权必究
举报电话:(010)68533533
http://foodmate.net.
GB/T 4789.38—2008
本标准的第一法和第二法修改采用美国食品药品管理局(FDA)细菌学分析乎册》第4章大肠析菌和大肠菌群计数(2002 年)(Bactcriological Analytical Manual,Chaptcr 4,Enumeration of Escherichia coti and the caliform bacleria,2002),第三法修改来用国际分析家学会(AOAC INTERNATIONAL)AOAC991.14≤食品中大肠菌群和大肠杆菌计数Pctrifilm测试片法》(1994年)(AOAC.OricialMethod 9g1, 14,Coliform and Eseherichiu cti colinls in foods Dry rehydratahle film Petrifilm E, coficauntplateandPetrifilmcoliformcountplatemethods,1994)和A(AC998.08%禽、肉和水产品中大肠杆菌计数(1998年)(A0ACOfficialMethod998.08,ComfirmedEscherichiacotiinpoultry,meatsand scafood -Dry rehydratable film method Petrifilm E. coti count plate, l998) .本标准的第-法和第二法与FDA方法的主要区别是:将样品制备时取样量50g(或50ml)修为25名(或25mL);将培养温度35℃1℃修改为36℃+1℃;将EC培养温度 45. 5 ℃±0. 2 ℃(一般食品)和 44. 5 ℃±0. 2 ℃(贝类)统一为 44. 5 ℃±o.2℃
本标准的第法与 AOAC方法的上要区别是:将样品制备时取样50g(或50mL)修改为25g(或25mL);将培养温度35℃十1℃修改为36℃±1℃。本标准的附录 A.附录 B 为规范性附录。本标准电中华人民法和国卫生部提出并归。本标准由中华人民共和国卫生部负责解释。本标准负责起草单位:中国疾病预防控制中心营养与食品安全所。本标准参与起草单位:中华人民共和国内蒙古出人境检验检疫局、江苏省疾病预防控制中心、上海市疾病预防控制中心、中华人民共和国辽宁出人境检验检疫局。本标准主要起草人:刘秀梅、刘中学、袁宝君、刘弘、陈敏卢行安、田静。1
1范围
食品卫生微生物学检验
大肠杆菌计数
木标雄规定了食晶中大肠杆菌计数的法。本标谁适用于各类食品中大肠杆菌的计数,其中第二法不适用于贝类产品。2术语和定义
下列术语和定义适用于本标准。2.1
GB/T 4789.38—2008
大肠杆茵Escherichia coli
广泛存在于人和温血动物的肠道中,能够在44.5℃发酵乳糖产酸气,IMViC(靛基质,甲基红,VP试验、柠檬酸盐)生化试验为十十二一或一十一一的革兰氏阴性析菌。以此作为粪便污染指标来评价食品的卫生状况,推断食品中肠道致病菌污染的可能性。2.2
最可能数
most probable number; MPN
基于泊松分布的·-种间接计数方法3设备和材料
除微生物实验室常规火菌及培养设备外,其他设备和材料如下:3.1恒温培养箱:36℃±1℃。
3. 2 冰箱:2 ℃~5℃
3.3恒温水裕箱:44.5℃±0.2℃。3.4天平:感量0. 1 g。
3.5均质器。
3.6振荔器。
3.7无菌吸管:1mL(具0.01mL刻度)、10mL(具0.1mL刻度)或微量移液器及吸头:3.8无菌锥形瓶:容量500ml。
3. 9无菌培养血;直径 90 mm
3.10pH计或pH比色管或精密pH试纸,3.11菌落计数器或PctrifilmTm1>自动判读仪。3.12紫外灯:波长360nm~366nm,功率≤6W。A培养基和试剂
4.1月桂基磺酸盐胰蛋白陈(laurylsul(atetryptose,LST)肉汤:见第A,1章。4.2EC肉汤(E.coibroth):见第A.2章。4.3蛋白陈水:见第A.3章,
4.4缓冲葡荷糖蛋白陈水(MR-VP实验用):见第A.1章。4.5Korser柠檬酸盐肉汤:见第A,5章。PetrifilnTu是由3M公司提供的产品的商品名。给出这一信息是为了方便本标准的使用者,并不表示对该产1)
品的认可。如果其他等效产品具有相同的效果,则可使用这些等效的产品。品成伴网ht
GB/T 4789.38—2008
磷酸盐缓冲腋:见第A.6章。
伊红美蓝(easin mcthylene bilue,EMB)琼脂:见第 A.7章。营养琼脂斜面:见第 A,8章。
4.9结晶紫中性红胆盐(violetredbilc,VRB)琼脂:见第A,9章。VRB-MUG琼脂:见第A.10章。
革兰氏染色液:见第A.11章。
Kovars 靛基质试剂:见第 A. 12 章。甲基红指示剂:见第A.13章。
Voges-pros kauer(V-P)试剂:见第 A. 14 。无菌生理盐水,称取8.5g氯化钠溶于1000mL蒸馏水中,121℃高压灭菌15min。tmol/L氢氧化钠(NaOH):称取40g氢氧化钠溶于1000mL蒸馏水中。Imo1/L盐酸(HCl):移取浓盐酸90ml用蒸馏水稀释至I000mL。PctrililmEM大肠菌群/大肠杆菌检验澍试片。第一法大肠杆菌MPN计数
5检验程序
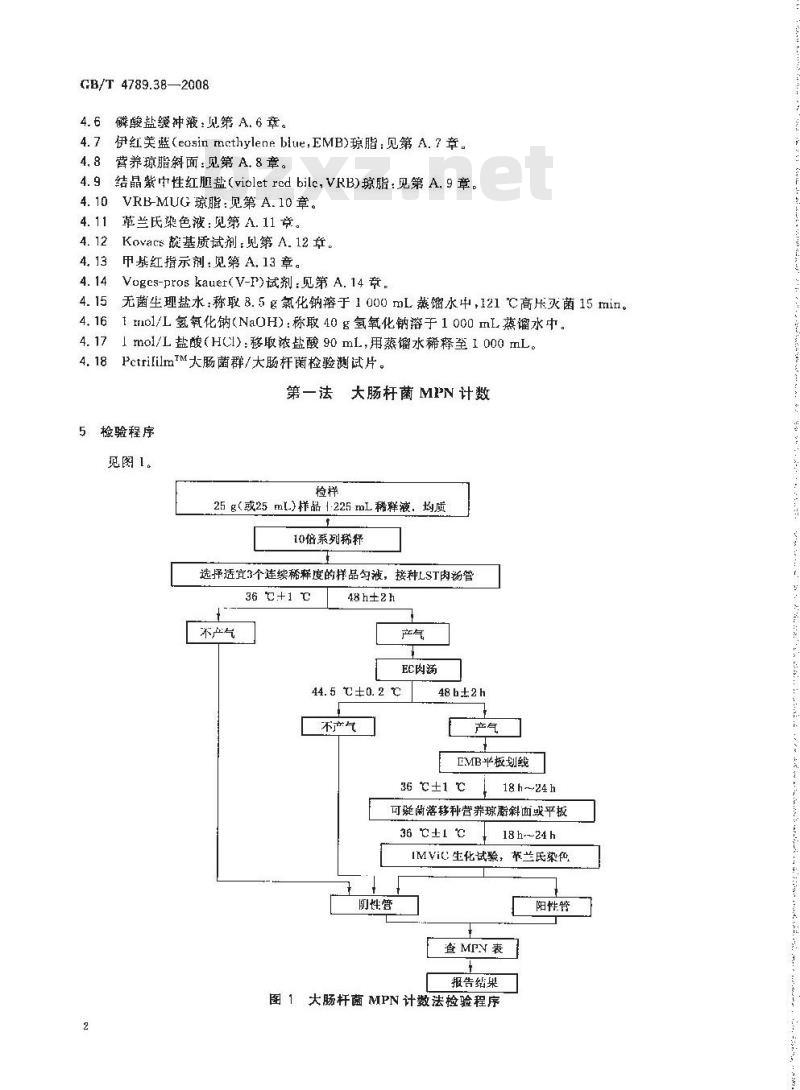
见图1。
25g(或25 ml)样品1-225 mL稀液。均质10倍系列稀释
选择适宜3个连续稀释度的样品勾液,接种LST肉汤管36 ℃+1 ℃
不产气
48h±2h
EC肉汤
44. 5±0. 2℃
不产气
48b±2h
EMB平板划线
36 ℃±1 ℃
18h~24h
可蜓菌落移种营养琼胎斜面或平板36 ±1 ℃
18h-24h
IMViC生化试验,求兰氏染色
阴性管
查MPN表
报告结果
图1大肠杆菌MPN计数法检验程序2
http:
rungfooc
ate net
阳性管
6操作步骤
6.1样品的稀释
GB/T 4789.38—2008
6.1.1固体和半固体样品:以菌操作取25g样品,置盛有225mL磷酸盐缓冲液的无菌均质杯内80001/min~10000r/min均质1min~2min,制成1:10样品勾液,或置盛有225mL磷酸盐缓冲液的无菌均质袋中,用拍击式均质器拍打1min~2min制成1:10的样品勾液。6.1.2液体样品:以无菌吸管吸取样品25mL置盛有225ml.磷酸盐缓冲液的无菌锥形瓶(瓶内预置适当数量的玻璃珠)中,充分振摇,制成1:10的样品勾液。6.1.3样品匀液的PH值应在6.5~~7.5之间,必要时分别用1ol/L氢氧化钠6.1.4用1mL无菌吸管或微量移液器吸取110样品勾液1mL,沿管徐徐注入盛有9mL磷酸盐缓冲液的无菌试管中(注意吸管或吸头尖端不要触及稀释液面),振摇试管或换用1支1ⅡL无菌吸管或吸头反复吹打,使其混合均匀,制成1:100的样品匀液。6.1.5根据对样品污染状况的估计,按上述操作,依次制成10倍递增系列样战勾液。每递增稀释1次,换用1支1mL无菌吸管或吸头。从制备样品勾被至样品接种完毕,全过程不得超过15min,6.2初发酵试验
每个样品,选择3个适宜的连续稀释度的样品勾液(液体样品可以选择原液)。每个稀释度接种3管月桂基磺酸盘胰蛋白陈(LST)肉汤,每管接种1mL(如接种量超过1ml则用双料LST肉汤)。36℃士1℃培养24h士2h观察小倒管内是否有气泡产生,如未产气则继续培养垒48h土2h,记录在24h~48h内产气的LST肉汤管数。如所有LST肉汤管均末产气,即可报告大肠杆菌MPN结果,如有产气者,则进行复发酵试验。6,3复发酵试验
用接种环分别从所有培养18h土2h内发酵产气的1.ST肉汤管中取培养物1环,移种十已提前预温至45℃的EC肉汤管中,放人带盖的14.5℃三0.2℃水浴箱内。水裕的水面应高于肉汤培养基液面,培养24h士2h,检查小倒管内是否有气泡产生,如末产气则继续培养至48h土21。记录在24h利48h内产气的EC肉汤管数。如所有EC肉汤臂均未产气,即可报告大肠杆菌MPN结果,如有产气者则进行EMB平板分离培养。
6.4伊红美蓝平板分离培养
轻轻振摇各产气管,用接种环取培养物划线分别接种于EMB平板,36℃±1℃培养18h~24h检验平板上有无具黑色中心有光泽或尤光泽的典型菌落。6.5营养琼脂斜面或平板培养
从每个平板[-挑5个典型菌落,如无典型菌落则挑取可疑菌落。用接种针接触菌落中心部位,移种到营养琼脂斜面或平板13GC土1℃,培养18h~24h。取培养物进行革兰氏染色和生化试验。6.6生化试验
6.6.1靛基质试验:将培养物接种蛋白陈水,36℃土1C培养24h土2h后,加Kovacs靛基质试剂0.2ml0.3mL,上层出现红色为靓基质阳性反应,6.6.2MR-VP试验:将培养物接种MR-VP培养基,36℃土1C培养48h士2h。移取培养物1mL.至13mm×100mm试管中,加5%α-素酚乙醇溶液0.6mL、40%氢氧化钾溶液0.2ml.和少许肌酸结晶,振摇试管后静置2h,如出现红色,为VP试验阳性。将MRVP培养液的剩余部分再培养48h后滴加5滴甲基红指示剂。培养物变红色,为甲基红试验阳性,若变黄色则为阴性反应。6.6.3柠檬酸盐利用试验:将培养物接种Koscr氏柠檬酸盐肉汤,36℃+1℃培养96h士2h,记录有无细菌生长。
GB/T 4789.38—2008
大肠杆菌与非人肠杆菌的生化鉴别见表1.表1大肠杆菌与非大肠杆菌的生化鉴别靛基质(I)
甲基红(MR)
VP 试验(VP)
柠檬酸盐(C)
墨延(型别)
典型大托菌
非典型大肠杆菌
典型中间型
非典型中间型
典型产气肠杆菌
非典型产气肠杆
注1:如出现表1以外的生化反应类型,表明培养物可能不纯,应重新刘线分离,必要时做重复试验。注2:生化试验也可以选用VITEKGNI鉴延卡、API20E等方法,按照产品说明书进行操作。6.7大肠杆菌MPN计数的报告
大肠杆菌为革兰氏阴性无芽胞杆菌,发酵乳糖、产酸、产气,IMViC生化试验为+:+一一或。只要有1个菌落鉴定为大肠杆菌,其所代表的LST肉汤管即为大肠杆菌阳性。依据LST肉汤阳性管数查MPV表(见附录B),报告每克(或亳升)样品中大肠杆菌MPN值。大肠杆菌VRB-MUG乎板计数法
第二法
检验程序
见图2。
25g(或25mL)样品+225mL稀释液,均质10倍系列稀释
选择2个3个适宜连续稀释度的样品液,按种VRB-MUJG半板36 ℃±1 ℃
18 h~21 h
紫外灯照射,计数发荧光菌落
报告结果
图2大肠杆菌VRB-MUG平板计数法检验程序8样品稀释
按6.1进行。
9检验
GB/T 4789.38—2008
选取2个-3个适宜的连续稀释度的样品句液,每个稀释度分别取1mL注人两个无菌平。另取1 mL稀释液注人一个尤菌平血中,作空白对照:将 45 ℃土0. 5 ℃的 VRB琼脂 10 mL~15 mL 倾注于每个平Ⅲ中。小心旋转平Ⅲ,将培养基与样品匀液充分混勾。待琼脂凝固后,再加 3 nL~4InL VRBMUG琼脂盖平板表层。疑固后翻转平板,36℃土1℃培养18h~24h。选择菌落数为10~100的平板,暗窄中360nm~366nm波长紫外灯照射下,计数平板上发浅蓝色荧光的菌落,检验时用已知MUG阳性菌株(如大肠杆菌ATCC25922)和产气肠杆菌(如ATCC13048)做阳性和阴性对照。
10大肠杆菌平板计数的报告
两个半板上发荧光菌落数的平均数乘以稀释倍数,报告每克(或毫升)样品中大肠杆菌数,以CFU/g(CFU/mlL)表示.
第三法大肠杆菌PelrifilimrM测试片计数法11检验程序
见图3。
25g(或25ml.)样品+225mL稀释液,均质10倍系列稀释
选择适宜2个~~3个连续稀释度的样品勾液,接种Pctrifilm:M测试36 ℃±1 ℃
24h±2 h或48 h±2 h
计数Petrifilm\hi测试片上的蓝色借气泡菌报告结果
图3大肠杆菌PetrifilmM测试片计数法检验程序12样品稀释
按6.1进行。
13检验
13.1接种和培养
选取2个~3个适宜的连续稀释度的样品匀液,每个稀释度接种两张测试片。将测试片置于平坦实验台面,揭开上层膜,用吸管吸取样品匀液1mL垂直滴加在测试片的中央,将上层膜缓慢益下,避免5
ht
GB/T 4789.38—2008
气泡产生和.1-层膜直接落下,将压板(平面底朗下)放置在上层膜中央处,轻轻地乐下,使样品匀液均勾覆盖于圆形的培养膜表面,切勿扭转压板。拿起压板,静置至少1min以使培养基凝固。将测试片的透明面朝上置于培养箱内,堆叠片数不超过20片,36℃士1℃培养。肉、家禽和水产品,培养时间为24h士2h;其他食品,培养时间为48 h士2h,13.2判读
肉服观察计数,或用菌落计数器、放大镜.PetririlrnrM自动判读仪计数。蓝色有气泡的菌葬确认为人肠杆菌,不论蓝色的深浅,部分蓝色的带气泡菌落也判定为大肠杆菌。圆形培养膜边缘及边缘以外的菌落不计数。当测试片出现大量气泡、不明显的小菌落,培养区呈蓝色时,需要进一步稀释样品勾液,重新检验。
14大肠杆菌测试片计数的报告
选择菌落数在15~150之间的稀释度,两张测试片菌落平均数乘以稀释倍数,即为每克(或毫升)样品巾大肠杆菌数,以CFU/g(CFU/mL)表示。如果所有稀释度测试片七的菌落数郁小于15,计数最低稀释度测试片上的平均菌落数乘以稀释倍数报;如果所有稀释度的测试片上均无菌落生长,以“小于1乘以最低稀释倍数”报告;如果所有稀释度的菌落数都人于150,计数最高稀释度测试片上的平均菌落数乘以稀释倍数报告。计数菌落数大于150个的测试片时,可计数·个或两个具有代表性的方格内的菌落数,换算成单个方格内的菌落数后乘以20,即为测试片1估算的菌落数(圆形生长面积为20cm)。6
A.1月桂基磺酸盐胰蛋白陈(LST)肉汤A.1.1成分
胰蛋白陈或胰酪陈
氯化钠
磷酸氢二钾(K,HPO,)
磷酸二氨钾(KH,PO)
月桂基硫酸钠
蒸馏水
pH6.8±0.2
A. 1.2制法
附录A
(规范性附录)
培养基和试剂
1 000 nL
GB/T4789.38—2008
将上述成分溶解于蒸馅水中,调节pII。分装到有玻璃小倒管的试管中,每管10mL,121C高压灭菌 15 min。
制备双料LST肉汤时,除蒸馏水外其他成分加倍。A,2EC肉汤
A.2.1戒分
胰蛋白豚或胰酪陈
3号胆盐或混合脏盐
磷酸氢二钾(K.HPO,)
磷酸二氢钾(KH,PO)
氯化钠
蒸馏水
pH6. 9±0.1
A.2.2制法
1 000.0 mL
将上述成分溶解于蒸馏水中,调节pH,分装于有倒立小发酵管的试管中,每管8mL。121℃高压灭菌 15 min。
A.3蛋白陈水
A,3.1 成分
膀陈或胰酪陈
蒸馏水
pH6. 9±0. 2
A.3.2制法
1 000. 0 ml
加热搅拌解映豚或胰酪陈于蒸馏水中。分装试管,每管5mL。121℃高压灭菌15tmin。7
http:/
ate net
GB/T 4789.38200B
A, 4缓冲葡萄糖蛋白陈水(MR-VP 实验用)A.4.1成分
葡萄糖
癣酸氨二钾(K,HPO,)
蒸馏水
pH6.9±0.2
A.4.2制法
1 000.0 mL
将上述成分溶于蒸馅水中,调节pH,分装试管,121℃高压灭菌15min。A.5Korsr氏柠檬酸盐肉汤
A.5.1成分
磷酸氢铵钠(NaNHHPO4·4H,O)
磷酸氨一钾(KHPO
硫酸镁(MgS0,·7H,0)
柠檬酸钠(含2H,O)
蒸馏水
pH6.7±0.2
A.5.2制法
1 000. 0 mL
将上述成分溶解于蒸馏水中,调节pH,分装试管,每管10mL,121℃高压炎菌15min。A.6磷酸盐缓冲液
A.6.1成分
磷酸二氨钾(KH,PO,)
蒸馏水
A, 6.2制法
500 mL
贮存液:称取34.0g的磷酸二氢钾溶于500mL蒸馏水中,用大约175mL的1mol/L氢氧化钠溶液调节pH至7.2.用蒸馏水稀释至1000mL后贮存于冰箱。稀释液:取贮存液1.25mL,用蒸馏水稀释至1000ml,分装于适宜容器中,121℃高压灭菌15min。
伊红美蓝琼脂(EMB)
A.7.1成分
蛋白豚
磷酸氢二钾(K,HPO)
伊红水溶液)
蒸馏水
pH 7. 1±0.2
0. 1 多或 2%水溶液 20 mL
0.065g或0.5%水溶液13ml.
1 000.0 mL
品成伴网httn
A.7.2制法
GB/T 4789.38—2008
在1 000 mL 蒸馏水中煮沸溶解蛋白陈,磷酸盐和琼脂,加水补足。分装于三角烧瓶中,钙瓶100 mL 或 200 mL,调节 pH,高压灭菌。使用前将琼脂融化,于每 1U0 mL.琼脂中加5 ml. 灭菌的 20%乳糖溶液,2 mL的 2%的伊红 水溶液和 1. 3 mL 0. 5%的美蓝水溶液,摇勺,冷至 45 ℃~50 ℃倾注平血。
A.8营养琼脂斜面
A.8.1成分wwW.bzxz.Net
牛肉膏
蛋白陈
蒸馏水
pH7.3±0.1
A.,B.2制法
1 000. 0 mL
将上述成分加于蒸馏水中,点沸溶解,调节pH,分装合适的试管,121℃高压灭菌15min。灭菌后摆成斜面备用。
A, 9结晶紫中性红胆盐(VRB)琼脂A. 9. 1 成分
蛋白膝
酵母膏
氯化钠
胆盐或3号服盐
中性红
结晶紫
蒸馏水
pH7.4±0. 1
A.9.2制法
15 g~18 g
1 000.0 mL
将上述成分溶于蒸水中,静置儿分钟,充分揽拌,调节pH。煮沸2min,将培养基冷至45℃~50℃癫注平板,临用时制备,不得超过3h。A.10VRB-MUG琼脂
A.10.1成分
蛋白陈
酵母湾
氯化钠
胆盐或 3号胆盐
中性红
结晶紫
15 g-18 g
http:
rungfooc
atenet
小提示:此标准内容仅展示完整标准里的部分截取内容,若需要完整标准请到上方自行免费下载完整标准文档。
中华人民共和国国家标准
GB/T4789.382008
食品卫生微生物学检验
大肠杆菌计数
Microbiological examination of food hygiene-Fnumeration of Escherichia coli2008-11-21发布
中华人民共和国卫生部
中国国家标准化管理委员会
2009-03-01实施
中华人民共利国
国家标准
食品卫生微生物学检验
大肠杆菌计数
GR/T 4789,38- 2008
中国标准出版社出版发行
北京复兴门外三里河北街16号
邮致编码:100045
网址 spc. net. cn
电话:6852394668517548
中国标准出版社秦皇岛印刷厂印刷各地新华书店经销
开本880×12301/16
印张 1字数 24千宁
2009年3月第一版
2009年3月第一次印刷
书号:155066·1-36115定价16.00元由本社发行中心调换
如有印装差错
版校专有
傻权必究
举报电话:(010)68533533
http://foodmate.net.
GB/T 4789.38—2008
本标准的第一法和第二法修改采用美国食品药品管理局(FDA)细菌学分析乎册》第4章大肠析菌和大肠菌群计数(2002 年)(Bactcriological Analytical Manual,Chaptcr 4,Enumeration of Escherichia coti and the caliform bacleria,2002),第三法修改来用国际分析家学会(AOAC INTERNATIONAL)AOAC991.14≤食品中大肠菌群和大肠杆菌计数Pctrifilm测试片法》(1994年)(AOAC.OricialMethod 9g1, 14,Coliform and Eseherichiu cti colinls in foods Dry rehydratahle film Petrifilm E, coficauntplateandPetrifilmcoliformcountplatemethods,1994)和A(AC998.08%禽、肉和水产品中大肠杆菌计数(1998年)(A0ACOfficialMethod998.08,ComfirmedEscherichiacotiinpoultry,meatsand scafood -Dry rehydratable film method Petrifilm E. coti count plate, l998) .本标准的第-法和第二法与FDA方法的主要区别是:将样品制备时取样量50g(或50ml)修为25名(或25mL);将培养温度35℃1℃修改为36℃+1℃;将EC培养温度 45. 5 ℃±0. 2 ℃(一般食品)和 44. 5 ℃±0. 2 ℃(贝类)统一为 44. 5 ℃±o.2℃
本标准的第法与 AOAC方法的上要区别是:将样品制备时取样50g(或50mL)修改为25g(或25mL);将培养温度35℃十1℃修改为36℃±1℃。本标准的附录 A.附录 B 为规范性附录。本标准电中华人民法和国卫生部提出并归。本标准由中华人民共和国卫生部负责解释。本标准负责起草单位:中国疾病预防控制中心营养与食品安全所。本标准参与起草单位:中华人民共和国内蒙古出人境检验检疫局、江苏省疾病预防控制中心、上海市疾病预防控制中心、中华人民共和国辽宁出人境检验检疫局。本标准主要起草人:刘秀梅、刘中学、袁宝君、刘弘、陈敏卢行安、田静。1
1范围
食品卫生微生物学检验
大肠杆菌计数
木标雄规定了食晶中大肠杆菌计数的法。本标谁适用于各类食品中大肠杆菌的计数,其中第二法不适用于贝类产品。2术语和定义
下列术语和定义适用于本标准。2.1
GB/T 4789.38—2008
大肠杆茵Escherichia coli
广泛存在于人和温血动物的肠道中,能够在44.5℃发酵乳糖产酸气,IMViC(靛基质,甲基红,VP试验、柠檬酸盐)生化试验为十十二一或一十一一的革兰氏阴性析菌。以此作为粪便污染指标来评价食品的卫生状况,推断食品中肠道致病菌污染的可能性。2.2
最可能数
most probable number; MPN
基于泊松分布的·-种间接计数方法3设备和材料
除微生物实验室常规火菌及培养设备外,其他设备和材料如下:3.1恒温培养箱:36℃±1℃。
3. 2 冰箱:2 ℃~5℃
3.3恒温水裕箱:44.5℃±0.2℃。3.4天平:感量0. 1 g。
3.5均质器。
3.6振荔器。
3.7无菌吸管:1mL(具0.01mL刻度)、10mL(具0.1mL刻度)或微量移液器及吸头:3.8无菌锥形瓶:容量500ml。
3. 9无菌培养血;直径 90 mm
3.10pH计或pH比色管或精密pH试纸,3.11菌落计数器或PctrifilmTm1>自动判读仪。3.12紫外灯:波长360nm~366nm,功率≤6W。A培养基和试剂
4.1月桂基磺酸盐胰蛋白陈(laurylsul(atetryptose,LST)肉汤:见第A,1章。4.2EC肉汤(E.coibroth):见第A.2章。4.3蛋白陈水:见第A.3章,
4.4缓冲葡荷糖蛋白陈水(MR-VP实验用):见第A.1章。4.5Korser柠檬酸盐肉汤:见第A,5章。PetrifilnTu是由3M公司提供的产品的商品名。给出这一信息是为了方便本标准的使用者,并不表示对该产1)
品的认可。如果其他等效产品具有相同的效果,则可使用这些等效的产品。品成伴网ht
GB/T 4789.38—2008
磷酸盐缓冲腋:见第A.6章。
伊红美蓝(easin mcthylene bilue,EMB)琼脂:见第 A.7章。营养琼脂斜面:见第 A,8章。
4.9结晶紫中性红胆盐(violetredbilc,VRB)琼脂:见第A,9章。VRB-MUG琼脂:见第A.10章。
革兰氏染色液:见第A.11章。
Kovars 靛基质试剂:见第 A. 12 章。甲基红指示剂:见第A.13章。
Voges-pros kauer(V-P)试剂:见第 A. 14 。无菌生理盐水,称取8.5g氯化钠溶于1000mL蒸馏水中,121℃高压灭菌15min。tmol/L氢氧化钠(NaOH):称取40g氢氧化钠溶于1000mL蒸馏水中。Imo1/L盐酸(HCl):移取浓盐酸90ml用蒸馏水稀释至I000mL。PctrililmEM大肠菌群/大肠杆菌检验澍试片。第一法大肠杆菌MPN计数
5检验程序
见图1。
25g(或25 ml)样品1-225 mL稀液。均质10倍系列稀释
选择适宜3个连续稀释度的样品勾液,接种LST肉汤管36 ℃+1 ℃
不产气
48h±2h
EC肉汤
44. 5±0. 2℃
不产气
48b±2h
EMB平板划线
36 ℃±1 ℃
18h~24h
可蜓菌落移种营养琼胎斜面或平板36 ±1 ℃
18h-24h
IMViC生化试验,求兰氏染色
阴性管
查MPN表
报告结果
图1大肠杆菌MPN计数法检验程序2
http:
rungfooc
ate net
阳性管
6操作步骤
6.1样品的稀释
GB/T 4789.38—2008
6.1.1固体和半固体样品:以菌操作取25g样品,置盛有225mL磷酸盐缓冲液的无菌均质杯内80001/min~10000r/min均质1min~2min,制成1:10样品勾液,或置盛有225mL磷酸盐缓冲液的无菌均质袋中,用拍击式均质器拍打1min~2min制成1:10的样品勾液。6.1.2液体样品:以无菌吸管吸取样品25mL置盛有225ml.磷酸盐缓冲液的无菌锥形瓶(瓶内预置适当数量的玻璃珠)中,充分振摇,制成1:10的样品勾液。6.1.3样品匀液的PH值应在6.5~~7.5之间,必要时分别用1ol/L氢氧化钠
每个样品,选择3个适宜的连续稀释度的样品勾液(液体样品可以选择原液)。每个稀释度接种3管月桂基磺酸盘胰蛋白陈(LST)肉汤,每管接种1mL(如接种量超过1ml则用双料LST肉汤)。36℃士1℃培养24h士2h观察小倒管内是否有气泡产生,如未产气则继续培养垒48h土2h,记录在24h~48h内产气的LST肉汤管数。如所有LST肉汤管均末产气,即可报告大肠杆菌MPN结果,如有产气者,则进行复发酵试验。6,3复发酵试验
用接种环分别从所有培养18h土2h内发酵产气的1.ST肉汤管中取培养物1环,移种十已提前预温至45℃的EC肉汤管中,放人带盖的14.5℃三0.2℃水浴箱内。水裕的水面应高于肉汤培养基液面,培养24h士2h,检查小倒管内是否有气泡产生,如末产气则继续培养至48h土21。记录在24h利48h内产气的EC肉汤管数。如所有EC肉汤臂均未产气,即可报告大肠杆菌MPN结果,如有产气者则进行EMB平板分离培养。
6.4伊红美蓝平板分离培养
轻轻振摇各产气管,用接种环取培养物划线分别接种于EMB平板,36℃±1℃培养18h~24h检验平板上有无具黑色中心有光泽或尤光泽的典型菌落。6.5营养琼脂斜面或平板培养
从每个平板[-挑5个典型菌落,如无典型菌落则挑取可疑菌落。用接种针接触菌落中心部位,移种到营养琼脂斜面或平板13GC土1℃,培养18h~24h。取培养物进行革兰氏染色和生化试验。6.6生化试验
6.6.1靛基质试验:将培养物接种蛋白陈水,36℃土1C培养24h土2h后,加Kovacs靛基质试剂0.2ml0.3mL,上层出现红色为靓基质阳性反应,6.6.2MR-VP试验:将培养物接种MR-VP培养基,36℃土1C培养48h士2h。移取培养物1mL.至13mm×100mm试管中,加5%α-素酚乙醇溶液0.6mL、40%氢氧化钾溶液0.2ml.和少许肌酸结晶,振摇试管后静置2h,如出现红色,为VP试验阳性。将MRVP培养液的剩余部分再培养48h后滴加5滴甲基红指示剂。培养物变红色,为甲基红试验阳性,若变黄色则为阴性反应。6.6.3柠檬酸盐利用试验:将培养物接种Koscr氏柠檬酸盐肉汤,36℃+1℃培养96h士2h,记录有无细菌生长。
GB/T 4789.38—2008
大肠杆菌与非人肠杆菌的生化鉴别见表1.表1大肠杆菌与非大肠杆菌的生化鉴别靛基质(I)
甲基红(MR)
VP 试验(VP)
柠檬酸盐(C)
墨延(型别)
典型大托菌
非典型大肠杆菌
典型中间型
非典型中间型
典型产气肠杆菌
非典型产气肠杆
注1:如出现表1以外的生化反应类型,表明培养物可能不纯,应重新刘线分离,必要时做重复试验。注2:生化试验也可以选用VITEKGNI鉴延卡、API20E等方法,按照产品说明书进行操作。6.7大肠杆菌MPN计数的报告
大肠杆菌为革兰氏阴性无芽胞杆菌,发酵乳糖、产酸、产气,IMViC生化试验为+:+一一或。只要有1个菌落鉴定为大肠杆菌,其所代表的LST肉汤管即为大肠杆菌阳性。依据LST肉汤阳性管数查MPV表(见附录B),报告每克(或亳升)样品中大肠杆菌MPN值。大肠杆菌VRB-MUG乎板计数法
第二法
检验程序
见图2。
25g(或25mL)样品+225mL稀释液,均质10倍系列稀释
选择2个3个适宜连续稀释度的样品液,按种VRB-MUJG半板36 ℃±1 ℃
18 h~21 h
紫外灯照射,计数发荧光菌落
报告结果
图2大肠杆菌VRB-MUG平板计数法检验程序8样品稀释
按6.1进行。
9检验
GB/T 4789.38—2008
选取2个-3个适宜的连续稀释度的样品句液,每个稀释度分别取1mL注人两个无菌平。另取1 mL稀释液注人一个尤菌平血中,作空白对照:将 45 ℃土0. 5 ℃的 VRB琼脂 10 mL~15 mL 倾注于每个平Ⅲ中。小心旋转平Ⅲ,将培养基与样品匀液充分混勾。待琼脂凝固后,再加 3 nL~4InL VRBMUG琼脂盖平板表层。疑固后翻转平板,36℃土1℃培养18h~24h。选择菌落数为10~100的平板,暗窄中360nm~366nm波长紫外灯照射下,计数平板上发浅蓝色荧光的菌落,检验时用已知MUG阳性菌株(如大肠杆菌ATCC25922)和产气肠杆菌(如ATCC13048)做阳性和阴性对照。
10大肠杆菌平板计数的报告
两个半板上发荧光菌落数的平均数乘以稀释倍数,报告每克(或毫升)样品中大肠杆菌数,以CFU/g(CFU/mlL)表示.
第三法大肠杆菌PelrifilimrM测试片计数法11检验程序
见图3。
25g(或25ml.)样品+225mL稀释液,均质10倍系列稀释
选择适宜2个~~3个连续稀释度的样品勾液,接种Pctrifilm:M测试36 ℃±1 ℃
24h±2 h或48 h±2 h
计数Petrifilm\hi测试片上的蓝色借气泡菌报告结果
图3大肠杆菌PetrifilmM测试片计数法检验程序12样品稀释
按6.1进行。
13检验
13.1接种和培养
选取2个~3个适宜的连续稀释度的样品匀液,每个稀释度接种两张测试片。将测试片置于平坦实验台面,揭开上层膜,用吸管吸取样品匀液1mL垂直滴加在测试片的中央,将上层膜缓慢益下,避免5
ht
GB/T 4789.38—2008
气泡产生和.1-层膜直接落下,将压板(平面底朗下)放置在上层膜中央处,轻轻地乐下,使样品匀液均勾覆盖于圆形的培养膜表面,切勿扭转压板。拿起压板,静置至少1min以使培养基凝固。将测试片的透明面朝上置于培养箱内,堆叠片数不超过20片,36℃士1℃培养。肉、家禽和水产品,培养时间为24h士2h;其他食品,培养时间为48 h士2h,13.2判读
肉服观察计数,或用菌落计数器、放大镜.PetririlrnrM自动判读仪计数。蓝色有气泡的菌葬确认为人肠杆菌,不论蓝色的深浅,部分蓝色的带气泡菌落也判定为大肠杆菌。圆形培养膜边缘及边缘以外的菌落不计数。当测试片出现大量气泡、不明显的小菌落,培养区呈蓝色时,需要进一步稀释样品勾液,重新检验。
14大肠杆菌测试片计数的报告
选择菌落数在15~150之间的稀释度,两张测试片菌落平均数乘以稀释倍数,即为每克(或毫升)样品巾大肠杆菌数,以CFU/g(CFU/mL)表示。如果所有稀释度测试片七的菌落数郁小于15,计数最低稀释度测试片上的平均菌落数乘以稀释倍数报;如果所有稀释度的测试片上均无菌落生长,以“小于1乘以最低稀释倍数”报告;如果所有稀释度的菌落数都人于150,计数最高稀释度测试片上的平均菌落数乘以稀释倍数报告。计数菌落数大于150个的测试片时,可计数·个或两个具有代表性的方格内的菌落数,换算成单个方格内的菌落数后乘以20,即为测试片1估算的菌落数(圆形生长面积为20cm)。6
A.1月桂基磺酸盐胰蛋白陈(LST)肉汤A.1.1成分
胰蛋白陈或胰酪陈
氯化钠
磷酸氢二钾(K,HPO,)
磷酸二氨钾(KH,PO)
月桂基硫酸钠
蒸馏水
pH6.8±0.2
A. 1.2制法
附录A
(规范性附录)
培养基和试剂
1 000 nL
GB/T4789.38—2008
将上述成分溶解于蒸馅水中,调节pII。分装到有玻璃小倒管的试管中,每管10mL,121C高压灭菌 15 min。
制备双料LST肉汤时,除蒸馏水外其他成分加倍。A,2EC肉汤
A.2.1戒分
胰蛋白豚或胰酪陈
3号胆盐或混合脏盐
磷酸氢二钾(K.HPO,)
磷酸二氢钾(KH,PO)
氯化钠
蒸馏水
pH6. 9±0.1
A.2.2制法
1 000.0 mL
将上述成分溶解于蒸馏水中,调节pH,分装于有倒立小发酵管的试管中,每管8mL。121℃高压灭菌 15 min。
A.3蛋白陈水
A,3.1 成分
膀陈或胰酪陈
蒸馏水
pH6. 9±0. 2
A.3.2制法
1 000. 0 ml
加热搅拌解映豚或胰酪陈于蒸馏水中。分装试管,每管5mL。121℃高压灭菌15tmin。7
http:/
ate net
GB/T 4789.38200B
A, 4缓冲葡萄糖蛋白陈水(MR-VP 实验用)A.4.1成分
葡萄糖
癣酸氨二钾(K,HPO,)
蒸馏水
pH6.9±0.2
A.4.2制法
1 000.0 mL
将上述成分溶于蒸馅水中,调节pH,分装试管,121℃高压灭菌15min。A.5Korsr氏柠檬酸盐肉汤
A.5.1成分
磷酸氢铵钠(NaNHHPO4·4H,O)
磷酸氨一钾(KHPO
硫酸镁(MgS0,·7H,0)
柠檬酸钠(含2H,O)
蒸馏水
pH6.7±0.2
A.5.2制法
1 000. 0 mL
将上述成分溶解于蒸馏水中,调节pH,分装试管,每管10mL,121℃高压炎菌15min。A.6磷酸盐缓冲液
A.6.1成分
磷酸二氨钾(KH,PO,)
蒸馏水
A, 6.2制法
500 mL
贮存液:称取34.0g的磷酸二氢钾溶于500mL蒸馏水中,用大约175mL的1mol/L氢氧化钠溶液调节pH至7.2.用蒸馏水稀释至1000mL后贮存于冰箱。稀释液:取贮存液1.25mL,用蒸馏水稀释至1000ml,分装于适宜容器中,121℃高压灭菌15min。
伊红美蓝琼脂(EMB)
A.7.1成分
蛋白豚
磷酸氢二钾(K,HPO)
伊红水溶液)
蒸馏水
pH 7. 1±0.2
0. 1 多或 2%水溶液 20 mL
0.065g或0.5%水溶液13ml.
1 000.0 mL
品成伴网httn
A.7.2制法
GB/T 4789.38—2008
在1 000 mL 蒸馏水中煮沸溶解蛋白陈,磷酸盐和琼脂,加水补足。分装于三角烧瓶中,钙瓶100 mL 或 200 mL,调节 pH,高压灭菌。使用前将琼脂融化,于每 1U0 mL.琼脂中加5 ml. 灭菌的 20%乳糖溶液,2 mL的 2%的伊红 水溶液和 1. 3 mL 0. 5%的美蓝水溶液,摇勺,冷至 45 ℃~50 ℃倾注平血。
A.8营养琼脂斜面
A.8.1成分wwW.bzxz.Net
牛肉膏
蛋白陈
蒸馏水
pH7.3±0.1
A.,B.2制法
1 000. 0 mL
将上述成分加于蒸馏水中,点沸溶解,调节pH,分装合适的试管,121℃高压灭菌15min。灭菌后摆成斜面备用。
A, 9结晶紫中性红胆盐(VRB)琼脂A. 9. 1 成分
蛋白膝
酵母膏
氯化钠
胆盐或3号服盐
中性红
结晶紫
蒸馏水
pH7.4±0. 1
A.9.2制法
15 g~18 g
1 000.0 mL
将上述成分溶于蒸水中,静置儿分钟,充分揽拌,调节pH。煮沸2min,将培养基冷至45℃~50℃癫注平板,临用时制备,不得超过3h。A.10VRB-MUG琼脂
A.10.1成分
蛋白陈
酵母湾
氯化钠
胆盐或 3号胆盐
中性红
结晶紫
15 g-18 g
http:
rungfooc
atenet
小提示:此标准内容仅展示完整标准里的部分截取内容,若需要完整标准请到上方自行免费下载完整标准文档。
标准图片预览:




- 热门标准
- 国家标准(GB)
- GB/T2828.1-2012 计数抽样检验程序 第1部分:按接收质量限(AQL)检索的逐批检验抽样计划
- GB/T18204.4-2000 公共场所毛巾、床上卧具微生物检验方法细菌总数测定
- GB/T23892.3-2009 滑动轴承 稳态条件下流体动压可倾瓦块止推轴承 第3部分:可倾瓦块止推轴承计算的许用值
- GB/T11839-1989 二氧化铀芯块中硼的测定 姜黄素萃取光度法
- GB/T1804-2000 一般公差 未注公差的线性和角度尺寸的公差
- GB15603-2022 危险化学品仓库储存通则
- GB/T5738-1995 瓶装酒、饮料塑料周转箱
- GB/T7433-1987 对称电缆载波通信系统抗无线电广播和通信干扰的指标
- GB/T21238-2007 玻璃纤维增强塑料夹砂管
- GB/T28809-2012 轨道交通 通信、信号和处理系统 信号用安全相关电子系统
- GB/T9239-1988 刚性转子平衡品质 许用不平衡的确定
- GB/T15917.3-1995 金属镝及氧化镝化学分析方法 对氯苯基荧光酮--溴化十六烷基三甲基胺分光光度法测定钽量
- GB5793-1986 字鼓式行式打印机色带卷轴基本尺寸
- GB/T11813-2008 压水堆燃料棒氦质谱检漏
- GB/T38780-2020 竹席
- 行业新闻
请牢记:“bzxz.net”即是“标准下载”四个汉字汉语拼音首字母与国际顶级域名“.net”的组合。 ©2025 标准下载网 www.bzxz.net 本站邮件:bzxznet@163.com
网站备案号:湘ICP备2025141790号-2
网站备案号:湘ICP备2025141790号-2