【国家标准(GB)】 蜂蜜中土霉素、四环素、金霉素、强力霉素残留量的测定方法液相色谱-串联质谱法
本网站 发布时间:
2024-07-18 08:39:46
- GB/T18932.23-2003
- 现行
- 点击下载此标准
标准号:
GB/T 18932.23-2003
标准名称:
蜂蜜中土霉素、四环素、金霉素、强力霉素残留量的测定方法液相色谱-串联质谱法
标准类别:
国家标准(GB)
标准状态:
现行-
发布日期:
2003-12-30 -
实施日期:
2004-06-01 出版语种:
简体中文下载格式:
.rar.pdf下载大小:
168.78 KB
手机扫码下载更方便
点击下载
标准简介:
标准下载解压密码:www.bzxz.net
GB/T 18932的本部分规定了蜂蜜中土霉素、四环素、金霉素、强力霉素残留量液相色谱-串联质谱测定方法。本部分适用于蜂蜜中土霉素、四环素、金霉素、强力霉素残留量的测定。本部分的方法检出限:土霉素、四环素为0.001mg/kg;金霉素、强力霉素为0.002mg/kg。 GB/T 18932.23-2003 蜂蜜中土霉素、四环素、金霉素、强力霉素残留量的测定方法液相色谱-串联质谱法 GB/T18932.23-2003
部分标准内容:
GB/T18932.23-—2003
GB/T18932的本部分修改采用加拿大标准ACC-042-V1.0《蜂蜜中四环素残留量测定——一液相色谱质谱法》,修改的主要内容是:淋洗液由甲醇改为乙酸乙酯;
-增加了羧酸型阴离子交换柱净化;单四极杆质谱检测器改为串联四极杆质谱检测器。本部分的附录A和附录B为资料性附录。本部分由国家质量监督检验检疫总局提出。本部分由中华全国供销合作总社归口。本部分起草单位:中华人民共和国秦皇岛出人境检验检疫局。本部分主要起草人:庞国芳、张进杰、曹彦忠、贯光群、范春林、刘永明、李学民、石玉秋。本部分系首次发布的国家标准。1
1范围
蜂蜜中土霉素、四环素、金霉素、强力霉素残留童的测定方法
液相色谱-串联质谱法
GB/T18932.23—2003
GB/T18932的本部分规定了蜂蜜密中土霉素、四环素、金霉素、强力霉素残留量液相色谱-串联质谱测定方法。
本部分适用于蜂蜜中土霉素、四环素、金霉素、强力霖素残留量的测定。本部分的方法检出限:土霉素、四环素为0.001.mg/kg;金霉素、强力霉素为0.002mg/kg。2规范性引用文件
下列文件中的条款通过GB/T18932的本部分的引用而成为本部分的条款。凡是注日期的引用文件,其随后所有的修改单(不包括勘误的内容)或修订版均不适用于本部分,然而,鼓励根据本部分达成协议的各方研究是否可使用这些文件的最新版本。凡是不注日期的引用文件,其最新版本适用于本部分。
GB/T6379测试方法的精密度通过实验室间试验确定标准测试方法的重复性和再现性(GB/T6379--1986,neq ISO 5725:1981)GB/T6682分析实验室用水规格和试验方法(GB/T6682-1992,neqISO3696:1987)3原理
试样中四环素族抗生素残留,用0.1mol/LNazEDTA-Mcllvaine(pH=4.0士0.05)缓冲溶液提取提取液经离心后,上清液用OasisHLB或相当的固相萃取柱和阴离子交换柱净化,液相色谱-串联质谱仪测定,外标法定量。
4试剂和材料
除另有说明外,所用试剂均为分析纯,水为GB/T6682规定的一级水。4.1甲醇:色谱纯。
4.2乙睛:色谱纯。
4.3乙酸乙酯:色谱纯。
4.4磷酸氢二钠(NazHPO·2H,O):优级纯。4.5柠檬酸(CHgO·H2O)。
4.6乙二胺四乙酸二钠(Na2EDTA·2H2O)。4.7草酸。
磷酸氢二钠溶液:0.2mol1/L。称取28.41g磷酸氢二钠(4.4),用水溶解,定容至1000mL。4.9柠檬酸溶液:0.1mol/L。称取21.01g柠檬酸(4.5),用水溶解,定容至1000mL。4.10Mcllvaine缓冲溶液:将1000mL0.1mol/L柠檬酸溶液(4.9)与625mL0.1mol/L磷酸氢二钠溶液(4.8)混合,必要时用NaOH或HCl调pH=4.0±0.05。4.11NazEDTA-Mcllvaine缓冲溶液:0.1mol/L。称取60.5g乙二胺四乙酸二钠(4.6)放人1625mLMcllvaine缓冲溶液(4.10)中,使其溶解,摇勾。1
GB/T 18932.23—2003
4.12甲醇+水(1+19):量取5mL甲醇(4.1)与95mL水混合。4.13OasisHLB固相萃取柱或相当者:500mg,6mL。使用前分别用5mL甲醇和10mL水预处理,保持柱体湿润。
4.14阴离子交换柱:羧酸型,500mg,3mL。使用前用5mL乙酸乙酯预处理,保持柱体湿润。4.15土霉素、四环素、金霉素、强力霉素标准物质:纯度≥95%。4.16土霉素、四环素、金霉素、强力莓素标准储备溶液:0.1mg/mL。准确称取适量的土霉素、四环素、金霉素、强力霉素标准物质(4.15),分别用甲醇配成0.1mg/mL的标准储备液。储备液贮存在一18℃冰柜中。
4.17土霉素、四环素、金霉素、强力霖素基质混合标准工作溶液:根据需要吸取适量土霉素、四环素、金素、强力霉素标准储备溶液(4.16),用空白样品提取液稀释成适当浓度的基质混合标准工作溶液,基质混合标准工作溶液在4℃保存,可使用三天。5仪器
5.1液相色谱-串联四极杆质谱仪,配有电喷雾离子源。5.2分析天平:感量0.1mg和0.01g各一台。5.3液体混匀器。
5.4固相萃取真空装置。
5.5贮液器:50mL。
5.6微量注射器:25μL,100μL。5.7刻度样品管:5mL,精度为0.1mL。5.8真空泵:真空度应达到80kPa。5.9离心管:50mL。
5.10平底烧瓶:100mL。
5.11pH计:测量精度±0.02。
6试样的制备与保存
6.1试样的制备
对无结晶的实验室样品,将其搅拌均勾。对有结晶的样品,在密闭情况下,置于不超过60℃的水浴中温热,振荡,待样品全部融化后揽匀,迅速冷却至室温。分出0.5kg作为试样。制备好的试样置于样品瓶中,密封,并做上标记。
6.2试样保存
将试样于常温下保存。
7测定步骤
7.1提取
称取6g试样(精确到0.01g)置于150mL三角瓶中,加人30mLNazEDTA-Mcllvaine缓冲溶液(4.11)于液体混勾器上快速混合1min,使试样完全溶解。样液倒人50mL离心管中,以3000r/min离心5min,待净化。
7.2净化
将上清液(7.1)移至下接OasisHLB柱(4.13)的贮液器中,以小于等于3mL/min通过Oasis固相萃取柱后,用5mL甲醇十水(4.12)洗柱,弃去全部流出液。在65kPa的负压下,减压抽干20min,最后用15mL乙酸乙酯(4.3)洗脱,收集洗脱液于100mL圆底烧瓶中。按上述方法使洗脱液(7.2)在减压情况下以小于等于3mL/min的流速通过阴离子交换柱(4.14),2
GB/T 18932.23—2003
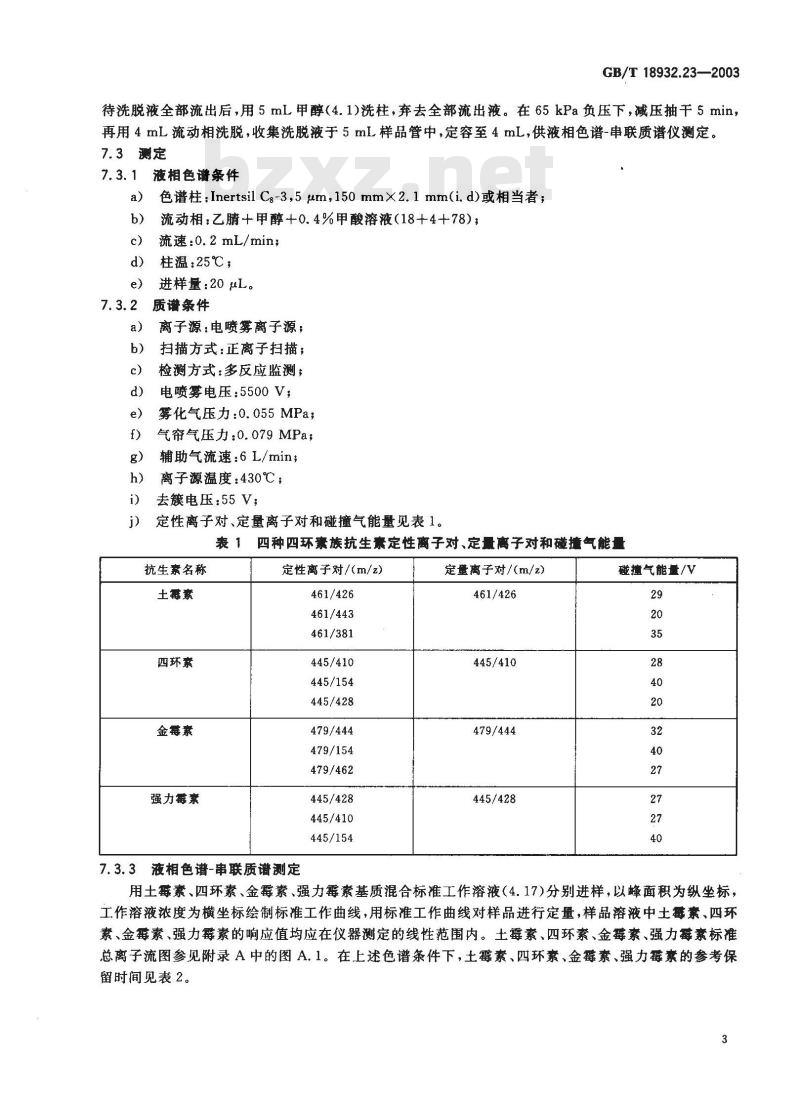
待洗脱液全部流出后,用5mL甲醇(4.1)洗柱,弃去全部流出液。在65kPa负压下,减压抽干5min,再用4mL流动相洗脱,收集洗脱液于5mL样品管中,定容至4mL,供液相色谱-串联质谱仪测定。7.3测定
7. 3. 1液相色谱条件
色谱柱:Inertsil Cg-3,5μm,150mmX2.1mm(i.d)或相当者;流动相:乙腈+甲醇+0.4%甲酸溶液(18+4+78);流速:0.2mL/min;
柱温:25℃;
进样量:20μL。
质谱条件
离子源:电喷雾离子源;
扫描方式:正离子扫描;
检测方式:多反应监测;
电喷雾电压:5500V;
雾化气压力:0.055MPa;
气帘气压力:0.079MPa;
辅助气流速:6L/min;
离子源温度:430℃;
去簇电压:55V;
定性离子对、定量离子对和碰撞气能量见表1。表1四种四环素族抗生素定性离子对、定量离子对和碰撞气能量抗生素名称
土覆素
四环系
金霉素
强力霉素
定性离子对/(m/2)
461/426
461/443
461/381
445/410
445/154
445/428
479/444
479/154
479/462
445/428
445/410
445/154
7.3.3液相色谱-串联质谱测定
定量离子对 /(m/ 2)
461/426
445/410
479/444
445/428
碰撞气能量/V
用土酶素、四环素、金霉素、强力霉素基质混合标准工作溶液(4.17)分别进样,以蜂面积为纵坐标,工作溶液浓度为横坐标绘制标准工作曲线,用标准工作曲线对样品进行定量,样品溶液中土霉素、四环素、金霉素、强力霉素的响应值均应在仪器测定的线性范围内。土霉素、四环素、金霉素、强力霉素标准总离子流图参见附录A中的图A.1。在上述色谱条件下,土霉素、四环素、金霉素、强力霉素的参考保留时间见表2。
GB/T 18932.23—2003
抗生素名称
土舞素
四环素
7.4平行试验
表 2四种四环素族抗生素参考保留时间保留时间/min
按以上步骤,对同一试样进行平行试验测定。7.5空白试验
除不称取试样外,均按上述步骤同时完成空白试验。8 结果计算
结果按式(1)计算:
式中:
抗生素名称
金霉素
强力霉素
X—试样中被测组分残留量,单位为毫克每千克(mg/kg);从标准工作曲线得到的被测组分溶液浓度,单位为微克每毫升(μg/mL);V—-样品溶液最终定容体积,单位为毫升(mL);m—样品溶液所代表最终试样的质量,单位为克(g)。注:计算结果应扣除空白值。
9精密度
保留时间/min
本部分的精密度数据是按照GB/T6379的规定确定的,重复性和再现性的值以95%的可信度来计算。
9. 1 重复性
在重复性条件下,获得的两次独立测试结果的绝对差值不超过重复性限(r),蜂蜜中土霉素、四环素、金素、强力霉素含量范围及重复性方程见表3。如果差值超过重复性限,应舍弃试验结果并重新完成两次单个试验的测定。9.2再现性
在再现性条件下,获得的两次独立测试结果的绝对差值不超过再现性限(R),蜂蜜中土霉素、四环素、金霉素、强力霉素的含量范围及再现性方程见表3。表3含量范围及重复性和再现性方程名称
土霉素
四环素
金霉素
强力霉素
含量范围/(mg/kg)
0. 002~0.100
0. 002~0. 100
0. 002-~0. 100
0.002~0.100
注:m为两次测定结果的算术平均值。4
重复性限r
Igr= 0. 966 81gm--0.868 6
lgr=0. 948 4lgm-0. 837 0
lgr=0. 839 5lgm—1. 087 2
lgr0. 920 9lgm-0. 846 2
再现性R
lgR=1. 009 6lgm--0. 659 7
IgR=1, 161 1lgm--0. 231 7
lgR=0. 906 0lgm-0. 813 6
IgR=0. 989 9lg m-0. 650 4
附黎A
(资料性附录)
标准物质总离子流图
土霉素、四环素、金霉素、强力霉素标准物质总离子流图,见图A.1。5000免费标准bzxz.net
2000手
GB/T18932.23--2003
3. 33 min 为土掌素
3. 89 min 为四环素
8. 04 min 为金素
12. 07 min 为强力霉素
15t/min
GB/T18932.23--2003
附录B
(资料性附录)
回收率
本部分中土霉素、四环素、金霉素、强力霉素添加浓度及其平均回收率的试验数据见表B.1。表 B. 1土雾素、四环素、金霉素、强力霉素添加浓度及其平均回收率的试验数据药物名称
土筝素
四环素
金霉素
强力霉素
添加浓度/(mg/kg)
平均回收率/(%)
GB/T18932的本部分修改采用加拿大标准ACC-042-V1.0《蜂蜜中四环素残留量测定——一液相色谱质谱法》,修改的主要内容是:淋洗液由甲醇改为乙酸乙酯;
-增加了羧酸型阴离子交换柱净化;单四极杆质谱检测器改为串联四极杆质谱检测器。本部分的附录A和附录B为资料性附录。本部分由国家质量监督检验检疫总局提出。本部分由中华全国供销合作总社归口。本部分起草单位:中华人民共和国秦皇岛出人境检验检疫局。本部分主要起草人:庞国芳、张进杰、曹彦忠、贯光群、范春林、刘永明、李学民、石玉秋。本部分系首次发布的国家标准。1
1范围
蜂蜜中土霉素、四环素、金霉素、强力霉素残留童的测定方法
液相色谱-串联质谱法
GB/T18932.23—2003
GB/T18932的本部分规定了蜂蜜密中土霉素、四环素、金霉素、强力霉素残留量液相色谱-串联质谱测定方法。
本部分适用于蜂蜜中土霉素、四环素、金霉素、强力霖素残留量的测定。本部分的方法检出限:土霉素、四环素为0.001.mg/kg;金霉素、强力霉素为0.002mg/kg。2规范性引用文件
下列文件中的条款通过GB/T18932的本部分的引用而成为本部分的条款。凡是注日期的引用文件,其随后所有的修改单(不包括勘误的内容)或修订版均不适用于本部分,然而,鼓励根据本部分达成协议的各方研究是否可使用这些文件的最新版本。凡是不注日期的引用文件,其最新版本适用于本部分。
GB/T6379测试方法的精密度通过实验室间试验确定标准测试方法的重复性和再现性(GB/T6379--1986,neq ISO 5725:1981)GB/T6682分析实验室用水规格和试验方法(GB/T6682-1992,neqISO3696:1987)3原理
试样中四环素族抗生素残留,用0.1mol/LNazEDTA-Mcllvaine(pH=4.0士0.05)缓冲溶液提取提取液经离心后,上清液用OasisHLB或相当的固相萃取柱和阴离子交换柱净化,液相色谱-串联质谱仪测定,外标法定量。
4试剂和材料
除另有说明外,所用试剂均为分析纯,水为GB/T6682规定的一级水。4.1甲醇:色谱纯。
4.2乙睛:色谱纯。
4.3乙酸乙酯:色谱纯。
4.4磷酸氢二钠(NazHPO·2H,O):优级纯。4.5柠檬酸(CHgO·H2O)。
4.6乙二胺四乙酸二钠(Na2EDTA·2H2O)。4.7草酸。
磷酸氢二钠溶液:0.2mol1/L。称取28.41g磷酸氢二钠(4.4),用水溶解,定容至1000mL。4.9柠檬酸溶液:0.1mol/L。称取21.01g柠檬酸(4.5),用水溶解,定容至1000mL。4.10Mcllvaine缓冲溶液:将1000mL0.1mol/L柠檬酸溶液(4.9)与625mL0.1mol/L磷酸氢二钠溶液(4.8)混合,必要时用NaOH或HCl调pH=4.0±0.05。4.11NazEDTA-Mcllvaine缓冲溶液:0.1mol/L。称取60.5g乙二胺四乙酸二钠(4.6)放人1625mLMcllvaine缓冲溶液(4.10)中,使其溶解,摇勾。1
GB/T 18932.23—2003
4.12甲醇+水(1+19):量取5mL甲醇(4.1)与95mL水混合。4.13OasisHLB固相萃取柱或相当者:500mg,6mL。使用前分别用5mL甲醇和10mL水预处理,保持柱体湿润。
4.14阴离子交换柱:羧酸型,500mg,3mL。使用前用5mL乙酸乙酯预处理,保持柱体湿润。4.15土霉素、四环素、金霉素、强力霉素标准物质:纯度≥95%。4.16土霉素、四环素、金霉素、强力莓素标准储备溶液:0.1mg/mL。准确称取适量的土霉素、四环素、金霉素、强力霉素标准物质(4.15),分别用甲醇配成0.1mg/mL的标准储备液。储备液贮存在一18℃冰柜中。
4.17土霉素、四环素、金霉素、强力霖素基质混合标准工作溶液:根据需要吸取适量土霉素、四环素、金素、强力霉素标准储备溶液(4.16),用空白样品提取液稀释成适当浓度的基质混合标准工作溶液,基质混合标准工作溶液在4℃保存,可使用三天。5仪器
5.1液相色谱-串联四极杆质谱仪,配有电喷雾离子源。5.2分析天平:感量0.1mg和0.01g各一台。5.3液体混匀器。
5.4固相萃取真空装置。
5.5贮液器:50mL。
5.6微量注射器:25μL,100μL。5.7刻度样品管:5mL,精度为0.1mL。5.8真空泵:真空度应达到80kPa。5.9离心管:50mL。
5.10平底烧瓶:100mL。
5.11pH计:测量精度±0.02。
6试样的制备与保存
6.1试样的制备
对无结晶的实验室样品,将其搅拌均勾。对有结晶的样品,在密闭情况下,置于不超过60℃的水浴中温热,振荡,待样品全部融化后揽匀,迅速冷却至室温。分出0.5kg作为试样。制备好的试样置于样品瓶中,密封,并做上标记。
6.2试样保存
将试样于常温下保存。
7测定步骤
7.1提取
称取6g试样(精确到0.01g)置于150mL三角瓶中,加人30mLNazEDTA-Mcllvaine缓冲溶液(4.11)于液体混勾器上快速混合1min,使试样完全溶解。样液倒人50mL离心管中,以3000r/min离心5min,待净化。
7.2净化
将上清液(7.1)移至下接OasisHLB柱(4.13)的贮液器中,以小于等于3mL/min通过Oasis固相萃取柱后,用5mL甲醇十水(4.12)洗柱,弃去全部流出液。在65kPa的负压下,减压抽干20min,最后用15mL乙酸乙酯(4.3)洗脱,收集洗脱液于100mL圆底烧瓶中。按上述方法使洗脱液(7.2)在减压情况下以小于等于3mL/min的流速通过阴离子交换柱(4.14),2
GB/T 18932.23—2003
待洗脱液全部流出后,用5mL甲醇(4.1)洗柱,弃去全部流出液。在65kPa负压下,减压抽干5min,再用4mL流动相洗脱,收集洗脱液于5mL样品管中,定容至4mL,供液相色谱-串联质谱仪测定。7.3测定
7. 3. 1液相色谱条件
色谱柱:Inertsil Cg-3,5μm,150mmX2.1mm(i.d)或相当者;流动相:乙腈+甲醇+0.4%甲酸溶液(18+4+78);流速:0.2mL/min;
柱温:25℃;
进样量:20μL。
质谱条件
离子源:电喷雾离子源;
扫描方式:正离子扫描;
检测方式:多反应监测;
电喷雾电压:5500V;
雾化气压力:0.055MPa;
气帘气压力:0.079MPa;
辅助气流速:6L/min;
离子源温度:430℃;
去簇电压:55V;
定性离子对、定量离子对和碰撞气能量见表1。表1四种四环素族抗生素定性离子对、定量离子对和碰撞气能量抗生素名称
土覆素
四环系
金霉素
强力霉素
定性离子对/(m/2)
461/426
461/443
461/381
445/410
445/154
445/428
479/444
479/154
479/462
445/428
445/410
445/154
7.3.3液相色谱-串联质谱测定
定量离子对 /(m/ 2)
461/426
445/410
479/444
445/428
碰撞气能量/V
用土酶素、四环素、金霉素、强力霉素基质混合标准工作溶液(4.17)分别进样,以蜂面积为纵坐标,工作溶液浓度为横坐标绘制标准工作曲线,用标准工作曲线对样品进行定量,样品溶液中土霉素、四环素、金霉素、强力霉素的响应值均应在仪器测定的线性范围内。土霉素、四环素、金霉素、强力霉素标准总离子流图参见附录A中的图A.1。在上述色谱条件下,土霉素、四环素、金霉素、强力霉素的参考保留时间见表2。
GB/T 18932.23—2003
抗生素名称
土舞素
四环素
7.4平行试验
表 2四种四环素族抗生素参考保留时间保留时间/min
按以上步骤,对同一试样进行平行试验测定。7.5空白试验
除不称取试样外,均按上述步骤同时完成空白试验。8 结果计算
结果按式(1)计算:
式中:
抗生素名称
金霉素
强力霉素
X—试样中被测组分残留量,单位为毫克每千克(mg/kg);从标准工作曲线得到的被测组分溶液浓度,单位为微克每毫升(μg/mL);V—-样品溶液最终定容体积,单位为毫升(mL);m—样品溶液所代表最终试样的质量,单位为克(g)。注:计算结果应扣除空白值。
9精密度
保留时间/min
本部分的精密度数据是按照GB/T6379的规定确定的,重复性和再现性的值以95%的可信度来计算。
9. 1 重复性
在重复性条件下,获得的两次独立测试结果的绝对差值不超过重复性限(r),蜂蜜中土霉素、四环素、金素、强力霉素含量范围及重复性方程见表3。如果差值超过重复性限,应舍弃试验结果并重新完成两次单个试验的测定。9.2再现性
在再现性条件下,获得的两次独立测试结果的绝对差值不超过再现性限(R),蜂蜜中土霉素、四环素、金霉素、强力霉素的含量范围及再现性方程见表3。表3含量范围及重复性和再现性方程名称
土霉素
四环素
金霉素
强力霉素
含量范围/(mg/kg)
0. 002~0.100
0. 002~0. 100
0. 002-~0. 100
0.002~0.100
注:m为两次测定结果的算术平均值。4
重复性限r
Igr= 0. 966 81gm--0.868 6
lgr=0. 948 4lgm-0. 837 0
lgr=0. 839 5lgm—1. 087 2
lgr0. 920 9lgm-0. 846 2
再现性R
lgR=1. 009 6lgm--0. 659 7
IgR=1, 161 1lgm--0. 231 7
lgR=0. 906 0lgm-0. 813 6
IgR=0. 989 9lg m-0. 650 4
附黎A
(资料性附录)
标准物质总离子流图
土霉素、四环素、金霉素、强力霉素标准物质总离子流图,见图A.1。5000免费标准bzxz.net
2000手
GB/T18932.23--2003
3. 33 min 为土掌素
3. 89 min 为四环素
8. 04 min 为金素
12. 07 min 为强力霉素
15t/min
GB/T18932.23--2003
附录B
(资料性附录)
回收率
本部分中土霉素、四环素、金霉素、强力霉素添加浓度及其平均回收率的试验数据见表B.1。表 B. 1土雾素、四环素、金霉素、强力霉素添加浓度及其平均回收率的试验数据药物名称
土筝素
四环素
金霉素
强力霉素
添加浓度/(mg/kg)
平均回收率/(%)
小提示:此标准内容仅展示完整标准里的部分截取内容,若需要完整标准请到上方自行免费下载完整标准文档。
标准图片预览:




- 热门标准
- 国家标准(GB)
- GB/T12949-1991 滑动轴承覆有减摩塑料层的双金属轴套
- GB/T38627-2020 信息技术 实时定位 磁定位数据接口
- GB/T1182-2018 产品几何技术规范(GPS) 几何公差 形状、方向、位置和跳动公差标注
- GB/T15349-1994 化学试剂 溴甲酚绿
- GB175-2023 通用硅酸盐水泥
- GB/T8878—2014 棉针织内衣
- GB/T228.1-2021 金属材料 拉伸试验 第1部分:室温试验方法
- GB/T10125-2021 人造气氛腐蚀试验 盐雾试验
- GB/T97.1-2002 平垫圈A级
- GB/T43802-2024 绿色产品评价 物流周转箱
- GB/T7588.1-2020 电梯制造与安装安全规范第1部分:乘客电梯和载货电梯
- GB31094-2014 防爆电梯制造与安装安全规范
- GB9178-1988 集成电路术语
- GB/T42970-2023 半导体集成电路 视频编解码电路测试方法
- GB/T38987-2020 硬质合金螺旋孔棒材
- 行业新闻
请牢记:“bzxz.net”即是“标准下载”四个汉字汉语拼音首字母与国际顶级域名“.net”的组合。 ©2025 标准下载网 www.bzxz.net 本站邮件:wymp4wang@gmail.com