- 您的位置:
- 标准下载网 >>
- 标准分类 >>
- 国家标准(GB) >>
- GB 4789.5-2012 食品微生物学检验 志贺氏菌检验
标准号:
GB 4789.5-2012
标准名称:
食品微生物学检验 志贺氏菌检验
标准类别:
国家标准(GB)
标准状态:
现行出版语种:
简体中文下载格式:
.rar .pdf下载大小:
部分标准内容:
中华人民共和国国家标准
GB4789.52012
食品安全国家标准
食品微生物学检验志贺氏菌检验2012-05-17发布
中华人民共和国卫生部
2012-07-17实施
本标准代替GB/T4789.5-2003《食品卫生微生物学检验本标准与GB/T4789.5-2003相比,主要变化如下:修改了标准名称;
-修改了培养基和试剂;
志贺氏菌检验》。
-修改了操作步骤中增菌部分和生化试验及附加生化试验部分;修改了表2;
-修改了表4。
GB4789.5-2012
1范围
食品安全国家标准
食品微生物学检验志贺氏菌检验本标准规定了食品中志贺氏菌(Shigella)的检验方法本标准适用于食品中志贺氏菌的检验。设备和材料
除微生物实验室常规灭菌及培养设备外,其他设备和材料如下:恒温培养箱:36℃土1℃;
b)冰箱:2℃~5℃;
膜过滤系统;
d)厌氧培养装置:41.5℃±1℃;电子天平:感量0.1g:
显微镜:10×~100×;
均质器;
振荡器:
GB4789.5-2012
无菌吸管:1mL(具0.01mL刻度)、10mL(具0.1mL刻度)或微量移液器及吸头无菌均质杯或无菌均质袋:容量500mL:j)
无菌培养Ⅲ:直径90mm;
pH计或pH比色管或精密pH试纸:m)
全自动微生物生化鉴定系统。
3培养基和试剂
3.1志贺氏菌增菌肉汤-新生霉素:见附录A中A.1。3.2麦康凯(MAC)琼脂:见附录A中A.2、3.3木糖赖氨酸脱氧胆酸盐(XLD)琼脂:见附录A中A.33.4志贺氏菌显色培养基。
3.5三糖铁(TSI)琼脂:见附录A中A.4。3.6营养琼脂斜面:见附录A中A.5。3.7半固体琼脂:见附录A中A.6。3.8葡萄糖铵培养基:见附录A中A.7。3.9尿素琼脂:见附录A中A.8。
3.10β-半乳糖苷酶培养基:见附录A中A.9。3.11氨基酸脱羧酶试验培养基:见附录A中A.10。3.12糖发酵管:见附录A中A.11。3.13西蒙氏柠檬酸盐培养基:见附录A中A.12。3.14粘液酸盐培养基:见附录A中A.133.15蛋白陈水、靛基质试剂:见附录A中A.14。3.16志贺氏菌属诊断血清。
3.17生化鉴定试剂盒。
4检验程序
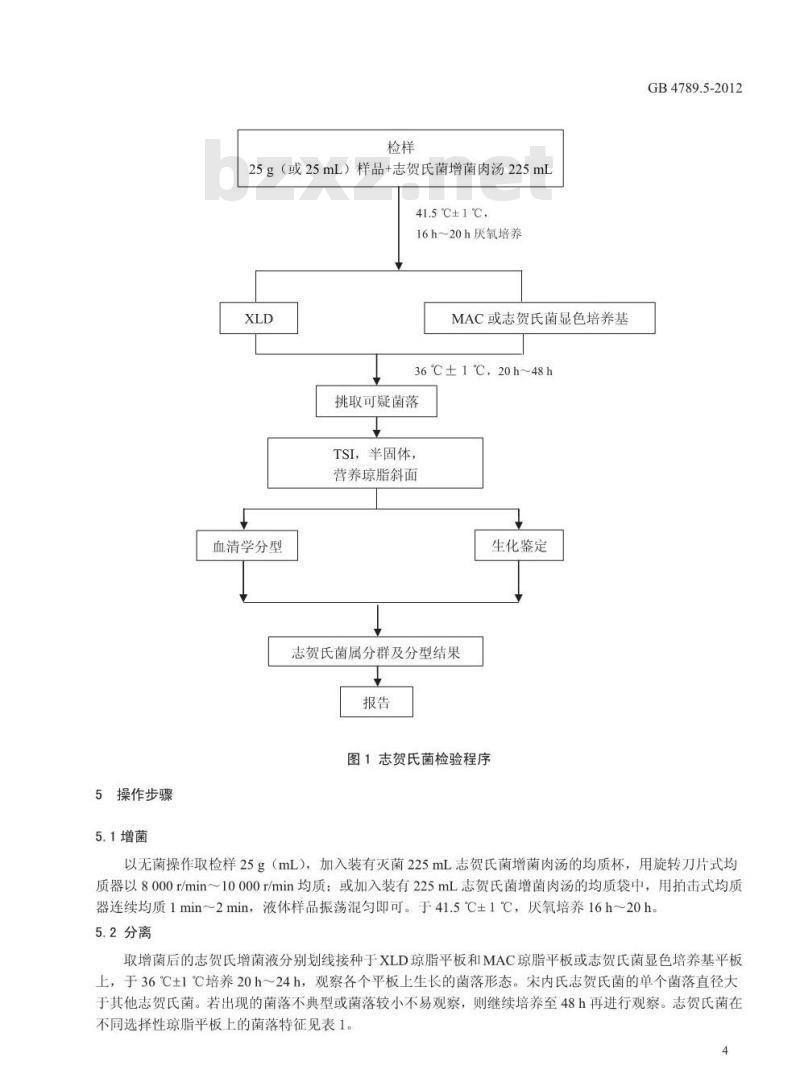
志贺氏菌检验程序见图1。
GB4789.5-2012
5操作步骤
5.1增菌
25g(或25mL)样品+志贺氏菌增菌肉汤225mL41.5℃±1℃
16h~20h厌氧培养
血清学分型
MAC或志贺氏菌显色培养基
36℃±1℃,20h~48h
挑取可疑菌落
TSI,半固体,
营养琼脂斜面
生化鉴定
志贺氏菌属分群及分型结果
图1志贺氏菌检验程序
GB4789.5-2012
以无菌操作取检样25g(mL),加入装有灭菌225mL志贺氏菌增菌肉汤的均质杯,用旋转刀片式均质器以8000r/min~10000r/min均质:或加入装有225mL志贺氏菌增菌肉汤的均质袋中,用拍击式均质器连续均质1min~2min,液体样品振荡混匀即可。于41.5℃±1℃,厌氧培养16h~20h。5.2分离
取增菌后的志贺氏增菌液分别划线接种于XLD琼脂平板和MAC琼脂平板或志贺氏菌显色培养基平板上,于36℃土1℃培养20h~24h,观察各个平板上生长的菌落形态。宋内氏志贺氏菌的单个菌落直径大于其他志贺氏菌。若出现的菌落不典型或菌落较小不易观察,则继续培养至48h再进行观察。志贺氏菌在不同选择性琼脂平板上的菌落特征见表1。4
选择性琼脂平板
MAC琼脂
XLD琼脂
志贺氏菌显色培养基
5.3初步生化试验
志贺氏菌在不同选择性琼脂平板上的菌落特征表1
志贺氏菌的菌落特征
无色至浅粉红色,半透明、光滑、湿润、圆形、边缘整齐或不齐粉红色至无色,半透明、光滑、湿润、圆形、边缘整齐或不齐按照显色培养基的说明进行判定GB 4789.5-2012
5.3.1自选择性琼脂平板上分别挑取2个以上典型或可疑菌落,分别接种TSI、半固体和营养琼脂斜面各管,置36℃土1℃培养20h~24h,分别观察结果。5.3.2凡是三糖铁琼脂中斜面产碱、底层产酸(发酵葡萄糖,不发酵乳糖,蔗糖)、不产气(福氏志贺氏菌6型可产生少量气体)、不产硫化氢、半固体管中无动力的菌株,挑取其5.3.1中已培养的营养琼脂斜面上生长的菌苔,进行生化试验和血清学分型5.4生化试验及附加生化试验
5.4.1生化试验
用5.3.1中已培养的营养琼脂斜面上生长的菌苔,进行生化试验,即β-半乳糖苷酶、尿素、赖氨酸脱羧酶、鸟氨酸脱羧酶以及水杨苷和七叶苷的分解试验。除宋内氏志贺氏菌、鲍氏志贺氏菌13型的鸟氨酸阳性;宋内氏菌和痢疾志贺氏菌1型,鲍氏志贺氏菌13型的β-半乳糖苷酶为阳性以外,其余生化试验志贺氏菌属的培养物均为阴性结果。另外由于福氏志贺氏菌6型的生化特性和疾志贺氏菌或鲍氏志贺氏菌相似,必要时还需加做靛基质、甘露醇、棉子糖、甘油试验,也可做革兰氏染色检查和氧化酶试验,应为氧化酶阴性的革兰氏阴性杆菌。生化反应不符合的菌株,即使能与某种志贺氏菌分型血清发生凝集,仍不得判定为志贺氏菌属。志贺氏菌属生化特性见表2。表2志贺氏菌属四个群的生化特征生化反应
B-半乳糖苷酶
赖氨酸脱羧酶
鸟氨酸脱羧酶
水杨苷
七叶苷
靛基质
甘露醇
棉子糖
A群:疾志贺氏菌
B群:福氏志贺氏菌
C群:鲍氏志贺氏菌
D群:宋内氏志贺氏菌
注:+表示阳性;-表示阴性;-+表示多数阴性;+/-表示多数阳性;(+)表示迟缓阳性;d表示有不同生化型,“痫疾志贺1型和鲍氏13型为阳性,b鲍氏13型为鸟氨酸阳性。
“福氏4型和6型常见甘露醇阴性变种。5.4.2附加生化实验
由于某些不活泼的大肠埃希氏菌(anaerogenicE.coli)、A-D(Alkalescens-Disparbiotypes碱性-异型)菌的部分生化特征与志贺氏菌相似,并能与某种志贺氏菌分型血清发生凝集:因此前面生化实验符合志贺氏菌属生化特性的培养物还需另加葡萄糖胺、西蒙氏柠檬酸盐、粘液酸盐试验(36℃培养24h~48h)。志贺氏菌属和不活泼大肠埃希氏菌、A-D菌的生化特性区别见表3。5
生化反应
葡萄糖铵
西蒙氏柠檬酸盐
粘液酸盐
表3志贺氏菌属和不活泼大肠埃希氏菌、A-D菌的生化特性区别A群:痢疾
志贺氏菌
B群:福氏
志贺氏菌
注1:+表示阳性;-表示阴性;d表示有不同生化型。C群:鲍氏
志贺氏菌
D群:宋内氏
志贺氏菌
GB 4789.5-2012
大肠埃希氏菌
A-D菌
注2:在葡萄糖铵、西蒙氏柠檬酸盐、粘液酸盐试验三项反应中志贺氏菌一般为阴性,而不活泼的大肠埃希氏菌、A-D(碱性-异型)菌至少有一项反应为阳性。5.4.3如选择生化鉴定试剂盒或全自动微生物生化鉴定系统,可根据5.3.2的初步判断结果,用5.3.1中已培养的营养琼脂斜面上生长的菌苔,使用生化鉴定试剂盒或全自动微生物生化鉴定系统进行鉴定。5.5血清学鉴定
5.5.1抗原的准备
志贺氏菌属没有动力,所以没有鞭毛抗原。志贺氏菌属主要有菌体(O)抗原。菌体O抗原又可分为型和群的特异性抗原。
般采用1.2%~1.5%琼脂培养物作为玻片凝集试验用的抗原。注1:一些志贺氏菌如果因为K抗原的存在而不出现凝集反应时,可挑取菌苔于1mL生理盐水做成浓菌液,100℃煮沸15min~60min去除K抗原后再检查。注2:D群志贺氏菌既可能是光滑型菌株也可能是粗糙型菌株,与其他志贺氏菌群抗原不存在交叉反应。与肠杆菌科不同,宋内氏志贺氏菌粗糙型菌株不一定会自凝。宋内氏志贺氏菌没有K抗原,5.5.2凝集反应
在玻片上划出2个约1cm×2cm的区域,挑取一环待测菌,各放1/2环于玻片上的每一区域上部,在其中一个区域下部加1滴抗血清,在另一区域下部加入1滴生理盐水,作为对照。再用无菌的接种环或针分别将两个区域内的菌落研成乳状液。将玻片倾斜摇动混合1min,并对着黑色背景进行观察,如果抗血清中出现凝结成块的颗粒,而且牛理盐水中没有发生自凝现象,那么凝集反应为阳性。如果生理盐水中出现凝集,视作为自凝。这时,应挑取同一培养基上的其他菌落继续进行试验。如果待测菌的生化特征符合志贺氏菌属生化特征,而其血清学试验为阴性的话,则按5.5.1注1进行试验。
5.5.3血清学分型(选做项目)
先用四种志贺氏菌多价血清检查,如果呈现凝集,则再用相应各群多价血清分别试验。先用B群福氏志贺氏菌多价血清进行实验,如呈现凝集,再用其群和型因子血清分别检查。如果B群多价血清不凝集,则用D群宋内氏志贺氏菌血清进行实验,如呈现凝集,则用其I相和IⅡI相血清检查:如果B、D群多价血清都不凝集,则用A群痢疾志贺氏菌多价血清及1~12各型因子血清检查,如果上述三种多价血清都不凝集,可用C群鲍氏志贺氏菌多价检查,并进一步用1~18各型因子血清检查。福氏志贺氏菌各型和亚型的型抗原和群抗原鉴别见表4。
表4福氏志贺氏菌各型和亚型的型抗原和群抗原的鉴别表型和亚型
型抗原
群抗原
(4),6
在群因子血清中的凝集
GB4789.5-2012
福氏志贺氏菌各型和亚型的型抗原和群抗原的鉴别表表4(续)
在群因子血清中的凝集
群抗原
型抗原
型和亚型
(3,4),6,7,8
(3,4),6
注:+表示凝集:-表示不凝集:()表示有或无。结果报告
综合以上生化试验和血清学鉴定的结果,报告25g(mL)样品中检出或未检出志贺氏菌。7
附录A
培养基和试剂
A.1志贺氏菌增菌肉汤-新生霉素(Shige/labroth)A.1.1志贺氏菌增菌肉汤
A.1.1.1成分
胰蛋白陈
葡萄糖
磷酸氢二钾
磷酸二氢钾
氯化钠
吐温80(Tween80)
蒸馏水
A.1.1.2制法
GB 4789.5-2012
将以上成分混合加热溶解,冷却至25℃左右校正pH至7.00.2,分装适当的容器,121℃灭菌15min。取出后冷却至50℃~55℃,加入除菌过滤的新生霉素溶液(0.5ug/mL),分装225mL备用。注:如不立即使用,在2℃~8℃条件下可储存一个月。A.1.2新生霉素溶液
A.1.2.1成分
新生霉素
蒸馏水
A.1.2.2制法
将新生霉素溶解于蒸馏水中,用0.22um过滤膜除菌,如不立即使用,在2℃~8℃条件下可储存一个月。
A.1.3临用时每225mL志贺氏菌增菌肉汤(A.1.1)加入5mL新生霉素溶液(A.1.2),混匀。A.2麦康凯(MAC)琼脂
A.2.1成分
蛋白陈
3号胆盐
氯化钠
中性红
结晶紫
蒸馏水
A.2.2制法
将以上成分混合加热溶解,冷却至25℃左右校正pH至7.2±0.2,分装,121℃高压灭菌15min。冷却至45℃~50℃,倾注平板。
注:如不立即使用,在2℃~8℃条件下可储存二周。A.3木糖赖氨酸脱氧胆盐(XLD)琼脂A.3.1成分
A.3.2制法
酵母膏
L-赖氨酸
脱氧胆酸钠
氯化钠
硫代硫酸钠
柠檬酸铁铵
蒸馏水
GB4789.5-2012
除酚红和琼脂外,将其他成分加入400mL蒸馏水中,煮沸溶解,校正pH至7.40.2。另将琼脂加入600mL蒸馏水中,煮沸溶解。
将上述两溶液混合均匀后,再加入指示剂,待冷至50℃~55℃倾注平血。注:本培养基不需要高压灭菌,在制备过程中不宜过分加热,避免降低其选择性,贮于室温暗处。本培养基宜于当天制备,第二天使用。使用前必须去除平板表面上的水珠,在37℃~55C温度下,琼脂面向下、平板盖亦向下烘干。另外如配制好的培养基不立即使用,在2℃~8℃条件下可储存二周。A.4三糖铁(TSI)琼脂
A.4.1成分
蛋白陈
牛肉浸膏
葡萄糖
硫酸亚铁铵(NH4)Fe(SO4)26H,O
氯化钠
硫代硫酸钠
蒸馏水
A.4.2制法
除酚红和琼脂外,将其他成分加于400mL蒸馏水中,搅拌均匀,静置约10min,加热使完全溶化,冷却至25℃左右校正pH至7.4士0.2。另将琼脂加于600mL蒸馏水中,静置约10min,加热使完全溶化。将两溶液混合均匀,加入5%酚红水溶液5mL,混匀,分装小号试管,每管约3mL。于121℃灭菌15min,制成高层斜面。冷却后呈桔红色。如不立即使用,在2℃~8℃条件下可储存一个月。A.5营养琼脂斜面
A.5.1成分
蛋白陈
牛肉膏
氯化钠
A.5.2制法
蒸馏水
GB 4789.5-2012
将除琼脂以外的各成分溶解于蒸馏水内,加入15%氢氧化钠溶液约2mL,冷却至25℃左右校正pH至7.0+0.2。加入琼脂,加热煮沸,使琼脂溶化。分装小号试管,每管约3mL。于121℃灭菌15min制成斜面。
注:如不立即使用,在2℃~8℃条件下可储存二周。A.6半固体琼脂
A.6.1成分
蛋白陈
牛肉膏
氯化钠wwW.bzxz.Net
蒸馏水
A.6.2制法
0.3g~0.7g
按以上成分配好,加热溶解,并校正pH至7.4±0.2,分装小试管,121℃灭菌15min,直立凝固备用。
A.7葡萄糖铵培养基
A.7.1成分
氯化钠
硫酸镁(MgSO4·7H2O)
磷酸二氢铵
磷酸氢二钾
葡萄糖
0.2%溴麝香草酚蓝水溶液
蒸馏水
A.7.2制法
先将盐类和糖溶解于水内,校正pH至6.8±0.2,再加琼脂加热溶解,然后加入指示剂。混合均匀后分装试管,121℃高压灭菌15min。制成斜面备用。A.7.3试验方法
用接种针轻轻触及培养物的表面,在盐水管内做成极稀的悬液,肉眼观察不到混浊,以每一接种环内含菌数在20~100之间为宜。将接种环灭菌后挑取菌液接种,同时再以同法接种普通斜面一支作为对照。于36℃土1℃培养24h。阳性者葡萄糖铵斜面上有正常大小的菌落生长:阴性者不生长,但在对照培养基上生长良好。如在葡萄糖铵斜面生长极微小的菌落可视为阴性结果注:容器使用前应用清洁液浸泡。再用清水、蒸馏水冲洗于净,并用新棉花做成棉塞,干热灭菌后使用。如果操作时不注意,有杂质污染时,易造成假阳性的结果。A.8尿素琼脂
A.8.1成分
蛋白陈
氯化钠
葡萄糖
磷酸二氢钾
0.4%酚红溶液
A.8.2制法
20%尿素溶液
蒸馏水
GB4789.5-2012
除酚红和尿素外的其他成分加热溶解,冷却至25℃左右校正pH至7.2±0.2,加入酚红指示剂,混匀,于121℃灭菌15min。冷至约55℃,加入用0.22um过滤膜除菌后的20%尿素水溶液100mL,混匀,以无菌操作分装灭菌试管,每管约3mL~4mL,制成斜面后放冰箱备用。A.8.3试验方法
挑取琼脂培养物接种,在36℃±1℃培养24h,观察结果。尿素酶阳性者由于产碱而使培养基变为红色。
A.9β-半乳糖苷酶培养基
A.9.1液体法(ONPG法)
A.9.1.1成分
邻硝基苯β-D-半乳糖苷(ONPG)0.01mol/L磷酸钠缓冲液(pH7.5±0.2)1%蛋白陈水(pH7.5±0.2)
A.9.1.2制法
将ONPG溶于缓冲液内,加入蛋白陈水,以过滤法除菌,分装于10mm×75mm试管内,每管0.5mL,用橡皮塞塞紧。
A.9.1.3试验方法
自琼脂斜面挑取培养物一满环接种,于36℃±1℃培养1h~3h和24h观察结果。如果β-D-半乳糖苷酶产生,则于1h~3h变黄色,如无此酶则24h不变色。A.9.2平板法(X-Gal法)
A.9.2.1成分
蛋白陈
氯化钠
5-溴-4-氯-3-吲哚-β-D-半乳糖苷(X-Gal)琼脂
蒸馏水
A.9.2.2制法
将各成分(A.9.2.1)加热煮沸于1L水中,冷却至25℃左右校正pH至7.2±0.2,115℃高压灭菌10min。倾注平板避光冷藏备用。
A.9.2.3试验方法
挑取琼脂斜面培养物接种于平板,划线和点种均可,于36℃±1℃培养18h~24h观察结果。如果β-D-半乳糖苷酶产生,则平板上培养物颜色变蓝色,如无此酶则培养物为无色或不透明色,培养48h~72h后有部分转为淡粉红色。
A.10氨基酸脱羧酶试验培养基
A.10.1成分
蛋白陈
酵母浸膏
葡萄糖
1.6%溴甲酚紫-乙醇溶液
L型或DL型赖氨酸和鸟氨酸
0.5g/100mL或1.0g/100mL
小提示:此标准内容仅展示完整标准里的部分截取内容,若需要完整标准请到上方自行免费下载完整标准文档。
GB4789.52012
食品安全国家标准
食品微生物学检验志贺氏菌检验2012-05-17发布
中华人民共和国卫生部
2012-07-17实施
本标准代替GB/T4789.5-2003《食品卫生微生物学检验本标准与GB/T4789.5-2003相比,主要变化如下:修改了标准名称;
-修改了培养基和试剂;
志贺氏菌检验》。
-修改了操作步骤中增菌部分和生化试验及附加生化试验部分;修改了表2;
-修改了表4。
GB4789.5-2012
1范围
食品安全国家标准
食品微生物学检验志贺氏菌检验本标准规定了食品中志贺氏菌(Shigella)的检验方法本标准适用于食品中志贺氏菌的检验。设备和材料
除微生物实验室常规灭菌及培养设备外,其他设备和材料如下:恒温培养箱:36℃土1℃;
b)冰箱:2℃~5℃;
膜过滤系统;
d)厌氧培养装置:41.5℃±1℃;电子天平:感量0.1g:
显微镜:10×~100×;
均质器;
振荡器:
GB4789.5-2012
无菌吸管:1mL(具0.01mL刻度)、10mL(具0.1mL刻度)或微量移液器及吸头无菌均质杯或无菌均质袋:容量500mL:j)
无菌培养Ⅲ:直径90mm;
pH计或pH比色管或精密pH试纸:m)
全自动微生物生化鉴定系统。
3培养基和试剂
3.1志贺氏菌增菌肉汤-新生霉素:见附录A中A.1。3.2麦康凯(MAC)琼脂:见附录A中A.2、3.3木糖赖氨酸脱氧胆酸盐(XLD)琼脂:见附录A中A.33.4志贺氏菌显色培养基。
3.5三糖铁(TSI)琼脂:见附录A中A.4。3.6营养琼脂斜面:见附录A中A.5。3.7半固体琼脂:见附录A中A.6。3.8葡萄糖铵培养基:见附录A中A.7。3.9尿素琼脂:见附录A中A.8。
3.10β-半乳糖苷酶培养基:见附录A中A.9。3.11氨基酸脱羧酶试验培养基:见附录A中A.10。3.12糖发酵管:见附录A中A.11。3.13西蒙氏柠檬酸盐培养基:见附录A中A.12。3.14粘液酸盐培养基:见附录A中A.133.15蛋白陈水、靛基质试剂:见附录A中A.14。3.16志贺氏菌属诊断血清。
3.17生化鉴定试剂盒。
4检验程序
志贺氏菌检验程序见图1。
GB4789.5-2012
5操作步骤
5.1增菌
25g(或25mL)样品+志贺氏菌增菌肉汤225mL41.5℃±1℃
16h~20h厌氧培养
血清学分型
MAC或志贺氏菌显色培养基
36℃±1℃,20h~48h
挑取可疑菌落
TSI,半固体,
营养琼脂斜面
生化鉴定
志贺氏菌属分群及分型结果
图1志贺氏菌检验程序
GB4789.5-2012
以无菌操作取检样25g(mL),加入装有灭菌225mL志贺氏菌增菌肉汤的均质杯,用旋转刀片式均质器以8000r/min~10000r/min均质:或加入装有225mL志贺氏菌增菌肉汤的均质袋中,用拍击式均质器连续均质1min~2min,液体样品振荡混匀即可。于41.5℃±1℃,厌氧培养16h~20h。5.2分离
取增菌后的志贺氏增菌液分别划线接种于XLD琼脂平板和MAC琼脂平板或志贺氏菌显色培养基平板上,于36℃土1℃培养20h~24h,观察各个平板上生长的菌落形态。宋内氏志贺氏菌的单个菌落直径大于其他志贺氏菌。若出现的菌落不典型或菌落较小不易观察,则继续培养至48h再进行观察。志贺氏菌在不同选择性琼脂平板上的菌落特征见表1。4
选择性琼脂平板
MAC琼脂
XLD琼脂
志贺氏菌显色培养基
5.3初步生化试验
志贺氏菌在不同选择性琼脂平板上的菌落特征表1
志贺氏菌的菌落特征
无色至浅粉红色,半透明、光滑、湿润、圆形、边缘整齐或不齐粉红色至无色,半透明、光滑、湿润、圆形、边缘整齐或不齐按照显色培养基的说明进行判定GB 4789.5-2012
5.3.1自选择性琼脂平板上分别挑取2个以上典型或可疑菌落,分别接种TSI、半固体和营养琼脂斜面各管,置36℃土1℃培养20h~24h,分别观察结果。5.3.2凡是三糖铁琼脂中斜面产碱、底层产酸(发酵葡萄糖,不发酵乳糖,蔗糖)、不产气(福氏志贺氏菌6型可产生少量气体)、不产硫化氢、半固体管中无动力的菌株,挑取其5.3.1中已培养的营养琼脂斜面上生长的菌苔,进行生化试验和血清学分型5.4生化试验及附加生化试验
5.4.1生化试验
用5.3.1中已培养的营养琼脂斜面上生长的菌苔,进行生化试验,即β-半乳糖苷酶、尿素、赖氨酸脱羧酶、鸟氨酸脱羧酶以及水杨苷和七叶苷的分解试验。除宋内氏志贺氏菌、鲍氏志贺氏菌13型的鸟氨酸阳性;宋内氏菌和痢疾志贺氏菌1型,鲍氏志贺氏菌13型的β-半乳糖苷酶为阳性以外,其余生化试验志贺氏菌属的培养物均为阴性结果。另外由于福氏志贺氏菌6型的生化特性和疾志贺氏菌或鲍氏志贺氏菌相似,必要时还需加做靛基质、甘露醇、棉子糖、甘油试验,也可做革兰氏染色检查和氧化酶试验,应为氧化酶阴性的革兰氏阴性杆菌。生化反应不符合的菌株,即使能与某种志贺氏菌分型血清发生凝集,仍不得判定为志贺氏菌属。志贺氏菌属生化特性见表2。表2志贺氏菌属四个群的生化特征生化反应
B-半乳糖苷酶
赖氨酸脱羧酶
鸟氨酸脱羧酶
水杨苷
七叶苷
靛基质
甘露醇
棉子糖
A群:疾志贺氏菌
B群:福氏志贺氏菌
C群:鲍氏志贺氏菌
D群:宋内氏志贺氏菌
注:+表示阳性;-表示阴性;-+表示多数阴性;+/-表示多数阳性;(+)表示迟缓阳性;d表示有不同生化型,“痫疾志贺1型和鲍氏13型为阳性,b鲍氏13型为鸟氨酸阳性。
“福氏4型和6型常见甘露醇阴性变种。5.4.2附加生化实验
由于某些不活泼的大肠埃希氏菌(anaerogenicE.coli)、A-D(Alkalescens-Disparbiotypes碱性-异型)菌的部分生化特征与志贺氏菌相似,并能与某种志贺氏菌分型血清发生凝集:因此前面生化实验符合志贺氏菌属生化特性的培养物还需另加葡萄糖胺、西蒙氏柠檬酸盐、粘液酸盐试验(36℃培养24h~48h)。志贺氏菌属和不活泼大肠埃希氏菌、A-D菌的生化特性区别见表3。5
生化反应
葡萄糖铵
西蒙氏柠檬酸盐
粘液酸盐
表3志贺氏菌属和不活泼大肠埃希氏菌、A-D菌的生化特性区别A群:痢疾
志贺氏菌
B群:福氏
志贺氏菌
注1:+表示阳性;-表示阴性;d表示有不同生化型。C群:鲍氏
志贺氏菌
D群:宋内氏
志贺氏菌
GB 4789.5-2012
大肠埃希氏菌
A-D菌
注2:在葡萄糖铵、西蒙氏柠檬酸盐、粘液酸盐试验三项反应中志贺氏菌一般为阴性,而不活泼的大肠埃希氏菌、A-D(碱性-异型)菌至少有一项反应为阳性。5.4.3如选择生化鉴定试剂盒或全自动微生物生化鉴定系统,可根据5.3.2的初步判断结果,用5.3.1中已培养的营养琼脂斜面上生长的菌苔,使用生化鉴定试剂盒或全自动微生物生化鉴定系统进行鉴定。5.5血清学鉴定
5.5.1抗原的准备
志贺氏菌属没有动力,所以没有鞭毛抗原。志贺氏菌属主要有菌体(O)抗原。菌体O抗原又可分为型和群的特异性抗原。
般采用1.2%~1.5%琼脂培养物作为玻片凝集试验用的抗原。注1:一些志贺氏菌如果因为K抗原的存在而不出现凝集反应时,可挑取菌苔于1mL生理盐水做成浓菌液,100℃煮沸15min~60min去除K抗原后再检查。注2:D群志贺氏菌既可能是光滑型菌株也可能是粗糙型菌株,与其他志贺氏菌群抗原不存在交叉反应。与肠杆菌科不同,宋内氏志贺氏菌粗糙型菌株不一定会自凝。宋内氏志贺氏菌没有K抗原,5.5.2凝集反应
在玻片上划出2个约1cm×2cm的区域,挑取一环待测菌,各放1/2环于玻片上的每一区域上部,在其中一个区域下部加1滴抗血清,在另一区域下部加入1滴生理盐水,作为对照。再用无菌的接种环或针分别将两个区域内的菌落研成乳状液。将玻片倾斜摇动混合1min,并对着黑色背景进行观察,如果抗血清中出现凝结成块的颗粒,而且牛理盐水中没有发生自凝现象,那么凝集反应为阳性。如果生理盐水中出现凝集,视作为自凝。这时,应挑取同一培养基上的其他菌落继续进行试验。如果待测菌的生化特征符合志贺氏菌属生化特征,而其血清学试验为阴性的话,则按5.5.1注1进行试验。
5.5.3血清学分型(选做项目)
先用四种志贺氏菌多价血清检查,如果呈现凝集,则再用相应各群多价血清分别试验。先用B群福氏志贺氏菌多价血清进行实验,如呈现凝集,再用其群和型因子血清分别检查。如果B群多价血清不凝集,则用D群宋内氏志贺氏菌血清进行实验,如呈现凝集,则用其I相和IⅡI相血清检查:如果B、D群多价血清都不凝集,则用A群痢疾志贺氏菌多价血清及1~12各型因子血清检查,如果上述三种多价血清都不凝集,可用C群鲍氏志贺氏菌多价检查,并进一步用1~18各型因子血清检查。福氏志贺氏菌各型和亚型的型抗原和群抗原鉴别见表4。
表4福氏志贺氏菌各型和亚型的型抗原和群抗原的鉴别表型和亚型
型抗原
群抗原
(4),6
在群因子血清中的凝集
GB4789.5-2012
福氏志贺氏菌各型和亚型的型抗原和群抗原的鉴别表表4(续)
在群因子血清中的凝集
群抗原
型抗原
型和亚型
(3,4),6,7,8
(3,4),6
注:+表示凝集:-表示不凝集:()表示有或无。结果报告
综合以上生化试验和血清学鉴定的结果,报告25g(mL)样品中检出或未检出志贺氏菌。7
附录A
培养基和试剂
A.1志贺氏菌增菌肉汤-新生霉素(Shige/labroth)A.1.1志贺氏菌增菌肉汤
A.1.1.1成分
胰蛋白陈
葡萄糖
磷酸氢二钾
磷酸二氢钾
氯化钠
吐温80(Tween80)
蒸馏水
A.1.1.2制法
GB 4789.5-2012
将以上成分混合加热溶解,冷却至25℃左右校正pH至7.00.2,分装适当的容器,121℃灭菌15min。取出后冷却至50℃~55℃,加入除菌过滤的新生霉素溶液(0.5ug/mL),分装225mL备用。注:如不立即使用,在2℃~8℃条件下可储存一个月。A.1.2新生霉素溶液
A.1.2.1成分
新生霉素
蒸馏水
A.1.2.2制法
将新生霉素溶解于蒸馏水中,用0.22um过滤膜除菌,如不立即使用,在2℃~8℃条件下可储存一个月。
A.1.3临用时每225mL志贺氏菌增菌肉汤(A.1.1)加入5mL新生霉素溶液(A.1.2),混匀。A.2麦康凯(MAC)琼脂
A.2.1成分
蛋白陈
3号胆盐
氯化钠
中性红
结晶紫
蒸馏水
A.2.2制法
将以上成分混合加热溶解,冷却至25℃左右校正pH至7.2±0.2,分装,121℃高压灭菌15min。冷却至45℃~50℃,倾注平板。
注:如不立即使用,在2℃~8℃条件下可储存二周。A.3木糖赖氨酸脱氧胆盐(XLD)琼脂A.3.1成分
A.3.2制法
酵母膏
L-赖氨酸
脱氧胆酸钠
氯化钠
硫代硫酸钠
柠檬酸铁铵
蒸馏水
GB4789.5-2012
除酚红和琼脂外,将其他成分加入400mL蒸馏水中,煮沸溶解,校正pH至7.40.2。另将琼脂加入600mL蒸馏水中,煮沸溶解。
将上述两溶液混合均匀后,再加入指示剂,待冷至50℃~55℃倾注平血。注:本培养基不需要高压灭菌,在制备过程中不宜过分加热,避免降低其选择性,贮于室温暗处。本培养基宜于当天制备,第二天使用。使用前必须去除平板表面上的水珠,在37℃~55C温度下,琼脂面向下、平板盖亦向下烘干。另外如配制好的培养基不立即使用,在2℃~8℃条件下可储存二周。A.4三糖铁(TSI)琼脂
A.4.1成分
蛋白陈
牛肉浸膏
葡萄糖
硫酸亚铁铵(NH4)Fe(SO4)26H,O
氯化钠
硫代硫酸钠
蒸馏水
A.4.2制法
除酚红和琼脂外,将其他成分加于400mL蒸馏水中,搅拌均匀,静置约10min,加热使完全溶化,冷却至25℃左右校正pH至7.4士0.2。另将琼脂加于600mL蒸馏水中,静置约10min,加热使完全溶化。将两溶液混合均匀,加入5%酚红水溶液5mL,混匀,分装小号试管,每管约3mL。于121℃灭菌15min,制成高层斜面。冷却后呈桔红色。如不立即使用,在2℃~8℃条件下可储存一个月。A.5营养琼脂斜面
A.5.1成分
蛋白陈
牛肉膏
氯化钠
A.5.2制法
蒸馏水
GB 4789.5-2012
将除琼脂以外的各成分溶解于蒸馏水内,加入15%氢氧化钠溶液约2mL,冷却至25℃左右校正pH至7.0+0.2。加入琼脂,加热煮沸,使琼脂溶化。分装小号试管,每管约3mL。于121℃灭菌15min制成斜面。
注:如不立即使用,在2℃~8℃条件下可储存二周。A.6半固体琼脂
A.6.1成分
蛋白陈
牛肉膏
氯化钠wwW.bzxz.Net
蒸馏水
A.6.2制法
0.3g~0.7g
按以上成分配好,加热溶解,并校正pH至7.4±0.2,分装小试管,121℃灭菌15min,直立凝固备用。
A.7葡萄糖铵培养基
A.7.1成分
氯化钠
硫酸镁(MgSO4·7H2O)
磷酸二氢铵
磷酸氢二钾
葡萄糖
0.2%溴麝香草酚蓝水溶液
蒸馏水
A.7.2制法
先将盐类和糖溶解于水内,校正pH至6.8±0.2,再加琼脂加热溶解,然后加入指示剂。混合均匀后分装试管,121℃高压灭菌15min。制成斜面备用。A.7.3试验方法
用接种针轻轻触及培养物的表面,在盐水管内做成极稀的悬液,肉眼观察不到混浊,以每一接种环内含菌数在20~100之间为宜。将接种环灭菌后挑取菌液接种,同时再以同法接种普通斜面一支作为对照。于36℃土1℃培养24h。阳性者葡萄糖铵斜面上有正常大小的菌落生长:阴性者不生长,但在对照培养基上生长良好。如在葡萄糖铵斜面生长极微小的菌落可视为阴性结果注:容器使用前应用清洁液浸泡。再用清水、蒸馏水冲洗于净,并用新棉花做成棉塞,干热灭菌后使用。如果操作时不注意,有杂质污染时,易造成假阳性的结果。A.8尿素琼脂
A.8.1成分
蛋白陈
氯化钠
葡萄糖
磷酸二氢钾
0.4%酚红溶液
A.8.2制法
20%尿素溶液
蒸馏水
GB4789.5-2012
除酚红和尿素外的其他成分加热溶解,冷却至25℃左右校正pH至7.2±0.2,加入酚红指示剂,混匀,于121℃灭菌15min。冷至约55℃,加入用0.22um过滤膜除菌后的20%尿素水溶液100mL,混匀,以无菌操作分装灭菌试管,每管约3mL~4mL,制成斜面后放冰箱备用。A.8.3试验方法
挑取琼脂培养物接种,在36℃±1℃培养24h,观察结果。尿素酶阳性者由于产碱而使培养基变为红色。
A.9β-半乳糖苷酶培养基
A.9.1液体法(ONPG法)
A.9.1.1成分
邻硝基苯β-D-半乳糖苷(ONPG)0.01mol/L磷酸钠缓冲液(pH7.5±0.2)1%蛋白陈水(pH7.5±0.2)
A.9.1.2制法
将ONPG溶于缓冲液内,加入蛋白陈水,以过滤法除菌,分装于10mm×75mm试管内,每管0.5mL,用橡皮塞塞紧。
A.9.1.3试验方法
自琼脂斜面挑取培养物一满环接种,于36℃±1℃培养1h~3h和24h观察结果。如果β-D-半乳糖苷酶产生,则于1h~3h变黄色,如无此酶则24h不变色。A.9.2平板法(X-Gal法)
A.9.2.1成分
蛋白陈
氯化钠
5-溴-4-氯-3-吲哚-β-D-半乳糖苷(X-Gal)琼脂
蒸馏水
A.9.2.2制法
将各成分(A.9.2.1)加热煮沸于1L水中,冷却至25℃左右校正pH至7.2±0.2,115℃高压灭菌10min。倾注平板避光冷藏备用。
A.9.2.3试验方法
挑取琼脂斜面培养物接种于平板,划线和点种均可,于36℃±1℃培养18h~24h观察结果。如果β-D-半乳糖苷酶产生,则平板上培养物颜色变蓝色,如无此酶则培养物为无色或不透明色,培养48h~72h后有部分转为淡粉红色。
A.10氨基酸脱羧酶试验培养基
A.10.1成分
蛋白陈
酵母浸膏
葡萄糖
1.6%溴甲酚紫-乙醇溶液
L型或DL型赖氨酸和鸟氨酸
0.5g/100mL或1.0g/100mL
小提示:此标准内容仅展示完整标准里的部分截取内容,若需要完整标准请到上方自行免费下载完整标准文档。
标准图片预览:




- 其它标准
- 热门标准
- 国家标准
- GB/T2828.1-2012 计数抽样检验程序 第1部分:按接收质量限(AQL)检索的逐批检验抽样计划
- GB/T2855.8-1990 冲模滑动导向模座 后侧导柱窄形下模座
- GB/T2481.2-1998 固结磨具用磨料 粒度组成的检测和标记 第2部分:微粉F230?F1200
- GB/T12611-2008 金属零(部)件镀覆前质量控制技术要求
- GB/T40094.2-2021 电子商务数据交易第2部分:数据描述规范
- GB/T33588.3-2020 雷电防护系统部件(LPSC)第3部分:隔离放电间隙(ISG)的要求
- GB/T39275-2020 电力电子系统和设备有源馈电变流器(AIC)应用的运行条件和特性
- GB/T29077-2024 星箭界面飞行环境遥测数据处理要求
- GB/T18487.1-2023 电动汽车传导充电系统 第1部分:通用要求
- GB24500-2020 工业锅炉能效限定值及能效等级
- GB4706.7-1999 家用和类似用途电器的安全真空吸尘器和吸水式清洁器的特殊要求
- GB/T3047.3-2003 高度进制为20mm的插箱、插件基本尺寸系列
- GB9075-1988 架空索道用钢丝绳检验和报废规范
- GB15735-2004 金属热处理生产过程安全卫生要求
- GB17378.5-1998 海洋监测规范 第5部分:沉积物分析
- 行业新闻
请牢记:“bzxz.net”即是“标准下载”四个汉字汉语拼音首字母与国际顶级域名“.net”的组合。 ©2025 标准下载网 www.bzxz.net 本站邮件:bzxznet@163.com
网站备案号:湘ICP备2025141790号-2
网站备案号:湘ICP备2025141790号-2