- 您的位置:
- 标准下载网 >>
- 标准分类 >>
- 国家标准(GB) >>
- GB/T 18638-2002 流行性乙型脑炎诊断技术
标准号:
GB/T 18638-2002
标准名称:
流行性乙型脑炎诊断技术
标准类别:
国家标准(GB)
标准状态:
现行-
发布日期:
2002-02-19 -
实施日期:
2002-05-01 出版语种:
简体中文下载格式:
.rar.pdf下载大小:
420.19 KB
点击下载
标准简介:
标准下载解压密码:www.bzxz.net
本标准规定了流行性乙型脑炎的病毒分离与鉴定、间接免疫荧光试验、补体结合试验、血凝抑制试验等技术要求。本标准适用于口岸、产地及集散地、饲养单位(或个人)的猪、马、骡、驴、牛、羊等的流行性乙型脑炎的诊断和检疫。 GB/T 18638-2002 流行性乙型脑炎诊断技术 GB/T18638-2002
部分标准内容:
GB/T186382002
流行性乙型脑炎又称目本乙型脑炎(JapanescBcncephalitis),是由流行性乙型脑炎病毒引起的一种蚊媒性人兽共患传染病。成年动物和人常皇隐性感染,幼龄动物特别是马感染后,可发生脑炎症状,妊娠母猪可引起流产、死胎及木乃伊胎公猪睾丸肿大,儿童可发生严重的脑炎。多发生于7~9月份。我国许多省(市)都有本病发生,特别是六七十年代,发病率最高。对人畜的健康可造成严重的威胁。世界动物卫生组织和国本的资料,都采用病毒分离鉴定、免疫荧光试验、血凝抑制试验、补体结合试验、血清中和试验等进行诊断。我国对本病的研究报道较多,而比较常用的诊断方法仍是本标准规定的病毒分离鉴定、匪凝抑制试验、补体结合试验。病毒分离鉴定适用于流行性乙型脑炎新疫区的确定和病畜的确诊。间接免疫荧光试验适用于可疑流行性乙型脑炎病毒标本的快速检测和病毒分离株的初步鉴定。补体结合试验,由于补体结合抗体一般在病后2~3周出现,5~6周达高峰,并可维持1年以上,故可适用流行性乙型脑炎的较早期诊断和流行病学调查,是最常用的方法。根据当时的实际需要,可任选一种或两种检疫方法,以达到准确诊断的鼠的。本标准的实施,对提高乙型脑炎的诊断和疫情预测水平,及时采取防制措施,保证人畜健康,将起到重要的作用。
本标准的附录A、附录B都是标准的附录。本标准由中华人民共和国农业部提出。本标准由全国动物检疫标准化技术委员会归口。本标准起草单位:中国人民解放军农牧大学本标准主要起草人:李佑民、宣华、李金中、刘振润。134
1范围
中华人民共和国国家标准
流行性乙型脑炎诊断技术
Diagnostic techniques for epidemic encephalitis BGB/T 18638--2002
本标准规定广流行性乙型脑炎的病毒分离与鉴定、间接免疫荧光试验、补体结合试验、血凝抑制试验等技术要求。
本标准适用于口岸、产地及集散地、饲养单位(或个人)的猪、马、骤、驴、牛、羊等的流行性乙型脑炎的诊断和检疫
2病毒的分离与鉴定
2.1材料准备
2.1.1器材:细胞培养瓶(或管),吸管.中试管,三角烧瓶,37C水浴箱,37C恒温箱,普通冰箱及低温冰箱,离心机及离心管,研磨器械,普通光学显微镜,G5级玻璃滤器,孔径0.45μm的微孔滤膜,0.25ml注射器及针头。
2.1.2试剂:汉克氏(Hanks)液,0.5%水解乳蛋白Hanks液,2万IU/ml.青霉素液,2万μg/mL链霉素液,7%碳酸氢钠液,1%胰蛋白酶液,1%酚红.(中性)液,伊格尔氏(Eagle)最低必要成分培养液(EMEM),小牛血清。
2.1.3小动物:小鼠(6g~8g)乳鼠。2.1.4鸡胚细胞、绿猴肾传代细胞(Vero)、仓鼠肾传代细胞(BHK21)、白蚊伊蚊C6/36传代细胞等。2.2病毒分离
2.2.1样品的采取和运送
2.2.1.1在流行的早期和发病的早期(即病毒血症阶段),无菌采取病畜的血液或脑脊髓液。2.2.1.2应在病畜死亡后3h内(越早越好)采取脑组织(选大脑皮质、脑干、中脑、海马回及桥脑)数小块放于灭菌玻璃瓶。
2.2.1.3猪应采取流产死胎的脑组织,置冰箱内立即送检。2.2.1.4不能立即检查者,应放-~25C~一30C冰箱,或加50%甘油生理盐水,4C保存送检,2.2.2样品的处理
2.2.2. 1血液应分离出血清或血浆。2.2.2.2脑脊髓液可直接应用。
2.2.2.3脑组织应研磨成糊状,加人0.5%水解乳蛋白Hanks液(或碱性肉汤或10%脱脂奶生理盐水),制成10%悬液,3000r/min离心30min,吸取上清液,加人青霉素500IU/mL和链霉素500ug/ml,在4C处理3h~4h(无污染者可不加青、链霉素处理),即得接种样品。2.2.2.4怀疑有污染的样品,也可用0.45um微孔滤膜过滤法处理。2.2.3动物分离法
2.2.3.1取6g~8g小鼠10只(或3~5日龄乳鼠--窝),用左手固定,在耳与眼之间用碘酒消毒。右手持吸取接种样品的0.25ml.注射器在消毒部刺人硬脑膜下,每只6g~8g小鼠注射0.03ml(乳鼠中华人民共和国国家质量监督检验检疫总局2002-02-19批准2002-05-01实施
GB/T18638-2002
0.01ml,~0.02ml.)。然后用左手拇指及食指抓住小鼠头顶部皮肤,翻转左手,使小鼠腹部朝上,将其尾部在左于掌与小手指之间,消毒腹部,右于持注射器向腹腔内注人样品0.2mL~0.5mlL。2.2.3.2对照小鼠2只,按同法同剂量注射稀释液。2.2.3.3接种后2d~4d,如对照鼠正常,而注射样品的小鼠表现松毛、弓背、沉郁、震颤、绕圈、后肢麻痹、继而死亡者,应解剖取鼠脑组织,按2.2.2.3制成接种样品,按2.2.3.1再接种小鼠。连续2代接种小鼠均有发病致死者,而且未检出致病细菌时,-方面继续传代并作鉴定,另.·方面用冰冻干燥法保存毒种。
2.2.3.4接种小鼠经7d~14d无一发病时,则取出2只,解剖取脑组织,按2.2.2.3制成样品盲传-代,观察2周如仍无死亡,即按未分离出病毒报告。2.2.4组织培养法
2.2.4.1取2.2.2制成的样品,接种鸡胚细胞、仓鼠肾单层细胞或VerO、BHK21、C6/36传代细胞单层,每份样品至少接种10管(或瓶),每管0.1mL~0.2mL,37C吸附1h,用Hanks液洗1次,加人EMEM液1ml,放37C培养7d~10d。
2.2.4.2同时设细胞对照2管(或瓶),不接种样品,其他步骤与接种样品管相同。2.2.4.3接种后观察约10d,第二天开始,每天在显微镜下观察细胞病变,若细胞对照管正常,而接种样品管细胞出现细胞萎缩、脱落、形成空斑等病变时,立即移种新的细胞单层,如出现相类似的病变,且日渐明显,即可收获,放25C~30C冰箱保存待检。2.2.4.4如盲传3代均无细胞病变,即按未分离出病毒报告。2.2.5鸡胚培养法
2.2.5.1取2.2.2制成的样品,接种于6d~8d龄鸡胚卵黄囊内,每胚接种0.5ml.,每份样品至少接种4胚。
2.2.5.2同时设对照鸡胚2个,对照鸡胚接种稀释液0.5ml.。2.2.5.3置37C培养4d,48h后对照鸡胚正常,而接种样品鸡胚死亡或到期未死亡者,解剖取出鸡胚磨碎,用碱性肉汤制成10%悬液,3000r/min离心30min,取上清液按2.2.3接种小鼠。2.2.5.4如小鼠发现2.2.3.3中死亡时,解剖取脑组织,冰冻保存待检。2.2.5.5如鸡胚培养3代均正常,即按未分离出病毒报告。2.2.6病毒的鉴定
经小鼠、鸡胚或组织培养法分离获得能稳定传代的病原,在细菌培养基上不生长,经除菌过滤(G5级玻璃滤器或0.45um微孔滤膜)仍保留其繁殖力和致病力,即可以认为已分离到病毒。2.2.6.1初步鉴定:将待检病毒制备抗原,用血凝抑制试验(第4章)、补体结合试验(第5章)作初步鉴定,确定病毒的属性。三种方法任选一种。2.2.6.2最后鉴定:小鼠中和试验方法如下:a)首先将被检血清56C30min灭活;b)与10倍连续稀释的乙型脑炎病毒等量混合,在37(感作1h;c)给3周龄小鼠脑内接种,每只接种0.03mL,每一稀释度病毒脑内接种相同小鼠5只,观察2周;d)根据各稀释度小鼠的死亡数和存活数按半数致死量(Reed-Muench)法计算LDsa;e)操作中要设①病毒对照组(已知参考病毒加阴性血清),②阳性血清对照组(已知参考病毒加阳性清);
f)试验组为③(被检病毒加阳性血清);g)结果判定:
组①LD-组②LDsn一阳性血清中和已知参考病毒的中和指数;组①LDso-组?LDsn=阳性血清中和被检病毒的中和指数。两者中和指数相接近(相差≤0.51.ID5),即可确定分离的病毒为流行性乙型脑炎病毒。如对中和指136
GB/T 18638-2002
数结果有怀疑,川用新分离的病毒制备免疫血清,再与参考株和新分离的病毒株进行交叉中和试验。如果对应的抗原抗体反应效价高于交叉反应的效价,则表明两者有区别。3补体结合试验
3.1材料准备
3.1.1器材
试管(7.5cm×1.0cm),吸管(10ml.、2ml、lml.),试管架,水浴箱(37C~38℃),离心机及离心管。
3.1.2试剂
3.1.2.1乙型脑炎抗原将病毒正常对照抗原,均由制标单位提供。3.1.2.2溶血素:由制标单位提供。效价应1:5000以上。3.1.2.3补体:由制标单位提供冻干补体,或用3只以上豚鼠血清混合的新鲜补体。3.1.2.4绵羊红细胞:由健康绵羊采血,加人三倍的阿氏液(见附录A中A3)内,4C保存可用1个月。用前取绵羊红细胞悬液适量,加5~10倍量的生理盐水(见附录A中A4),充分混勾后,以2500r/min离心15min,吸弃上清液后,再加生理盐水悬浮红细胞,如此洗涤3次。最后以2500r/min离心20min,吸弃上清液,沉涎的红细胞以钙镁盐水(4.1.2.7)配成1%绵羊红细胞悬液。3.1.2.5阳性对照血清由制标单位供应。3.1.2.6阴性对照血清由制标单位供应。3.1.2.7钙镁盐水:见附录A中A1。3.1.3样品
3.1.3.1被检血清应于发病早期和病后4周各采血1次,分离血清,密装灭菌小瓶,4C冰箱保存或立即检查。
3.1.3.2采血分离血清过程应无菌操作,防止污染。血清须新鲜透明不溶血。3.1.3.3试验前应将阴性血清、阳性血清、被检血清作2倍稀释,随后依动物种类进行不同温度的加热灭活30min。豚鼠56℃,马58℃~60℃,人、猴及小鼠60℃,牛、水牛、山羊、狗、猪、仓鼠62℃,骤、驴63C~64C,家兔65C。
3.2操作方法
3.2.1预备试验
见附录B(标准的附录)。
3.2.2正式试验
3.2.2.1操作程序:
n)取3排小试管,每排6支。
b)于第1排的第2~6管内各加钙镁盐水(见附录A中A1)0.3ml。(:)2倍稀释的被检血清0.1mL于各排第1管。d)于第1排第2管2倍稀释的被检血清加0.3ml.。e)混勾第1排第2管内容物,吸取0.5mL,分别加于第2、第3排的第2管,各加0.1mI.,加于第1排第3管余下的0.3mL。
)混勾第3臂内容物,如上连续稀释并移人第2、第3排的相应管,直到第6管。g)结果每排形成1:2到1:64稀释度的被检血清,每管含稀释的被检血清0.1mL。然后按表1加人乙脑病毒抗原,或正常对照抗原、钙镁盐水各0.1ml,再加2单位的补体0.2ml振摇混匀后置4(冰箱过夜,取出后置37C水浴30min。h)备管再加致敏绵羊红细胞悬液0.2ml,37C感作30min后判定。137
0. 1 被检血清
或阴、阳性血
清)的稀释倍数
1:32
1:32
1:64
1:32
工作价抗原
(乙脑抗原)
抗原)
(钙镁盐水对
GB/T 18638-2002
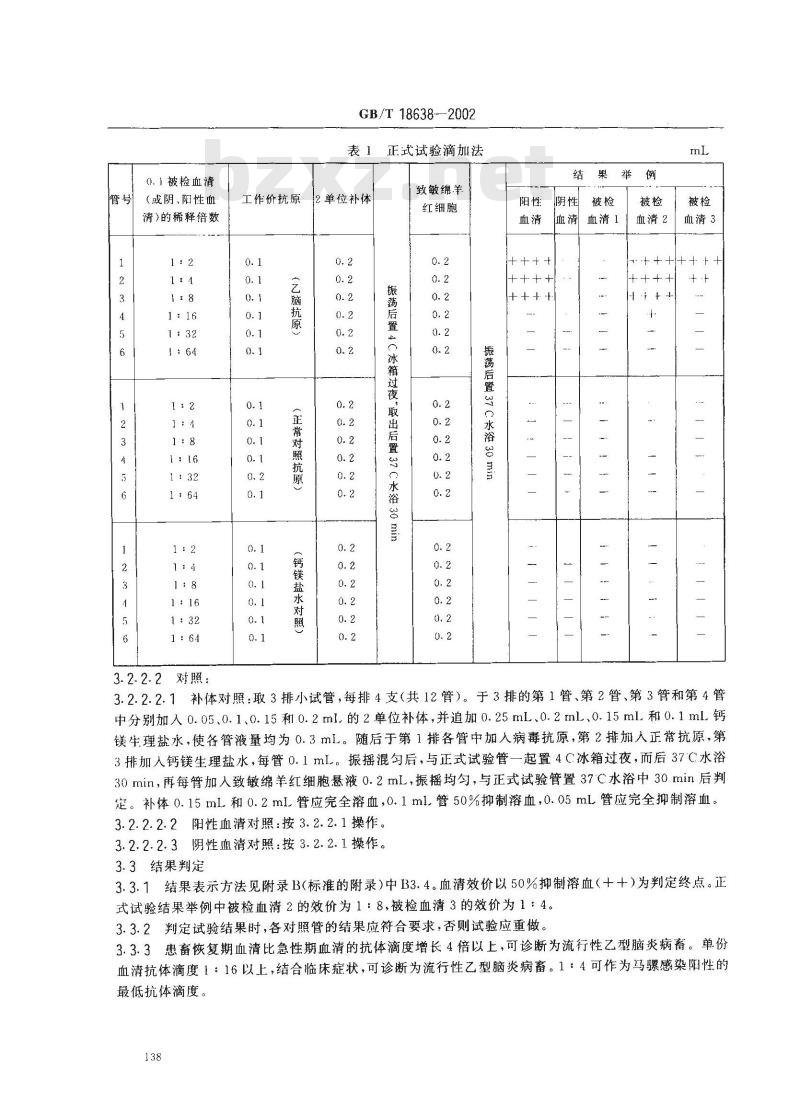
表1正式试验滴加法
致敏绵羊
2单位补体
荡后置
箱过夜”
红细胞
振荡后暨
结 果
血清血清1
血清 2
血清3
3.2.2.2对照:
3.2.2.2.1补体对照:取3排小试管,每排4支(共12管)。于3排的第1管、第2管、第3管和第4管中分别加人0.05、0.1、0.15和0.2ml.的2单位补体,并追加0.25mL、0.2ml、0.15ml.和0.1ml钙镁生理盐水,使各管液量均为0.3mL。随后于第1排各管中加人病毒抗原,第2排加入正常抗原,第3排加人钙镁生理盐水,每管0.1mI。振摇混勾后,与正式试验管一起置4C冰箱过夜,而后37C水浴30min,再每管加人致敏绵羊红细胞悬液0.2mL,振摇均匀,与正式试验管置37C水浴中30min后判定。补体0.15ml和0.2ml.管应完全溶血,0.1ml.管50%抑制溶血,0.05mL管应完全抑制溶血。3.2.2.2.2阳性血清对照:按3.2.2.1操作。3.2.2.2.3阴性血清对照:按3.2.2.1操作。3.3结果判定
3.3.1结果表示方法见附录B(标准的附录)中B3.4。血清效价以50%抑制溶血(++)为判定终点。正式试验结果举例中被检血清2的效价为1:8,被检血清3的效价为1:4。3.3.2判定试验结果时,各对照管的结果应符合要求,否则试验应重做。3.3.3患畜恢复期血清比急性期血清的抗体滴度增长4倍以上,可诊断为流行性乙型脑炎病畜。单份血清抗体滴度1:16以上,结合临床症状,可诊断为流行性乙型脑炎病畜。1:4可作为马骤感染阳性的最低抗体滴度。
4血凝抑制试验
4.1材料准备bzxZ.net
4.1.1器材
GB/T18638-2002
96孔V型微量血凝板,25μl移液管及吸头;微量振荡器;自动稀释器或稀释棒;离心机及离心管。4.1.2试剂
生理盐水;0.4%牛血清白蛋白pH9.0硼酸缓冲液(BABS);25%白陶土悬液;阿氏液(血球保存液);不间pH磷酸盐缓冲液[见附录A(标准的附录)]。4.1.3鹅红细胞
取无菌的5ml~10ml.注射器及针头付,从健康鹅的翅静脉无菌采血2ml.~3ml.,随即注入盛有15ml.左右阿氏液的三角烧瓶内,不时摇动3min后,置于4C冰箱过夜。次日将红细胞倒人刻度离心管,平衡后,2000r/min离心5min,弃上清液,加人10倍量生理盐水充分混勾,2000r/min离心5min,如此反复3次。第3次用同样速度离心10min,然后吸尽上清液。再用1mlL吸管插人离心管内的红细胞泥的中心部,吸取所需的红细胞,通过对不同pH值的磷酸盐缓冲液(见附录A中A6)试验,选取最适pH的磷酸盐缓冲液配成0.33%和8%的鹅红细胞悬液备用。4.1.4凝素
由制标单位提供,其效价的测定见附录C(标准的附录)。4.1.5样品的采集及处理
应于发病早期和病后3~4周各采血1次,分离血清,立即检查或4C冰箱保存待检。试验前,被检血清作如下处理,以除去非特异性血凝抑制物质和非特异性凝集素。取被检血清0.1ml.加pH7.4磷酸盐缓冲液(见附录A中A6)0.4mL,而后加热灭能,灭能温度同补体结合试验的被检血清的处理(3.1.3.3),灭能后加25%白陶土悬液(见附录A中A5)0.5ml,用力振荡摇勾,置37(1h或室温过夜后,1000r/min离心5min。取上清液再加8%鹅红细胞悬液0.05ml,混匀后,置3730min,1000r/min离心5min,上清液即为1:10稀释的被检血清。同时检查血清中的免疫球蛋自M(IgM)时,应另取被检血清0.1mI.,加pH7.4磷酸盐缓冲液0.4ml.,70(加热30min,而后按上述方法处理。性血清和阴性血清亦需同样处理。4.2操作方法
4.2.18单位血凝素的配制:如测定的血凝素效价为1280倍,则用预冷的0.4%pH9.0的硼酸缓冲液(见附录A中A2)将血凝素原液作160倍稀释。4.2.2在微量血凝板的第1排(横)各孔的上边分别标记被检血清号、阴性血清号、阳性血清号。第1行(纵)各孔的外侧边标记血清的稀释度。最后一排作红细胞对照。4.2.3第2排到第7排各孔加人0.4%pH9.0的硼酸缓冲液25μl。第8排加50μl.。4.2.4第1、2排按已标记的血清号每孔分别加相应的血清25ul。4.2.5自动稀释器,先经生理盐水预温,并排净液体,插人第2排各孔,充分混合后.蘸取25μL到第3排,依次倍比稀释至第7排,最后从第7排各孔中蘸取25μL弃去,第8排作红细胞对照。4.2.6除第8排外,各孔分别加人8个单位的血凝素25μl,在微量振荡器上振荡3min,置室温(20C~25 C)30 min。
4.2.7各孔分别加人0.33%鹅红细胞悬液25μL,摇勾后置37C恒温箱30min,取出判定结果。4.3结果判定
判时先看对照。当被检血清对照、阴性血清对照和红细胞对照均完全不凝集,血凝素对照除1单位孔呈“十十”或“+”凝集,而8单位孔、4单位孔、2单位孔均完全凝集时即可由前向后逐孔检查被检血清的抑制效价,以能完全抑制红细胞凝集的被检血清的最高稀释倍数作为该血清的血凝抑制抗体效价,139
GB/T 18638—2002
表2(举例)血清的血凝抑制抗体效价为1:160。患畜恢复期血清的血凝抑制抗体效价比急性期的血清高4倍以上,或单份血清作免疫球蛋白M(IgM)处理后,处理后血清的抗体效价比处理前的降低2个滴度以上时,均可诊断为流行性乙型脑炎病畜。马骤流行性乙型脑炎感染的血凝抑制抗体最低滴度暂定为1:40。
血清稀释度
0.4%pH9.0硼酸缓冲液
10倍稀释血清
8单位血凝素
0.33%鹅红
细胞(pH6.42
判定结果
微量血凝抑制试验(举例)
振荡3min后,置室温30min
摇匀后置37(温箱30min
*弃25
红细胞对照
A1钙镁溶液(用于补体结合试验)氯化镁(MgClz·6Hz0)
氯化钙(CaCl2·2H,O)
GB/T 18638--2002
附录A
(标准的附录)
试剂的配制
加蒸馏水至100ml。105kPa20min高压灭菌。A20.4%牛血清白蛋白pH9.0硼酸缓冲液(BABS)(用于血凝抑制试验)母液:0.05mol/L硼砂溶液
硼砂(Na2B,O, 12H,0)
双蒸馏水或无离子水加至
母液1:0.2mol/L.硼酸溶液
硼酸(H,BO)
加双蒸馏水或无离子水至
100 ml
使用液:母液I32mL十母液I8mL+生理盐水460mL。配好后测定pH,如不到9.0,可加适量0.05mol/L硼砂溶液。105kPa 20min高压灭菌。临用前,在使用液中添加0.4%牛恤清白蛋白。A3阿氏液(用于血凝抑制试验和补体结合试验)葡葡糖
柠檬酸钠
氯化钠(NaCI)
加双蒸馏水或无离子水至100mL,56kPa20min高压灭菌。A4生理盐水(用于补体结合试验和血凝抑制试验)氯化钠(NaCI)
加双蒸馏水或无离子水至1000mL,105kPa20min高压灭菌。A525%白陶土感液(用于血凝抑制试验)取优质白陶土粉末25g,加pH7.4磷酸盐缓冲液至100mL,105kPa20min高压灭菌。4C保存,可用1个月。临用前摇勾。
A6不同pH值磷酸盐缓冲液(PBS)
母液【:1/15mol/L磷酸氢二钠溶液配制无水磷酸氢二钠
加双蒸馏水或无离子水至1000ml.9.47g
母液I:1/15mol/I.磷酸二氢钾溶液配制磷酸二氢钾
加双蒸馏水或无离子水至1000mLpH5.8PBS:母液I8.0mL+母液92mL+生理盐水566mL;141
GB/T 18638- -- 2002
pH6.0PB3S:母液112.2mL+母液187.8mL+生理盐水566ml;pH6.2PBS:母液118.6ml.+母液181.4mL+生理盐水566mL;pH6.4PBS:母液126.7ml.+孕液73.3nL+生理盐水566ml.;pH6.6PBS:母液137.5ml+母液I62.5ml+生理盐水566ml-;pH7.4PI3S:液180.8ml+母液I19.2ml+生理盐水566mlL.。校正pH值后,105kPa20min高压灭菌。附录B
(标准的附录)
补体结合试验的预备试验
B1溶血素效价滴定
B1.1溶血素的稀释:吸取溶血素(.1mI(含50%甘油者用0.2mL),加钙镁盐水9.9mlL(含50%甘油者加9.8mL).混匀后即为1:100的溶血素,然后取1:100溶血素1mL加钙镁盐水4ml,即为1:500的溶血素.再按表31进行稀释。表B1
溶血素的稀释
试管号
钙镁盐水
溶血素
稀释倍数
1:1000
1:2000
1:3000
1:4000
1:5000
1:6000
1:7000
1:8000
1:9000
1:10000
B1.2溶血素的滴定:取一支1mI.吸管,由高稀释度开始,将各管已稀释的溶血素吸到另…一排小试管内,每管0.1ml,然后按表32依次加人补体、钙镁盐水及1%绵羊红细胞,播勾后,置37C水浴中30 min,观察结果。
溶血素
试管号
稀释度
1:1000
11:2000
11:3000
1:4000
1:5 000
146000
1:7000
1:8000
1:9000
110 0001
补体(1:50)
溶血素的滴定
钙镁盐水
1%绵羊红细胞悬液
摇勾后
置37℃
水浴中
30 min
人部分溶解
GB/T 18638---2002
B1.3溶血素单位计算:能使红细胞完全溶解的溶血素的最高稀释度.称为1个溶血素单位。表2中判定结果为第6管,即0.1ml.1:6000的溶血素含有1个单位。试验中应用2个单位的溶血素,邸将溶血素稀释成1:3000,则0.1ml。中含有2个单位溶血素。32补体效价滴定
B2.1滴定方法:吸取补体0.1ml,加钙镁盐水4.9ml.,即1:50稀释补体,然后按表B3的量,分别加人三排小试管中,再依次加人钙镁盐水、4个单位溶血素或15稀释抗原,混匀后,放37C水浴中30min,再加人致敏绵羊红细胞(1%绵羊红细胞悬液与等量2个单位溶血素相混合,放37C水浴中15min),摇匀后,放37C水浴中30min,观察结果。B2.2补体单位的计算:能使红细胞完全溶解的最小补体量为一个单位,正式试验和抗原滴定时都用2个单位的补体。如表B3所示,0.12ml的1:50补体为一个单位,2个单位补体应为0.24mL的1:50补体,由于正式试验和抗原滴定时每管应加的补体量为0.2mL,故需按式(B1)换算其稀释度:X a
(50 × 0. 2)
将未稀释补体稀释成1141,可使0.2mL内含2个单位的补体。具体方法是在1mL补体内加40ml钙镁盐水,即为1:41稀释。补体效价的滴定
稀释抗原
病毒抗原
正常脑组织对照抗原
盐水对照
钙镁盐水
水浴中
30mnin
致敏红细胞
水浴中
结果举例
微不溶
微不溶
微不溶
B3病毒抗原效价的滴定
GB/T 18638—2002
抗原滴定一般按方阵法进行,即用倍比稀释的已知阳性血清与倍比稀释的抗原进行试验。按表B4进行抗原和血清稀释,表中举例说明效价滴定结果。B3.1滴定方法
按表4纵横排列试管,分别加人稀释的抗原和免疫血清各0.1ml。每管加入稀释补体0.2mL(含2个单位)。
表B4抗原效价滴定(举例)
免疫血清
病毒抗原
1:64
正常抗原(1:4)抗
补体对照免疫血清
抗补体对照
B3.2对照管设置
正常血清(1:4)
抗补体对照
病毒抗原
抗补体对照
B3.2.1免疫血清抗补体对照:将免疫血清稀释为1:2、1:4、1:8,每管0.1ml.,每个稀释度再加入钙镁盐水0.1ml、稀释补体0.2mL,但不加抗原。B3.2.2病毒抗原抗补体对照:将病毒抗原稀释为1:2、1:4、1:8,每管各加0.1mL,再加钙镁盐水0.1ml,稀释补体0.2ml。
B3.2.3正常血清抗补体对照:在7管1:4正常血清0.1mL中,分别加入不同稀释度的病声抗原0.1ml.,稀释补体0.2ml.。
B3.2.4正常抗原抗补体对照:在7管1:4正常抗原0.1mL中,分别加入不同稀释度的免疫血清0. 1 ml.,稀释补体0.2ml.。
B3.2.5溶血素对照:加钙镁盐水0.4mL于1支小试管中。B3.3感作
将各管摇匀,置4C冰箱内过夜,次日取出,放于37C水浴中30min,每管加人致敏绵羊红细胞悬液0.2ml,置37C水浴内30min,判定结果。B3.4结果判定
完全抑制溶血者为“++++”,75%抑制溶血者为“+++”,50%抑制溶血者为“++”,25%抑制溶血者为“十”,完全不抑制溶血者为“一”。与最高稀释度免疫血清发生100%或75%抑制溶血的抗原,其抗原的最高稀释倍数就是抗原的效价。表B4举例为1:32。正式试验时须用较高浓度(约4~~8倍)的抗原,一般用抗原原液的1:4或1:8稀释液。141
小提示:此标准内容仅展示完整标准里的部分截取内容,若需要完整标准请到上方自行免费下载完整标准文档。
流行性乙型脑炎又称目本乙型脑炎(JapanescBcncephalitis),是由流行性乙型脑炎病毒引起的一种蚊媒性人兽共患传染病。成年动物和人常皇隐性感染,幼龄动物特别是马感染后,可发生脑炎症状,妊娠母猪可引起流产、死胎及木乃伊胎公猪睾丸肿大,儿童可发生严重的脑炎。多发生于7~9月份。我国许多省(市)都有本病发生,特别是六七十年代,发病率最高。对人畜的健康可造成严重的威胁。世界动物卫生组织和国本的资料,都采用病毒分离鉴定、免疫荧光试验、血凝抑制试验、补体结合试验、血清中和试验等进行诊断。我国对本病的研究报道较多,而比较常用的诊断方法仍是本标准规定的病毒分离鉴定、匪凝抑制试验、补体结合试验。病毒分离鉴定适用于流行性乙型脑炎新疫区的确定和病畜的确诊。间接免疫荧光试验适用于可疑流行性乙型脑炎病毒标本的快速检测和病毒分离株的初步鉴定。补体结合试验,由于补体结合抗体一般在病后2~3周出现,5~6周达高峰,并可维持1年以上,故可适用流行性乙型脑炎的较早期诊断和流行病学调查,是最常用的方法。根据当时的实际需要,可任选一种或两种检疫方法,以达到准确诊断的鼠的。本标准的实施,对提高乙型脑炎的诊断和疫情预测水平,及时采取防制措施,保证人畜健康,将起到重要的作用。
本标准的附录A、附录B都是标准的附录。本标准由中华人民共和国农业部提出。本标准由全国动物检疫标准化技术委员会归口。本标准起草单位:中国人民解放军农牧大学本标准主要起草人:李佑民、宣华、李金中、刘振润。134
1范围
中华人民共和国国家标准
流行性乙型脑炎诊断技术
Diagnostic techniques for epidemic encephalitis BGB/T 18638--2002
本标准规定广流行性乙型脑炎的病毒分离与鉴定、间接免疫荧光试验、补体结合试验、血凝抑制试验等技术要求。
本标准适用于口岸、产地及集散地、饲养单位(或个人)的猪、马、骤、驴、牛、羊等的流行性乙型脑炎的诊断和检疫
2病毒的分离与鉴定
2.1材料准备
2.1.1器材:细胞培养瓶(或管),吸管.中试管,三角烧瓶,37C水浴箱,37C恒温箱,普通冰箱及低温冰箱,离心机及离心管,研磨器械,普通光学显微镜,G5级玻璃滤器,孔径0.45μm的微孔滤膜,0.25ml注射器及针头。
2.1.2试剂:汉克氏(Hanks)液,0.5%水解乳蛋白Hanks液,2万IU/ml.青霉素液,2万μg/mL链霉素液,7%碳酸氢钠液,1%胰蛋白酶液,1%酚红.(中性)液,伊格尔氏(Eagle)最低必要成分培养液(EMEM),小牛血清。
2.1.3小动物:小鼠(6g~8g)乳鼠。2.1.4鸡胚细胞、绿猴肾传代细胞(Vero)、仓鼠肾传代细胞(BHK21)、白蚊伊蚊C6/36传代细胞等。2.2病毒分离
2.2.1样品的采取和运送
2.2.1.1在流行的早期和发病的早期(即病毒血症阶段),无菌采取病畜的血液或脑脊髓液。2.2.1.2应在病畜死亡后3h内(越早越好)采取脑组织(选大脑皮质、脑干、中脑、海马回及桥脑)数小块放于灭菌玻璃瓶。
2.2.1.3猪应采取流产死胎的脑组织,置冰箱内立即送检。2.2.1.4不能立即检查者,应放-~25C~一30C冰箱,或加50%甘油生理盐水,4C保存送检,2.2.2样品的处理
2.2.2. 1血液应分离出血清或血浆。2.2.2.2脑脊髓液可直接应用。
2.2.2.3脑组织应研磨成糊状,加人0.5%水解乳蛋白Hanks液(或碱性肉汤或10%脱脂奶生理盐水),制成10%悬液,3000r/min离心30min,吸取上清液,加人青霉素500IU/mL和链霉素500ug/ml,在4C处理3h~4h(无污染者可不加青、链霉素处理),即得接种样品。2.2.2.4怀疑有污染的样品,也可用0.45um微孔滤膜过滤法处理。2.2.3动物分离法
2.2.3.1取6g~8g小鼠10只(或3~5日龄乳鼠--窝),用左手固定,在耳与眼之间用碘酒消毒。右手持吸取接种样品的0.25ml.注射器在消毒部刺人硬脑膜下,每只6g~8g小鼠注射0.03ml(乳鼠中华人民共和国国家质量监督检验检疫总局2002-02-19批准2002-05-01实施
GB/T18638-2002
0.01ml,~0.02ml.)。然后用左手拇指及食指抓住小鼠头顶部皮肤,翻转左手,使小鼠腹部朝上,将其尾部在左于掌与小手指之间,消毒腹部,右于持注射器向腹腔内注人样品0.2mL~0.5mlL。2.2.3.2对照小鼠2只,按同法同剂量注射稀释液。2.2.3.3接种后2d~4d,如对照鼠正常,而注射样品的小鼠表现松毛、弓背、沉郁、震颤、绕圈、后肢麻痹、继而死亡者,应解剖取鼠脑组织,按2.2.2.3制成接种样品,按2.2.3.1再接种小鼠。连续2代接种小鼠均有发病致死者,而且未检出致病细菌时,-方面继续传代并作鉴定,另.·方面用冰冻干燥法保存毒种。
2.2.3.4接种小鼠经7d~14d无一发病时,则取出2只,解剖取脑组织,按2.2.2.3制成样品盲传-代,观察2周如仍无死亡,即按未分离出病毒报告。2.2.4组织培养法
2.2.4.1取2.2.2制成的样品,接种鸡胚细胞、仓鼠肾单层细胞或VerO、BHK21、C6/36传代细胞单层,每份样品至少接种10管(或瓶),每管0.1mL~0.2mL,37C吸附1h,用Hanks液洗1次,加人EMEM液1ml,放37C培养7d~10d。
2.2.4.2同时设细胞对照2管(或瓶),不接种样品,其他步骤与接种样品管相同。2.2.4.3接种后观察约10d,第二天开始,每天在显微镜下观察细胞病变,若细胞对照管正常,而接种样品管细胞出现细胞萎缩、脱落、形成空斑等病变时,立即移种新的细胞单层,如出现相类似的病变,且日渐明显,即可收获,放25C~30C冰箱保存待检。2.2.4.4如盲传3代均无细胞病变,即按未分离出病毒报告。2.2.5鸡胚培养法
2.2.5.1取2.2.2制成的样品,接种于6d~8d龄鸡胚卵黄囊内,每胚接种0.5ml.,每份样品至少接种4胚。
2.2.5.2同时设对照鸡胚2个,对照鸡胚接种稀释液0.5ml.。2.2.5.3置37C培养4d,48h后对照鸡胚正常,而接种样品鸡胚死亡或到期未死亡者,解剖取出鸡胚磨碎,用碱性肉汤制成10%悬液,3000r/min离心30min,取上清液按2.2.3接种小鼠。2.2.5.4如小鼠发现2.2.3.3中死亡时,解剖取脑组织,冰冻保存待检。2.2.5.5如鸡胚培养3代均正常,即按未分离出病毒报告。2.2.6病毒的鉴定
经小鼠、鸡胚或组织培养法分离获得能稳定传代的病原,在细菌培养基上不生长,经除菌过滤(G5级玻璃滤器或0.45um微孔滤膜)仍保留其繁殖力和致病力,即可以认为已分离到病毒。2.2.6.1初步鉴定:将待检病毒制备抗原,用血凝抑制试验(第4章)、补体结合试验(第5章)作初步鉴定,确定病毒的属性。三种方法任选一种。2.2.6.2最后鉴定:小鼠中和试验方法如下:a)首先将被检血清56C30min灭活;b)与10倍连续稀释的乙型脑炎病毒等量混合,在37(感作1h;c)给3周龄小鼠脑内接种,每只接种0.03mL,每一稀释度病毒脑内接种相同小鼠5只,观察2周;d)根据各稀释度小鼠的死亡数和存活数按半数致死量(Reed-Muench)法计算LDsa;e)操作中要设①病毒对照组(已知参考病毒加阴性血清),②阳性血清对照组(已知参考病毒加阳性清);
f)试验组为③(被检病毒加阳性血清);g)结果判定:
组①LD-组②LDsn一阳性血清中和已知参考病毒的中和指数;组①LDso-组?LDsn=阳性血清中和被检病毒的中和指数。两者中和指数相接近(相差≤0.51.ID5),即可确定分离的病毒为流行性乙型脑炎病毒。如对中和指136
GB/T 18638-2002
数结果有怀疑,川用新分离的病毒制备免疫血清,再与参考株和新分离的病毒株进行交叉中和试验。如果对应的抗原抗体反应效价高于交叉反应的效价,则表明两者有区别。3补体结合试验
3.1材料准备
3.1.1器材
试管(7.5cm×1.0cm),吸管(10ml.、2ml、lml.),试管架,水浴箱(37C~38℃),离心机及离心管。
3.1.2试剂
3.1.2.1乙型脑炎抗原将病毒正常对照抗原,均由制标单位提供。3.1.2.2溶血素:由制标单位提供。效价应1:5000以上。3.1.2.3补体:由制标单位提供冻干补体,或用3只以上豚鼠血清混合的新鲜补体。3.1.2.4绵羊红细胞:由健康绵羊采血,加人三倍的阿氏液(见附录A中A3)内,4C保存可用1个月。用前取绵羊红细胞悬液适量,加5~10倍量的生理盐水(见附录A中A4),充分混勾后,以2500r/min离心15min,吸弃上清液后,再加生理盐水悬浮红细胞,如此洗涤3次。最后以2500r/min离心20min,吸弃上清液,沉涎的红细胞以钙镁盐水(4.1.2.7)配成1%绵羊红细胞悬液。3.1.2.5阳性对照血清由制标单位供应。3.1.2.6阴性对照血清由制标单位供应。3.1.2.7钙镁盐水:见附录A中A1。3.1.3样品
3.1.3.1被检血清应于发病早期和病后4周各采血1次,分离血清,密装灭菌小瓶,4C冰箱保存或立即检查。
3.1.3.2采血分离血清过程应无菌操作,防止污染。血清须新鲜透明不溶血。3.1.3.3试验前应将阴性血清、阳性血清、被检血清作2倍稀释,随后依动物种类进行不同温度的加热灭活30min。豚鼠56℃,马58℃~60℃,人、猴及小鼠60℃,牛、水牛、山羊、狗、猪、仓鼠62℃,骤、驴63C~64C,家兔65C。
3.2操作方法
3.2.1预备试验
见附录B(标准的附录)。
3.2.2正式试验
3.2.2.1操作程序:
n)取3排小试管,每排6支。
b)于第1排的第2~6管内各加钙镁盐水(见附录A中A1)0.3ml。(:)2倍稀释的被检血清0.1mL于各排第1管。d)于第1排第2管2倍稀释的被检血清加0.3ml.。e)混勾第1排第2管内容物,吸取0.5mL,分别加于第2、第3排的第2管,各加0.1mI.,加于第1排第3管余下的0.3mL。
)混勾第3臂内容物,如上连续稀释并移人第2、第3排的相应管,直到第6管。g)结果每排形成1:2到1:64稀释度的被检血清,每管含稀释的被检血清0.1mL。然后按表1加人乙脑病毒抗原,或正常对照抗原、钙镁盐水各0.1ml,再加2单位的补体0.2ml振摇混匀后置4(冰箱过夜,取出后置37C水浴30min。h)备管再加致敏绵羊红细胞悬液0.2ml,37C感作30min后判定。137
0. 1 被检血清
或阴、阳性血
清)的稀释倍数
1:32
1:32
1:64
1:32
工作价抗原
(乙脑抗原)
抗原)
(钙镁盐水对
GB/T 18638-2002
表1正式试验滴加法
致敏绵羊
2单位补体
荡后置
箱过夜”
红细胞
振荡后暨
结 果
血清血清1
血清 2
血清3
3.2.2.2对照:
3.2.2.2.1补体对照:取3排小试管,每排4支(共12管)。于3排的第1管、第2管、第3管和第4管中分别加人0.05、0.1、0.15和0.2ml.的2单位补体,并追加0.25mL、0.2ml、0.15ml.和0.1ml钙镁生理盐水,使各管液量均为0.3mL。随后于第1排各管中加人病毒抗原,第2排加入正常抗原,第3排加人钙镁生理盐水,每管0.1mI。振摇混勾后,与正式试验管一起置4C冰箱过夜,而后37C水浴30min,再每管加人致敏绵羊红细胞悬液0.2mL,振摇均匀,与正式试验管置37C水浴中30min后判定。补体0.15ml和0.2ml.管应完全溶血,0.1ml.管50%抑制溶血,0.05mL管应完全抑制溶血。3.2.2.2.2阳性血清对照:按3.2.2.1操作。3.2.2.2.3阴性血清对照:按3.2.2.1操作。3.3结果判定
3.3.1结果表示方法见附录B(标准的附录)中B3.4。血清效价以50%抑制溶血(++)为判定终点。正式试验结果举例中被检血清2的效价为1:8,被检血清3的效价为1:4。3.3.2判定试验结果时,各对照管的结果应符合要求,否则试验应重做。3.3.3患畜恢复期血清比急性期血清的抗体滴度增长4倍以上,可诊断为流行性乙型脑炎病畜。单份血清抗体滴度1:16以上,结合临床症状,可诊断为流行性乙型脑炎病畜。1:4可作为马骤感染阳性的最低抗体滴度。
4血凝抑制试验
4.1材料准备bzxZ.net
4.1.1器材
GB/T18638-2002
96孔V型微量血凝板,25μl移液管及吸头;微量振荡器;自动稀释器或稀释棒;离心机及离心管。4.1.2试剂
生理盐水;0.4%牛血清白蛋白pH9.0硼酸缓冲液(BABS);25%白陶土悬液;阿氏液(血球保存液);不间pH磷酸盐缓冲液[见附录A(标准的附录)]。4.1.3鹅红细胞
取无菌的5ml~10ml.注射器及针头付,从健康鹅的翅静脉无菌采血2ml.~3ml.,随即注入盛有15ml.左右阿氏液的三角烧瓶内,不时摇动3min后,置于4C冰箱过夜。次日将红细胞倒人刻度离心管,平衡后,2000r/min离心5min,弃上清液,加人10倍量生理盐水充分混勾,2000r/min离心5min,如此反复3次。第3次用同样速度离心10min,然后吸尽上清液。再用1mlL吸管插人离心管内的红细胞泥的中心部,吸取所需的红细胞,通过对不同pH值的磷酸盐缓冲液(见附录A中A6)试验,选取最适pH的磷酸盐缓冲液配成0.33%和8%的鹅红细胞悬液备用。4.1.4凝素
由制标单位提供,其效价的测定见附录C(标准的附录)。4.1.5样品的采集及处理
应于发病早期和病后3~4周各采血1次,分离血清,立即检查或4C冰箱保存待检。试验前,被检血清作如下处理,以除去非特异性血凝抑制物质和非特异性凝集素。取被检血清0.1ml.加pH7.4磷酸盐缓冲液(见附录A中A6)0.4mL,而后加热灭能,灭能温度同补体结合试验的被检血清的处理(3.1.3.3),灭能后加25%白陶土悬液(见附录A中A5)0.5ml,用力振荡摇勾,置37(1h或室温过夜后,1000r/min离心5min。取上清液再加8%鹅红细胞悬液0.05ml,混匀后,置3730min,1000r/min离心5min,上清液即为1:10稀释的被检血清。同时检查血清中的免疫球蛋自M(IgM)时,应另取被检血清0.1mI.,加pH7.4磷酸盐缓冲液0.4ml.,70(加热30min,而后按上述方法处理。性血清和阴性血清亦需同样处理。4.2操作方法
4.2.18单位血凝素的配制:如测定的血凝素效价为1280倍,则用预冷的0.4%pH9.0的硼酸缓冲液(见附录A中A2)将血凝素原液作160倍稀释。4.2.2在微量血凝板的第1排(横)各孔的上边分别标记被检血清号、阴性血清号、阳性血清号。第1行(纵)各孔的外侧边标记血清的稀释度。最后一排作红细胞对照。4.2.3第2排到第7排各孔加人0.4%pH9.0的硼酸缓冲液25μl。第8排加50μl.。4.2.4第1、2排按已标记的血清号每孔分别加相应的血清25ul。4.2.5自动稀释器,先经生理盐水预温,并排净液体,插人第2排各孔,充分混合后.蘸取25μL到第3排,依次倍比稀释至第7排,最后从第7排各孔中蘸取25μL弃去,第8排作红细胞对照。4.2.6除第8排外,各孔分别加人8个单位的血凝素25μl,在微量振荡器上振荡3min,置室温(20C~25 C)30 min。
4.2.7各孔分别加人0.33%鹅红细胞悬液25μL,摇勾后置37C恒温箱30min,取出判定结果。4.3结果判定
判时先看对照。当被检血清对照、阴性血清对照和红细胞对照均完全不凝集,血凝素对照除1单位孔呈“十十”或“+”凝集,而8单位孔、4单位孔、2单位孔均完全凝集时即可由前向后逐孔检查被检血清的抑制效价,以能完全抑制红细胞凝集的被检血清的最高稀释倍数作为该血清的血凝抑制抗体效价,139
GB/T 18638—2002
表2(举例)血清的血凝抑制抗体效价为1:160。患畜恢复期血清的血凝抑制抗体效价比急性期的血清高4倍以上,或单份血清作免疫球蛋白M(IgM)处理后,处理后血清的抗体效价比处理前的降低2个滴度以上时,均可诊断为流行性乙型脑炎病畜。马骤流行性乙型脑炎感染的血凝抑制抗体最低滴度暂定为1:40。
血清稀释度
0.4%pH9.0硼酸缓冲液
10倍稀释血清
8单位血凝素
0.33%鹅红
细胞(pH6.42
判定结果
微量血凝抑制试验(举例)
振荡3min后,置室温30min
摇匀后置37(温箱30min
*弃25
红细胞对照
A1钙镁溶液(用于补体结合试验)氯化镁(MgClz·6Hz0)
氯化钙(CaCl2·2H,O)
GB/T 18638--2002
附录A
(标准的附录)
试剂的配制
加蒸馏水至100ml。105kPa20min高压灭菌。A20.4%牛血清白蛋白pH9.0硼酸缓冲液(BABS)(用于血凝抑制试验)母液:0.05mol/L硼砂溶液
硼砂(Na2B,O, 12H,0)
双蒸馏水或无离子水加至
母液1:0.2mol/L.硼酸溶液
硼酸(H,BO)
加双蒸馏水或无离子水至
100 ml
使用液:母液I32mL十母液I8mL+生理盐水460mL。配好后测定pH,如不到9.0,可加适量0.05mol/L硼砂溶液。105kPa 20min高压灭菌。临用前,在使用液中添加0.4%牛恤清白蛋白。A3阿氏液(用于血凝抑制试验和补体结合试验)葡葡糖
柠檬酸钠
氯化钠(NaCI)
加双蒸馏水或无离子水至100mL,56kPa20min高压灭菌。A4生理盐水(用于补体结合试验和血凝抑制试验)氯化钠(NaCI)
加双蒸馏水或无离子水至1000mL,105kPa20min高压灭菌。A525%白陶土感液(用于血凝抑制试验)取优质白陶土粉末25g,加pH7.4磷酸盐缓冲液至100mL,105kPa20min高压灭菌。4C保存,可用1个月。临用前摇勾。
A6不同pH值磷酸盐缓冲液(PBS)
母液【:1/15mol/L磷酸氢二钠溶液配制无水磷酸氢二钠
加双蒸馏水或无离子水至1000ml.9.47g
母液I:1/15mol/I.磷酸二氢钾溶液配制磷酸二氢钾
加双蒸馏水或无离子水至1000mLpH5.8PBS:母液I8.0mL+母液92mL+生理盐水566mL;141
GB/T 18638- -- 2002
pH6.0PB3S:母液112.2mL+母液187.8mL+生理盐水566ml;pH6.2PBS:母液118.6ml.+母液181.4mL+生理盐水566mL;pH6.4PBS:母液126.7ml.+孕液73.3nL+生理盐水566ml.;pH6.6PBS:母液137.5ml+母液I62.5ml+生理盐水566ml-;pH7.4PI3S:液180.8ml+母液I19.2ml+生理盐水566mlL.。校正pH值后,105kPa20min高压灭菌。附录B
(标准的附录)
补体结合试验的预备试验
B1溶血素效价滴定
B1.1溶血素的稀释:吸取溶血素(.1mI(含50%甘油者用0.2mL),加钙镁盐水9.9mlL(含50%甘油者加9.8mL).混匀后即为1:100的溶血素,然后取1:100溶血素1mL加钙镁盐水4ml,即为1:500的溶血素.再按表31进行稀释。表B1
溶血素的稀释
试管号
钙镁盐水
溶血素
稀释倍数
1:1000
1:2000
1:3000
1:4000
1:5000
1:6000
1:7000
1:8000
1:9000
1:10000
B1.2溶血素的滴定:取一支1mI.吸管,由高稀释度开始,将各管已稀释的溶血素吸到另…一排小试管内,每管0.1ml,然后按表32依次加人补体、钙镁盐水及1%绵羊红细胞,播勾后,置37C水浴中30 min,观察结果。
溶血素
试管号
稀释度
1:1000
11:2000
11:3000
1:4000
1:5 000
146000
1:7000
1:8000
1:9000
110 0001
补体(1:50)
溶血素的滴定
钙镁盐水
1%绵羊红细胞悬液
摇勾后
置37℃
水浴中
30 min
人部分溶解
GB/T 18638---2002
B1.3溶血素单位计算:能使红细胞完全溶解的溶血素的最高稀释度.称为1个溶血素单位。表2中判定结果为第6管,即0.1ml.1:6000的溶血素含有1个单位。试验中应用2个单位的溶血素,邸将溶血素稀释成1:3000,则0.1ml。中含有2个单位溶血素。32补体效价滴定
B2.1滴定方法:吸取补体0.1ml,加钙镁盐水4.9ml.,即1:50稀释补体,然后按表B3的量,分别加人三排小试管中,再依次加人钙镁盐水、4个单位溶血素或15稀释抗原,混匀后,放37C水浴中30min,再加人致敏绵羊红细胞(1%绵羊红细胞悬液与等量2个单位溶血素相混合,放37C水浴中15min),摇匀后,放37C水浴中30min,观察结果。B2.2补体单位的计算:能使红细胞完全溶解的最小补体量为一个单位,正式试验和抗原滴定时都用2个单位的补体。如表B3所示,0.12ml的1:50补体为一个单位,2个单位补体应为0.24mL的1:50补体,由于正式试验和抗原滴定时每管应加的补体量为0.2mL,故需按式(B1)换算其稀释度:X a
(50 × 0. 2)
将未稀释补体稀释成1141,可使0.2mL内含2个单位的补体。具体方法是在1mL补体内加40ml钙镁盐水,即为1:41稀释。补体效价的滴定
稀释抗原
病毒抗原
正常脑组织对照抗原
盐水对照
钙镁盐水
水浴中
30mnin
致敏红细胞
水浴中
结果举例
微不溶
微不溶
微不溶
B3病毒抗原效价的滴定
GB/T 18638—2002
抗原滴定一般按方阵法进行,即用倍比稀释的已知阳性血清与倍比稀释的抗原进行试验。按表B4进行抗原和血清稀释,表中举例说明效价滴定结果。B3.1滴定方法
按表4纵横排列试管,分别加人稀释的抗原和免疫血清各0.1ml。每管加入稀释补体0.2mL(含2个单位)。
表B4抗原效价滴定(举例)
免疫血清
病毒抗原
1:64
正常抗原(1:4)抗
补体对照免疫血清
抗补体对照
B3.2对照管设置
正常血清(1:4)
抗补体对照
病毒抗原
抗补体对照
B3.2.1免疫血清抗补体对照:将免疫血清稀释为1:2、1:4、1:8,每管0.1ml.,每个稀释度再加入钙镁盐水0.1ml、稀释补体0.2mL,但不加抗原。B3.2.2病毒抗原抗补体对照:将病毒抗原稀释为1:2、1:4、1:8,每管各加0.1mL,再加钙镁盐水0.1ml,稀释补体0.2ml。
B3.2.3正常血清抗补体对照:在7管1:4正常血清0.1mL中,分别加入不同稀释度的病声抗原0.1ml.,稀释补体0.2ml.。
B3.2.4正常抗原抗补体对照:在7管1:4正常抗原0.1mL中,分别加入不同稀释度的免疫血清0. 1 ml.,稀释补体0.2ml.。
B3.2.5溶血素对照:加钙镁盐水0.4mL于1支小试管中。B3.3感作
将各管摇匀,置4C冰箱内过夜,次日取出,放于37C水浴中30min,每管加人致敏绵羊红细胞悬液0.2ml,置37C水浴内30min,判定结果。B3.4结果判定
完全抑制溶血者为“++++”,75%抑制溶血者为“+++”,50%抑制溶血者为“++”,25%抑制溶血者为“十”,完全不抑制溶血者为“一”。与最高稀释度免疫血清发生100%或75%抑制溶血的抗原,其抗原的最高稀释倍数就是抗原的效价。表B4举例为1:32。正式试验时须用较高浓度(约4~~8倍)的抗原,一般用抗原原液的1:4或1:8稀释液。141
小提示:此标准内容仅展示完整标准里的部分截取内容,若需要完整标准请到上方自行免费下载完整标准文档。
标准图片预览:




- 其它标准
- 热门标准
- 国家标准(GB)
- GB/T42970-2023 半导体集成电路 视频编解码电路测试方法
- GB/T42854-2023 民用飞机客户培训飞行模拟机通用技术规范
- GB/T43802-2024 绿色产品评价 物流周转箱
- GB29140-2024 纯碱单位产品能源消耗限额
- GB/T38920-2020 危险废物储运单元编码要求
- GB/T7967-1987 声学 水声发射器的大功率特性和测量
- GB1913.2-1990 漂白浸渍绝缘纸
- GB28129-2011 乙羧氟草醚原药
- GB/T10599-1998 多绳摩擦式提升机
- GB31604.49-2023 食品安全国家标准 食品接触材料及制品 多元素的测定和多元素迁移量的测定
- GB/T18721.4-2024 印刷技术 印前数据交换 第4部分:显示用宽色域标准彩色图像数据 [Adobe RGB (1998)/SCID]
- GB/T39249-2020 橡胶和塑料软管及非增强软管织物增强型 低温压扁试验
- GB15193.5-2003 骨髓细胞微核试验
- GB/T15412-1994 应用电视摄像机云台通用技术条件
- GB/T97.1-2002 平垫圈A级
- 行业新闻
请牢记:“bzxz.net”即是“标准下载”四个汉字汉语拼音首字母与国际顶级域名“.net”的组合。 ©2025 标准下载网 www.bzxz.net 本站邮件:bzxznet@163.com
网站备案号:湘ICP备2025141790号-2
网站备案号:湘ICP备2025141790号-2