- 您的位置:
- 标准下载网 >>
- 标准分类 >>
- 国家标准(GB) >>
- GB/T 4789.10-2008 食品卫生微生物学检验 金黄色葡萄球菌检验
标准号:
GB/T 4789.10-2008
标准名称:
食品卫生微生物学检验 金黄色葡萄球菌检验
标准类别:
国家标准(GB)
标准状态:
现行-
发布日期:
1984-12-25 -
实施日期:
2009-03-01 出版语种:
简体中文下载格式:
.rar.pdf下载大小:
782.21 KB
替代情况:
替代GB/T 4789.10-2003采标情况:
AOAC 987.09,NEQ ISO 6888-1-1999,NEQ
点击下载
标准简介:
标准下载解压密码:www.bzxz.net
本标准规定了食品中金黄色葡萄球菌的检验方法。本标准适用于各类食品和食物中毒样品中金黄色葡萄球菌的检验。 GB/T 4789.10-2008 食品卫生微生物学检验 金黄色葡萄球菌检验 GB/T4789.10-2008
部分标准内容:
ICS 07. 100. 30
中华人民共和国国家标准
GB/T 4789.10—2008
代替GB/T4789.102003
食品卫生微生物学检验
金黄色葡萄球菌检验
Microbiological examination of food hygiene-Detection of Sta phyiococcus aureus2008-11-21发布
中华人民共和国卫生部
中国国家标准化管理委员会
2009-03-01实施
中华人民共和国
国家标准
食品卫生微生物学检验
金黄色葡萄球菌检验
GB/T4789.10—2008
中国标准出版社出版发行
北京复兴门外三里河北街16号
邮政编码:100015
网址 spc. nct. cn
电话:6852394668517548
中国标准出版杜案皇岛印刷厂印剧各地新华书店经销
开本880×1230
印张1
字数 21 千字
2009年3月第一版
2009年3月第一次印刷
号:155066·136102
如有印装差错
定价16.00元
由本社发行中心调换
版权专有权必究
举报电话:(010)68533533
http://foodmate.net言
GB/T 4789.10--2008
本标准对应于国际分析家学会(AOACINTFRNATIONAT)AOAC987.09食品中金黄色葡葡球菌分离和计数 MPN法\(1991 年)(AOAC Official Method 987.09,Staphytococcus aureus in faodsmostprobablenumbermcthodforisolationandcnumcration)和国际标雅化组织ISQ68881:1999《食品和动物何料中而浆凝固酶阳性葡萄球菌、金黄色葡药球菌和其他葡萄球菌计数方法》(Microbiologyof food and animal fccding stuffs Horizontal method for the cnumcration of coagulase-pusitive staph-ytococci, Staphytococcus aureaus end other species-Pur1 l: Technique using Baird-Parker agar mcdium)。本标准与A0ACOfficialMethod987.09、ISO6B88-1:1999的一致性程度为非等效。本标代替GB/T4789.102003食品卫生微生物学检验金黄色葡萄球菌检验》。本标准与GB/T 4789.10—2003比主要修改如下:规范了样品制备过程;
对原标准中血浆凝固酶部分逃行了修改。本标的附录 A,附录 B为规范性附录。本标摊由中华人民共和国卫生部提出并归口。本标准由中华人民共和国卫生部负贵解释。本标准负责起草单位:中国疾病预防控制中心营养与食品安全所。本标准参与起草单位:上海市疾病预防控制中心、中华人民共和国辽宁出人境检验检疫局、中华人民共和国内篆古出人境检验捡疫局,江苏省疾病预防控制中心。本标准主要起草人:刘秀梅、陈敏、刘弘、刘中学、卢行安、袁宝君、田静。本标准所代替标准的历次版本发布情况为:G 1789. 10—1984,GB/T 4789.10—1994,GB/T 4789.102003.1范围
食品卫生微生物学检验
金黄色葡萄球菌检验
本标推规定了食品中金黄色葡葡球菌的检验方法。本标准适用于各类食品和食物中毒样品中金黄色葡萄球菌的检验。2设备和材料
除微生物实验室常规灭菌及培养设备外,其他设备和材料如下:2.1恒温培养箱:36 ℃+1℃,
2.2冰箱:2~5℃。
2.3恒温水浴箱:37℃士1℃。
2.4天半:感量0.1g。
2.5均质器:
2.6振滋器,
GB/T 4789.10—2008
2.7无菌吸管:1mL具0.01mL刻度).10mL(具0.【mL刻度)或微量移液器及吸头。2.8无菌锥形瓶:容量100 mL、500 mL。2.9尤菌培养Ⅲl:直径90mm。
2.10注射器:0.5mL
2. 11 pH 计或 pH 比色管或精密 pH 试纸,3培养基和试剂
3.110%氯化钠胰酪陈人豆肉汤:见第A.1章。3, 2 7. 5%氯化钠肉汤;见第 A, 2 章。3.3血琼脂平板:见第A,3章,
3,4 Baird-Parkcr琼脂平板:见第 A.4章。3.5脑心浸出液(BHI)肉汤:见第A.5章。3. 6 免血浆;见第 A. 6 章。
磷酸盐缓冲液:见第A.7章。
3.8营养琼脂斜面:见第A.8章。3, 9革兰氏染色液:见第 A. 9 章。3.10无菌生理盐水:称取8.5g氯化钠溶于1000mL蒸馅水中,121℃高压灭菌15nin。3.111mol/L氢氧化钠(NaOH):称取10g氢氧化钢(NaOH)溶于1000mL蒸馏水中。3.121mol/1盐酸(HCl):37%浓盐酸90mL.加蒸馏水到1000mL。4 检验程序
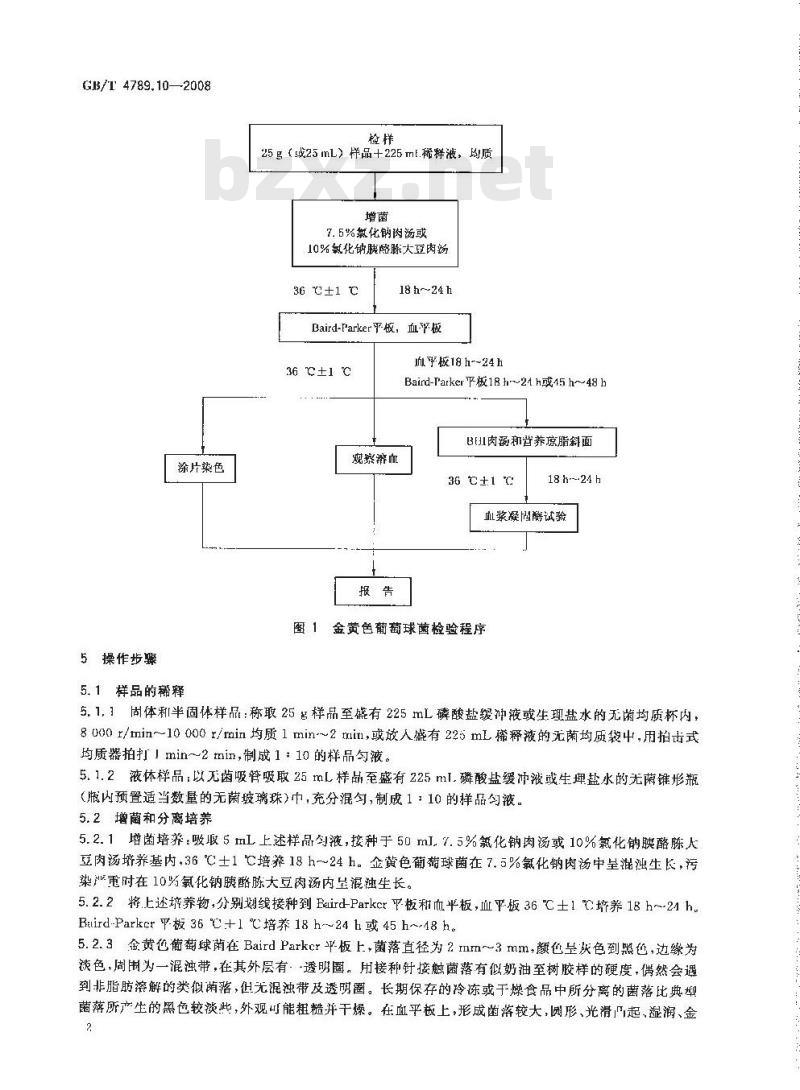
检验程序见图 1。
品成伴网h
GB/T 4789.10—2008
涂片染色
5操作步骤
5.1样品的稀释
25g(或25mL)样品+225mt.稀释液,均质增菌
7.5%氯化钠肉汤或
10%氯化钠胰酪藤大豆肉汤
36 ℃±1 ℃
18 h24h
Baird-Parker平板,血平板
36 ℃± ℃
观察游血
帅板18h-~24h
Baird-Parker平板18 h~21 h或45 h~48 hBEJ肉盈和营养琼脂斜面
36 c±1
18 h--24 h
血浆凝固试验
图1金黄色葡萄球菌检验程序
5.1.1固体和半固体样品:称取25g样品至盛有225mL磷酸盐缓冲液或生现盐水的无菌均质杯内,8000r/min~10000r/rmin均质1min2mit,或放人盛有225mL稀释液的无菌均质袋中,用拍击式均质器拍打!min~2min,制成1:10的样品匀液。5.1.2液体样品:以无菌吸管吸取25mL样品至盛有225ml.磷酸盐缓冲液或生盐水的无菌罐形瓶(瓶内预置适当数量的无菌玻璃珠巾,充分混匀,制成1:10的样品勾液。5.2增菌和分离培养
5.2.1增菌培养:吸圾5mL上述样品匀液,按种于50mI.7.5%氟化钠肉汤或10%氯化钠胰酪陈人豆肉汤培养基内,36℃士1C培18h24h。金黄色葡葡球菌在7.5%氯化钠肉汤中呈混浊生长,污染严重时在10头氯化钠胰酪陈大豆肉汤内呈混独生长。5.2.2将上述培养物,分别划线接种到Baird-Parkcr平板和血平板,血平板36℃土1C培养18h~24h。Baird-Parkcr乎板36℃+1℃培养18 h-~24h或 45h~48 h。5.2.3金黄色葡萄球南在BairdParkcr平板上,菌落直径为2Im~3mm,颜色呈灰色到黑色,边缘为淡色,周围为一混浊带,在其外层有,透明圈。用接种针接触菌落有似奶油至树胶样的硬度,偶然会遇到非脂肪解的类似菌落,但光混独带及透明圈。长期保存的冷冻或于燥食品中所分离的菌落比典型菌落所产生的黑色较淡些,外观可能粗糙并干燥。在血平板上,形成菌落较大,圆形、光滑起、湿润、金2
btt
GB/T4789.10—200B
黄色(有时为白色).菌落周围可见完全透明溶血圈。挑取上述菌落进行革兰氏染色镜检及血浆凝固酶试验。
5.2.4形态:翁黄色葡萄球菌为革兰氏阳性球菌.排列呈葡萄球状,无芽胞,无英膜,直径约为0.5μm1μm。
5.3血浆凝固酶试验
5.3.1挑取Baird-Parkcr板或血平板上可疑菌落1个或以上,分别接种到5nL BHI和营养琼脂斜面,36℃±1℃培养18h~24h
5.3.2取新鲜配制免血浆0.5ml,放人小试管中,再加人5.3.1BH1培养物0.2mL0.3ml搬荡搭匀,置36℃工1℃温箱或水浴箱内,每半小时观察一次,观察6h,如呈现凝固(即将试节倾斜或倒置时,呈现凝块)或凝固体积人于原体积的半,被判定为阳性结果。同时以血浆凝固酶试验阳性和阴性葡萄球菌菌株的肉培养物作为对照。也可用商品化的试剂,按说明书操作,进行血浆凝固酶试验。5. 3. 3结果如可疑,挑取营养琼脂斜面的菌落到 5 mL BHI.36 ℃ 1 ℃培养 18 h-~48 h,重复 5. 3,2。5.4葡萄球菌肠毒素的捡测
可食物中毒样品产生葡萄球菌肠毒素的金黄色葡萄球菌菌株的鉴定,应按附录B检测葡荷球蘭炀毒素.
6结果与报告
6.1结果判定:衍合5.2.3、5.2.4.血浆凝固酶试验阳性,可判定为金黄色葡萄球菌。6.2结果报告:在25g(或25mL.)样品中检出或末检出金黄色葡球菌。3
GB/T4789.10-2008
A.110%氯化钠胰酪陈大豆肉汤
A.1.1成分
胰酪豚(或胰蛋白陈)
植物蛋白陈(或火豆蛋白陈)
氯化钠
磷酸氢二钾
丙酶酸钠
葡萄糖
蒸馏水
pH7. 3+0.2
A.1.2制法
附录A
(规范性附录)
培养基和试剂
1000 mL
将上述成分混合,加热,轻轻搅拌并溶解,调节pH,分装,每瓶50mL,121℃高压灭菌15min。A.27.5%氯化钠肉汤
A,2.1成分
蛋白陈
牛肉膏
氯化钠
蒸馏水
A.2.2制法
1 000 ml.
将上述成分加热溶解,调节pH,分装,每瓶50mL,121℃高压灭菌15min。3血琼脂平板
A.3.1成分
豆粉琼脂(pH7.4~7.6)
脱纤维羊血(或兔血)
A.3.2制法
5 mL~-10 mL
热溶化琼脂,冷却至50℃,以无菌操作加人脱纤继羊血(或兔血),播匀,倾注平板A,4Baird-Parker琼脂平板
A.4.1成分
胰蛋白陈
牛肉旁
酵母膏
丙酮酸钠
甘氨氮酸
品伴网httn
氯化锂(LiC1·6H,O)
蒸馏水
pH7.0-+0. 2
A.4,2增菌剂的配法
GB/T 4789.10—2008
30%卵黄盐水50InL与经过除菌过滤的1%亚碲酸钾溶液10mL混合·保存于冰箱内。A.4.3制法
将各成分加到蒸馏水中,加热煮沸至完全溶解,调节pH。分装每瓶95mL,121℃高压灭菌15min。临用时加热溶化琼脂,冷至50℃,每95mL加入预热至50℃的卵黄亚确酸钾增菌剂5mL,摇后倾注平板。培养基应是致密不透明的。使用前在冰箱储存不得超过48 h。A.5脑心浸出液(BHI)肉汤
A.5. 1 成分
胰蛋白质陈
氯化钠
磷酸氢二钠(Na2HPO·12H,O)
葡萄糖
非心浸出液
pH7.4±0.2
A.5. 2制法
加热溶解,调节pH,分装16mm×160mm试管,每管5mL.置121℃,15min火菌,A.6兔血浆
取柠檬酸钠3.8g,加蒸熔水100mL,溶解后过滤,装瓶,121℃高压灭菌15min。免血浆制备:取3.8%柠檬酸钠溶液一份,加兔全血四份,混好静置(或以3000r/min离心30min),使血液细胞下降,即可得血浆。
A.7磷酸盐缓冲液
A.7、1成分
磷酸二氢钾(KH,PO)
蒸馏水
A.7.2制法
贮存液:称取 34. 0 g的磷酸二氢钾溶于 500mL蒸馏水中,用大约175 mL的! mol/L氢氢化钠溶液调节pH至7.2,用蒸馏水稀释至1000mL后贮存于冰箱。稀释液:取必存液1.25mL,用蒸馏水稀释至1U00mL,分装于适宜容器中,121℃高压灭菌15min。
A.8营养琼脂斜面
A,8.1成分
蛋白陈
牛肉旁
品球科网
GB/T4789.10—2008
蒸馏水
pH7. 2~-7. 4
A,B.2制法
15g~20g
1 000 ml
将除琼胎以外的各成分溶解于蒸馏水内,加人15%签氧化钠溶液约2mL,校正pH至7.2~7.1。加人琼脂,加热煮沸,使琼脂溶化,分装13mm×130mm管,121℃高压灭菌15min。A.9革兰氏染色液
A.9、1结晶染色液
A. 9. 1. 1 成分
结晶紫
95%乙醇
1%草酸铵水溶液
A, 9. 1. 2制法
将结晶紫完全解于乙醇中,然后与草酸铵溶液混合。A.9.2革兰氏碘液
A.9.2.1成分
碘化钾
蒸馏水
A.9.2.2制法
将碘与碘化钾先行混合,加入蒸馏水少许充分振播,待究企溶解后,再加蒸馏水至300mL。A.9.3沙黄复染液
A.9.3.1成分
95%乙醇
蒸馏水
A, 9. 3.2制法
将沙黄溶解于乙醇中,然后用蒸馅水稀释。A.9.4染色法
A.9.4.1涂片在火焰上固定,滴加结晶紫染液,染1min,水洗。A.9.4.2滴加革兰氏碘液,作用1min,水洗。A.9.4.3滴加95%乙醇脱色约15s~~30s,真至染色液被洗掉,不要过分脱色,水洗。A.9.4.4滴加复染液,复染1min,水洗、待·、镜检。6
合伙伴网
B.1设备和材料
B. 1. 1 冰箱:0 ℃~4 ℃。
附录B
(规范性附录)
葡萄球菌肠霉素检测方法
B.1.2恒温或振荡培养箱:36℃+1℃。B. 1. 3
酶标仪。
B.1.4离心机:80001/min。
B.1.5均质器或火菌乳。
层祈柱:40mmX(20mm~25mm)。
微量加样器:200 uI、50 u。
细滴管。
B. 1. 9 分液斗。
透析袋。
洗瓶。www.bzxz.net
灭菌吸管:1mL(具0.01ml.刻度)、10mL(真0.1ml.刻度),灭菌培养ⅢL:径 150 mm。
灭菌锥形瓶:250 mL
有机玻璃模板。
打孔器:直径 2. 5 mm。
载玻片、橡皮圈。
灭菌玻璃纸、L棒、锻子等。
B.2培养基和试剂
B.2.1肠萨素产毒培养基:
B.2.1.1成分
蛋白陈
胰消化酪蛋白
氯化钠
磷酸氢二钾
磷酸二氢钾
氯化钙
硫酸镁
蒸馏水
1 000 ml.
10 g~12g(固体透析培养用)
GB/T 4789.10—2008
B. 2. 1. 2制法
除琼脂外将所有成分混于水中,溶解后调pH7.2~7.4,如用固体透析培养法再加人琼脂,121℃高压灭菌 30 min。
B.2.2营养琼脂:
B.2.2.1成分
蛋白陈
http
GR/T 4789.10—2008
牛肉膏
氯化钠
蒸馏水
B.2.2.2制法
1 000 mL
将除琼脂以外的各成分溶解于蒸馏水内,加人15%氢氧化钠溶液约2mL,校止pH7.2~-7.4。加人琼脂,加热煮沸,121C高压灭菌15minB.2.31%琼脂糖溶液(0.9%生理盐水配制)。B.2.40.2mol/LPH7.5磷酸盐缓冲液。B.2.5
三氯甲烷。
6mol/L盐酸溶液。
5mol/L氢氧化钠。
0.85%生理盐水。
1%乙酸溶液。
0.1%壤嗪红R或氨基黑B。
硅胶或凡土林。
A,B、C、D型葡萄球菌肠毒素和抗血清,羧甲基纤维素(CM22或CM11Whatnan)0.2mol/LpH6.8磷酸盐缓冲液。
酶标记A、B、C、D肠荷素抗血清或酶联免疫试剂盒0.1mol/LH9.5碳酸缓冲液。
0.05%0.02mal/L.PH7.2温-20缓冲液。邻苯二胺酶底物。
2 mol/L 梳酸。
检测程序
从分离菌株培养物中检测葡萄球菌肠毒素,检测流程见图B.1。菌株
营养琼胎斜面36℃±1℃,18h~24h用盐水洗下菌苔,放入产毒培养基固体培养法:36℃±1培养48h
液体培养汰:36C±1操蒋培养48h8000r/min离心20min,取上清液,加热10010min,8000t/min离心10mit,取上消液,浓缩双相琼脂扩散:微玻片法战玻片法检测葡葡球菌肠毒素报告
图B.1分离菌株培养物中葡萄球菌肠毒素的检测流程图合品球伴网httn
E.3.2从食物样品中提取和检测谢萄球菌肠毒素GB/T 4789.102008
B.3.2.1微玻片法检测食品中葡葡球菌肠毒素(浓缩法和层析法)流程,见图B.2。固体格样100g如入0.2mol/L.H7.5解龄盐缓冲100mL,1C浸泡18 h~24 h;液体检样直接吸取100 mL固体拉样用纱布过滤
液体检样:离心8 000 rinit 20 min取 上清液固体检样:离心8 000 rimin 20 min取,L消液加入三氮甲烷10 ml.-15 ml.,报荡10 imin,静置,弃去三氯甲烷加入6toll,盐酸济液调l1至4.5:B000r/min,20min,取上清液加入5tnol/L氢氧化钠游液,调pH至7.5,8000t/min,20min取上清液,放入透析内,放多聚乙醇或用电风扇吹干,浓缩到1 iml.--2 mL用微玻片法检测菌萄球菌肠毒素报告
浓缔法
用蒸增水洗下浓缩物
装入透析袋,以0.008ol/LpII5.6磷酸盐缓冲波平衡过CM层析柱(流魂l mlmin~2 mL/min)用0.008mol/LpH5.6磷酸盐缓冲波药1(00 ml,洗脱用0.2mol/LpIG.8磷酸盐缓冲波洗脱出葡萄球菌肠毒素用微玻片法极测葡萄球菌肠毒素报告
层析法
图B.2微玻片法检测葡萄球菌肠毒素(浓缩法和层析法)流程图e
小提示:此标准内容仅展示完整标准里的部分截取内容,若需要完整标准请到上方自行免费下载完整标准文档。
中华人民共和国国家标准
GB/T 4789.10—2008
代替GB/T4789.102003
食品卫生微生物学检验
金黄色葡萄球菌检验
Microbiological examination of food hygiene-Detection of Sta phyiococcus aureus2008-11-21发布
中华人民共和国卫生部
中国国家标准化管理委员会
2009-03-01实施
中华人民共和国
国家标准
食品卫生微生物学检验
金黄色葡萄球菌检验
GB/T4789.10—2008
中国标准出版社出版发行
北京复兴门外三里河北街16号
邮政编码:100015
网址 spc. nct. cn
电话:6852394668517548
中国标准出版杜案皇岛印刷厂印剧各地新华书店经销
开本880×1230
印张1
字数 21 千字
2009年3月第一版
2009年3月第一次印刷
号:155066·136102
如有印装差错
定价16.00元
由本社发行中心调换
版权专有权必究
举报电话:(010)68533533
http://foodmate.net言
GB/T 4789.10--2008
本标准对应于国际分析家学会(AOACINTFRNATIONAT)AOAC987.09食品中金黄色葡葡球菌分离和计数 MPN法\(1991 年)(AOAC Official Method 987.09,Staphytococcus aureus in faodsmostprobablenumbermcthodforisolationandcnumcration)和国际标雅化组织ISQ68881:1999《食品和动物何料中而浆凝固酶阳性葡萄球菌、金黄色葡药球菌和其他葡萄球菌计数方法》(Microbiologyof food and animal fccding stuffs Horizontal method for the cnumcration of coagulase-pusitive staph-ytococci, Staphytococcus aureaus end other species-Pur1 l: Technique using Baird-Parker agar mcdium)。本标准与A0ACOfficialMethod987.09、ISO6B88-1:1999的一致性程度为非等效。本标代替GB/T4789.102003食品卫生微生物学检验金黄色葡萄球菌检验》。本标准与GB/T 4789.10—2003比主要修改如下:规范了样品制备过程;
对原标准中血浆凝固酶部分逃行了修改。本标的附录 A,附录 B为规范性附录。本标摊由中华人民共和国卫生部提出并归口。本标准由中华人民共和国卫生部负贵解释。本标准负责起草单位:中国疾病预防控制中心营养与食品安全所。本标准参与起草单位:上海市疾病预防控制中心、中华人民共和国辽宁出人境检验检疫局、中华人民共和国内篆古出人境检验捡疫局,江苏省疾病预防控制中心。本标准主要起草人:刘秀梅、陈敏、刘弘、刘中学、卢行安、袁宝君、田静。本标准所代替标准的历次版本发布情况为:G 1789. 10—1984,GB/T 4789.10—1994,GB/T 4789.102003.1范围
食品卫生微生物学检验
金黄色葡萄球菌检验
本标推规定了食品中金黄色葡葡球菌的检验方法。本标准适用于各类食品和食物中毒样品中金黄色葡萄球菌的检验。2设备和材料
除微生物实验室常规灭菌及培养设备外,其他设备和材料如下:2.1恒温培养箱:36 ℃+1℃,
2.2冰箱:2~5℃。
2.3恒温水浴箱:37℃士1℃。
2.4天半:感量0.1g。
2.5均质器:
2.6振滋器,
GB/T 4789.10—2008
2.7无菌吸管:1mL具0.01mL刻度).10mL(具0.【mL刻度)或微量移液器及吸头。2.8无菌锥形瓶:容量100 mL、500 mL。2.9尤菌培养Ⅲl:直径90mm。
2.10注射器:0.5mL
2. 11 pH 计或 pH 比色管或精密 pH 试纸,3培养基和试剂
3.110%氯化钠胰酪陈人豆肉汤:见第A.1章。3, 2 7. 5%氯化钠肉汤;见第 A, 2 章。3.3血琼脂平板:见第A,3章,
3,4 Baird-Parkcr琼脂平板:见第 A.4章。3.5脑心浸出液(BHI)肉汤:见第A.5章。3. 6 免血浆;见第 A. 6 章。
磷酸盐缓冲液:见第A.7章。
3.8营养琼脂斜面:见第A.8章。3, 9革兰氏染色液:见第 A. 9 章。3.10无菌生理盐水:称取8.5g氯化钠溶于1000mL蒸馅水中,121℃高压灭菌15nin。3.111mol/L氢氧化钠(NaOH):称取10g氢氧化钢(NaOH)溶于1000mL蒸馏水中。3.121mol/1盐酸(HCl):37%浓盐酸90mL.加蒸馏水到1000mL。4 检验程序
检验程序见图 1。
品成伴网h
GB/T 4789.10—2008
涂片染色
5操作步骤
5.1样品的稀释
25g(或25mL)样品+225mt.稀释液,均质增菌
7.5%氯化钠肉汤或
10%氯化钠胰酪藤大豆肉汤
36 ℃±1 ℃
18 h24h
Baird-Parker平板,血平板
36 ℃± ℃
观察游血
帅板18h-~24h
Baird-Parker平板18 h~21 h或45 h~48 hBEJ肉盈和营养琼脂斜面
36 c±1
18 h--24 h
血浆凝固试验
图1金黄色葡萄球菌检验程序
5.1.1固体和半固体样品:称取25g样品至盛有225mL磷酸盐缓冲液或生现盐水的无菌均质杯内,8000r/min~10000r/rmin均质1min2mit,或放人盛有225mL稀释液的无菌均质袋中,用拍击式均质器拍打!min~2min,制成1:10的样品匀液。5.1.2液体样品:以无菌吸管吸取25mL样品至盛有225ml.磷酸盐缓冲液或生盐水的无菌罐形瓶(瓶内预置适当数量的无菌玻璃珠巾,充分混匀,制成1:10的样品勾液。5.2增菌和分离培养
5.2.1增菌培养:吸圾5mL上述样品匀液,按种于50mI.7.5%氟化钠肉汤或10%氯化钠胰酪陈人豆肉汤培养基内,36℃士1C培18h24h。金黄色葡葡球菌在7.5%氯化钠肉汤中呈混浊生长,污染严重时在10头氯化钠胰酪陈大豆肉汤内呈混独生长。5.2.2将上述培养物,分别划线接种到Baird-Parkcr平板和血平板,血平板36℃土1C培养18h~24h。Baird-Parkcr乎板36℃+1℃培养18 h-~24h或 45h~48 h。5.2.3金黄色葡萄球南在BairdParkcr平板上,菌落直径为2Im~3mm,颜色呈灰色到黑色,边缘为淡色,周围为一混浊带,在其外层有,透明圈。用接种针接触菌落有似奶油至树胶样的硬度,偶然会遇到非脂肪解的类似菌落,但光混独带及透明圈。长期保存的冷冻或于燥食品中所分离的菌落比典型菌落所产生的黑色较淡些,外观可能粗糙并干燥。在血平板上,形成菌落较大,圆形、光滑起、湿润、金2
btt
GB/T4789.10—200B
黄色(有时为白色).菌落周围可见完全透明溶血圈。挑取上述菌落进行革兰氏染色镜检及血浆凝固酶试验。
5.2.4形态:翁黄色葡萄球菌为革兰氏阳性球菌.排列呈葡萄球状,无芽胞,无英膜,直径约为0.5μm1μm。
5.3血浆凝固酶试验
5.3.1挑取Baird-Parkcr板或血平板上可疑菌落1个或以上,分别接种到5nL BHI和营养琼脂斜面,36℃±1℃培养18h~24h
5.3.2取新鲜配制免血浆0.5ml,放人小试管中,再加人5.3.1BH1培养物0.2mL0.3ml搬荡搭匀,置36℃工1℃温箱或水浴箱内,每半小时观察一次,观察6h,如呈现凝固(即将试节倾斜或倒置时,呈现凝块)或凝固体积人于原体积的半,被判定为阳性结果。同时以血浆凝固酶试验阳性和阴性葡萄球菌菌株的肉培养物作为对照。也可用商品化的试剂,按说明书操作,进行血浆凝固酶试验。5. 3. 3结果如可疑,挑取营养琼脂斜面的菌落到 5 mL BHI.36 ℃ 1 ℃培养 18 h-~48 h,重复 5. 3,2。5.4葡萄球菌肠毒素的捡测
可食物中毒样品产生葡萄球菌肠毒素的金黄色葡萄球菌菌株的鉴定,应按附录B检测葡荷球蘭炀毒素.
6结果与报告
6.1结果判定:衍合5.2.3、5.2.4.血浆凝固酶试验阳性,可判定为金黄色葡萄球菌。6.2结果报告:在25g(或25mL.)样品中检出或末检出金黄色葡球菌。3
GB/T4789.10-2008
A.110%氯化钠胰酪陈大豆肉汤
A.1.1成分
胰酪豚(或胰蛋白陈)
植物蛋白陈(或火豆蛋白陈)
氯化钠
磷酸氢二钾
丙酶酸钠
葡萄糖
蒸馏水
pH7. 3+0.2
A.1.2制法
附录A
(规范性附录)
培养基和试剂
1000 mL
将上述成分混合,加热,轻轻搅拌并溶解,调节pH,分装,每瓶50mL,121℃高压灭菌15min。A.27.5%氯化钠肉汤
A,2.1成分
蛋白陈
牛肉膏
氯化钠
蒸馏水
A.2.2制法
1 000 ml.
将上述成分加热溶解,调节pH,分装,每瓶50mL,121℃高压灭菌15min。3血琼脂平板
A.3.1成分
豆粉琼脂(pH7.4~7.6)
脱纤维羊血(或兔血)
A.3.2制法
5 mL~-10 mL
热溶化琼脂,冷却至50℃,以无菌操作加人脱纤继羊血(或兔血),播匀,倾注平板A,4Baird-Parker琼脂平板
A.4.1成分
胰蛋白陈
牛肉旁
酵母膏
丙酮酸钠
甘氨氮酸
品伴网httn
氯化锂(LiC1·6H,O)
蒸馏水
pH7.0-+0. 2
A.4,2增菌剂的配法
GB/T 4789.10—2008
30%卵黄盐水50InL与经过除菌过滤的1%亚碲酸钾溶液10mL混合·保存于冰箱内。A.4.3制法
将各成分加到蒸馏水中,加热煮沸至完全溶解,调节pH。分装每瓶95mL,121℃高压灭菌15min。临用时加热溶化琼脂,冷至50℃,每95mL加入预热至50℃的卵黄亚确酸钾增菌剂5mL,摇后倾注平板。培养基应是致密不透明的。使用前在冰箱储存不得超过48 h。A.5脑心浸出液(BHI)肉汤
A.5. 1 成分
胰蛋白质陈
氯化钠
磷酸氢二钠(Na2HPO·12H,O)
葡萄糖
非心浸出液
pH7.4±0.2
A.5. 2制法
加热溶解,调节pH,分装16mm×160mm试管,每管5mL.置121℃,15min火菌,A.6兔血浆
取柠檬酸钠3.8g,加蒸熔水100mL,溶解后过滤,装瓶,121℃高压灭菌15min。免血浆制备:取3.8%柠檬酸钠溶液一份,加兔全血四份,混好静置(或以3000r/min离心30min),使血液细胞下降,即可得血浆。
A.7磷酸盐缓冲液
A.7、1成分
磷酸二氢钾(KH,PO)
蒸馏水
A.7.2制法
贮存液:称取 34. 0 g的磷酸二氢钾溶于 500mL蒸馏水中,用大约175 mL的! mol/L氢氢化钠溶液调节pH至7.2,用蒸馏水稀释至1000mL后贮存于冰箱。稀释液:取必存液1.25mL,用蒸馏水稀释至1U00mL,分装于适宜容器中,121℃高压灭菌15min。
A.8营养琼脂斜面
A,8.1成分
蛋白陈
牛肉旁
品球科网
GB/T4789.10—2008
蒸馏水
pH7. 2~-7. 4
A,B.2制法
15g~20g
1 000 ml
将除琼胎以外的各成分溶解于蒸馏水内,加人15%签氧化钠溶液约2mL,校正pH至7.2~7.1。加人琼脂,加热煮沸,使琼脂溶化,分装13mm×130mm管,121℃高压灭菌15min。A.9革兰氏染色液
A.9、1结晶染色液
A. 9. 1. 1 成分
结晶紫
95%乙醇
1%草酸铵水溶液
A, 9. 1. 2制法
将结晶紫完全解于乙醇中,然后与草酸铵溶液混合。A.9.2革兰氏碘液
A.9.2.1成分
碘化钾
蒸馏水
A.9.2.2制法
将碘与碘化钾先行混合,加入蒸馏水少许充分振播,待究企溶解后,再加蒸馏水至300mL。A.9.3沙黄复染液
A.9.3.1成分
95%乙醇
蒸馏水
A, 9. 3.2制法
将沙黄溶解于乙醇中,然后用蒸馅水稀释。A.9.4染色法
A.9.4.1涂片在火焰上固定,滴加结晶紫染液,染1min,水洗。A.9.4.2滴加革兰氏碘液,作用1min,水洗。A.9.4.3滴加95%乙醇脱色约15s~~30s,真至染色液被洗掉,不要过分脱色,水洗。A.9.4.4滴加复染液,复染1min,水洗、待·、镜检。6
合伙伴网
B.1设备和材料
B. 1. 1 冰箱:0 ℃~4 ℃。
附录B
(规范性附录)
葡萄球菌肠霉素检测方法
B.1.2恒温或振荡培养箱:36℃+1℃。B. 1. 3
酶标仪。
B.1.4离心机:80001/min。
B.1.5均质器或火菌乳。
层祈柱:40mmX(20mm~25mm)。
微量加样器:200 uI、50 u。
细滴管。
B. 1. 9 分液斗。
透析袋。
洗瓶。www.bzxz.net
灭菌吸管:1mL(具0.01ml.刻度)、10mL(真0.1ml.刻度),灭菌培养ⅢL:径 150 mm。
灭菌锥形瓶:250 mL
有机玻璃模板。
打孔器:直径 2. 5 mm。
载玻片、橡皮圈。
灭菌玻璃纸、L棒、锻子等。
B.2培养基和试剂
B.2.1肠萨素产毒培养基:
B.2.1.1成分
蛋白陈
胰消化酪蛋白
氯化钠
磷酸氢二钾
磷酸二氢钾
氯化钙
硫酸镁
蒸馏水
1 000 ml.
10 g~12g(固体透析培养用)
GB/T 4789.10—2008
B. 2. 1. 2制法
除琼脂外将所有成分混于水中,溶解后调pH7.2~7.4,如用固体透析培养法再加人琼脂,121℃高压灭菌 30 min。
B.2.2营养琼脂:
B.2.2.1成分
蛋白陈
http
GR/T 4789.10—2008
牛肉膏
氯化钠
蒸馏水
B.2.2.2制法
1 000 mL
将除琼脂以外的各成分溶解于蒸馏水内,加人15%氢氧化钠溶液约2mL,校止pH7.2~-7.4。加人琼脂,加热煮沸,121C高压灭菌15minB.2.31%琼脂糖溶液(0.9%生理盐水配制)。B.2.40.2mol/LPH7.5磷酸盐缓冲液。B.2.5
三氯甲烷。
6mol/L盐酸溶液。
5mol/L氢氧化钠。
0.85%生理盐水。
1%乙酸溶液。
0.1%壤嗪红R或氨基黑B。
硅胶或凡土林。
A,B、C、D型葡萄球菌肠毒素和抗血清,羧甲基纤维素(CM22或CM11Whatnan)0.2mol/LpH6.8磷酸盐缓冲液。
酶标记A、B、C、D肠荷素抗血清或酶联免疫试剂盒0.1mol/LH9.5碳酸缓冲液。
0.05%0.02mal/L.PH7.2温-20缓冲液。邻苯二胺酶底物。
2 mol/L 梳酸。
检测程序
从分离菌株培养物中检测葡萄球菌肠毒素,检测流程见图B.1。菌株
营养琼胎斜面36℃±1℃,18h~24h用盐水洗下菌苔,放入产毒培养基固体培养法:36℃±1培养48h
液体培养汰:36C±1操蒋培养48h8000r/min离心20min,取上清液,加热10010min,8000t/min离心10mit,取上消液,浓缩双相琼脂扩散:微玻片法战玻片法检测葡葡球菌肠毒素报告
图B.1分离菌株培养物中葡萄球菌肠毒素的检测流程图合品球伴网httn
E.3.2从食物样品中提取和检测谢萄球菌肠毒素GB/T 4789.102008
B.3.2.1微玻片法检测食品中葡葡球菌肠毒素(浓缩法和层析法)流程,见图B.2。固体格样100g如入0.2mol/L.H7.5解龄盐缓冲100mL,1C浸泡18 h~24 h;液体检样直接吸取100 mL固体拉样用纱布过滤
液体检样:离心8 000 rinit 20 min取 上清液固体检样:离心8 000 rimin 20 min取,L消液加入三氮甲烷10 ml.-15 ml.,报荡10 imin,静置,弃去三氯甲烷加入6toll,盐酸济液调l1至4.5:B000r/min,20min,取上清液加入5tnol/L氢氧化钠游液,调pH至7.5,8000t/min,20min取上清液,放入透析内,放多聚乙醇或用电风扇吹干,浓缩到1 iml.--2 mL用微玻片法检测菌萄球菌肠毒素报告
浓缔法
用蒸增水洗下浓缩物
装入透析袋,以0.008ol/LpII5.6磷酸盐缓冲波平衡过CM层析柱(流魂l mlmin~2 mL/min)用0.008mol/LpH5.6磷酸盐缓冲波药1(00 ml,洗脱用0.2mol/LpIG.8磷酸盐缓冲波洗脱出葡萄球菌肠毒素用微玻片法极测葡萄球菌肠毒素报告
层析法
图B.2微玻片法检测葡萄球菌肠毒素(浓缩法和层析法)流程图e
小提示:此标准内容仅展示完整标准里的部分截取内容,若需要完整标准请到上方自行免费下载完整标准文档。
标准图片预览:




- 热门标准
- 国家标准(GB)
- GB/T2828.1-2012 计数抽样检验程序 第1部分:按接收质量限(AQL)检索的逐批检验抽样计划
- GB/T18204.4-2000 公共场所毛巾、床上卧具微生物检验方法细菌总数测定
- GB/T23892.3-2009 滑动轴承 稳态条件下流体动压可倾瓦块止推轴承 第3部分:可倾瓦块止推轴承计算的许用值
- GB/T11839-1989 二氧化铀芯块中硼的测定 姜黄素萃取光度法
- GB/T6122.1-2002 圆角铣刀 第1部分:型式和尺寸
- GB/T7433-1987 对称电缆载波通信系统抗无线电广播和通信干扰的指标
- GB/T21238-2007 玻璃纤维增强塑料夹砂管
- GB/T28809-2012 轨道交通 通信、信号和处理系统 信号用安全相关电子系统
- GB/T9124.1-2019 钢制管法兰 第1部分:PN 系列
- GB17945-2024 消防应急照明和疏散指示系统
- GB15603-2022 危险化学品仓库储存通则
- GB6819-1996 溶解乙炔
- GB/T9239-1988 刚性转子平衡品质 许用不平衡的确定
- GB/T15917.3-1995 金属镝及氧化镝化学分析方法 对氯苯基荧光酮--溴化十六烷基三甲基胺分光光度法测定钽量
- GB/T13985-1992 照相机操作力和强度
- 行业新闻
请牢记:“bzxz.net”即是“标准下载”四个汉字汉语拼音首字母与国际顶级域名“.net”的组合。 ©2025 标准下载网 www.bzxz.net 本站邮件:bzxznet@163.com
网站备案号:湘ICP备2025141790号-2
网站备案号:湘ICP备2025141790号-2