- 您的位置:
- 标准下载网 >>
- 标准分类 >>
- 商检行业标准(SN) >>
- SN/T 2218-2008 进出口动物源性食品中林可酰胺类药物残留量的检测方法 液相色谱-质谱/质谱法
【商检行业标准(SN)】 进出口动物源性食品中林可酰胺类药物残留量的检测方法 液相色谱-质谱/质谱法
本网站 发布时间:
2024-06-28 03:38:26
- SN/T2218-2008
- 现行
- 点击下载此标准
标准号:
SN/T 2218-2008
标准名称:
进出口动物源性食品中林可酰胺类药物残留量的检测方法 液相色谱-质谱/质谱法
标准类别:
商检行业标准(SN)
标准状态:
现行-
发布日期:
2008-11-18 -
实施日期:
2009-06-01 出版语种:
简体中文下载格式:
.rar.pdf下载大小:
1.26 MB
点击下载
标准简介:
标准下载解压密码:www.bzxz.net
SN/T 2218-2008 进出口动物源性食品中林可酰胺类药物残留量的检测方法 液相色谱-质谱/质谱法 SN/T2218-2008
部分标准内容:
中华人民共和国出入境检验检疫行业标准SN/T2218—-2008
进出口动物源食品中林可酰胺类药物残留量检测方法
液色谱-质谱/质谱法
Determination of lincosamide residues in foodstuffs of animal originfor import and export-LC-MS/MS nethod2008-11-18发布
中华人民共和国
国家质量监督检验检疫总局
2009-06-01实施
本标准的附录A和附录B均为资料性附录本标谁出国家认证认可监督管埋委员会提出并[:SN/T2218—2008
本标推起节单位:中华人民共和国深圳山人境检验检疫局,中华人民共和国广东山人境检验检疫局、中华人民共和国浙渐江出人境检验捡疫局:本际雅主要起草人:康游宁、肖锋、沈金灿、林峰、谢文、谢丽琪、韩瑞阳,葛丽雅。本标准系首次发布的出人境检验检疫行业标准,1范围
进出口动物源食品中林可酰胺类药物残留量检测方法
液相色谱-质谱/质谱法
SN/T 2218—2008
本标准规定了动物源食品中林可霉素、吡利素和克林需素残留量检测的制样和液相色谱-质谱/质谱检测方法。
本标准适用丁猪肉、鸡肉、猪肝、牛肝、鸡蛋,牛奶等动物源食品中林可霉素、吡利霉素和克林霉素残留量的检测和确证。
2方法提要
样品中林可酰胺类药物残留经磷酸盐缓冲溶波(pH80)提取,C1s固相萃取柱净化,浓缩、定容后,用液相色谱质谱/质谱法测定和确证,外标法定量。3试剂材料
除另有说明外,所用试剂均为分析纯.水为去离子水3.1甲醇:色谱纯。
3.2甲酸:色谱纯。
3.3氢氧化钠.
3.4氢氧化钠溶液(3mol/L):称取120g氢氧化钠(33)溶于800mmL去离子水中,待冷却至室温后用去离子水定容至1000ml.
3.5磷酸二氢钾。
氢钾(3.5溶解于800ml.水中.用氢氧化钠溶液3.6磷酸盐缓冲溶液(pH8.0)称取680g磷酸3.4)调节pH值对8.0,加水定容至1000mL3.70.1%甲酸水溶液:准确吸取1.0mL甲酸(3.2)于1000mL容量瓶中,加水定容至刻度线,混合均匀。
3.8甲醇+C.1%甲酸水溶液(1-9.体积比):准确量取10mL甲醇3.1)和90mL0.1%中酸水溶液(3.7),混合均匀:
3.9林可酰胺类药物标准晶:林可霉素盐Bincomycin
drochlorideCi.HN,O.S·HC)纯度大于99%.CASNo.:7179-49-9;吡利霉素盐酸盐(Pirlimycinhydrochloride,Cr.HaCIN,O.S·HCI)纯度为86.4%.CASNo.:79548-73-5;克林霉素盐酸盐(Clindamycinhydrochloride,CaHCIN.O.SHCI)纯度为94.5%CASVo.:21462-39-5.3.10标准储备溶液:100mg/L,分别称取适量(精确至0.1mg)林可酰胺类药物标准品(3.9),经折算相当于101g的林可霉素、吡利霉素和克林霉素,置于100mL容量瓶中,用甲醇(3.1)溶解并定容至刻度,混勾,一18℃保存,可使用12个月。3.11混合标准中间溶液:1.0mg/l。分别吸取1.0ml.标准储备溶液(3.10)于100ml容量瓶中,用甲醇(3.1)定容至刻度,4℃保存,可使用3个月3.12基质混合标准工作溶液:吸取适量的混合标准中间溶液(3.11),用空白样品提取液配成浓度为5.0μg/L、10.0cg/L、20.0μg/L.50.0μg/L、100μg/L.200μg/L的基质混合标准工作溶液。使用前配制。
SN/T 2218—2008
3.13C1固相率取样:500)mg6ml.,或相当者。使用前依次用5ml.甲醇、5ml.水、5ml.磷酸盐缓冲辫液(3.6)活化:保持杜体湿润:4仪器和设备
4.1液相色谱-质谱/质谱仪:配电喷雾离子源,4.2分析天:感量0.1g.0.01。
4.3容量瓶:100mL,1000ml.:
4.4聚闪烯离心管:50ml.和15mL.其塞。4.5旋涡混个器。
4.6离心机.
4.8固相率取装置。
4.9机械真空泵。
4.10均质器。
4.11吹氮浓缩仪
4.12膜:0.22um。
5样品制备与保存
5. 1动物肌肉、内脏、蛋
从所取全部样品中取山有代表性样品可食部分约500名·充分捣均约,均分成两份,分删装入洁净容器中,密封,并标明标记,于一18 ℃以下冷冻存放。5.2牛奶
从所取全部样品中政出有代表性样品约5008,均分成满份,分别装入洁净睿器中.密封.并标明标记,于℃冷藏存敲。
6测定步骤
6.1提取
6.1.1动物肌肉、内脏
称收均勾试样2g(精确到0.01g),置于501ml聚丙烯离心管中,加入10ml磷酸盐缓冲溶液(3,6),旋涡混合2 min,9000 r/mit离心5 Imin.提取液转移至另50 mL聚丙烯离心管中,再加入5mI.磷酸盐级冲溶液(3.6),重复七述操作两次,合并提取液,混匀,待净化,6.1.2蛋、牛奶
称取均勾样品5g(精确到0.0Fg).置下50m.聚内烯离心管中.川人20ml.磷酸就缓冲溶液(3.6),旋涡混个2min,取l0mJ.样液于15mL聚丙烯离心管中.9000r/nin离心5min取上层液,得净化,
6.2净化
滩确移取6,1中提取液5ml.以1涵/s速率过C:固萃取柱(3.13),以5ml.水淋洗小杜,淋洗液完全通过小柱后,抽点空10min以上:以5ml.甲醇(3.1)洗脱洗脱液用15ml.聚丙烯离心管改集,45T下氮气吹至近「,用甲醇一0.1关甲酸水溶液(3.8)定容至1ml.,泥匀。溶液经0.22um滤膜(1.12)过滤.供液相色谱-质谱/质谱测定:6.3测定
6.3.1液相色谱条件
a)色谱柱:c。性1.7μm.0 m×2.1 nm(内径).或当名:2
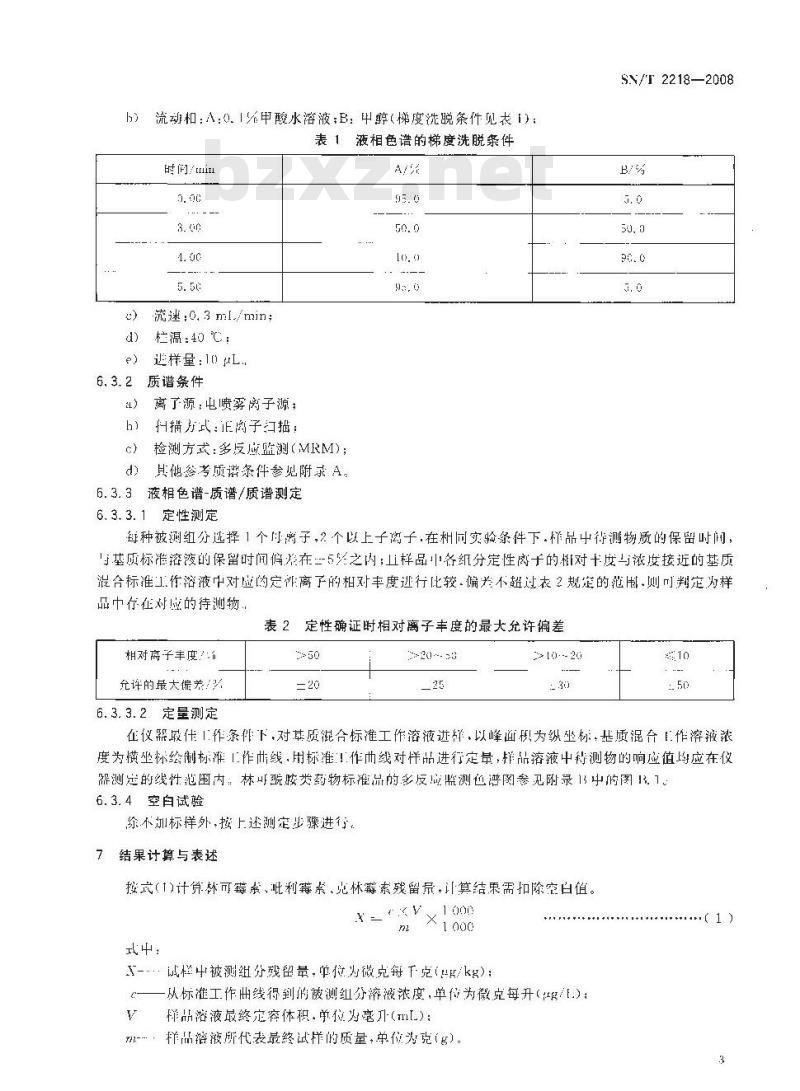
h)流动和:A:0.1%甲酸水溶液;B:甲醇(梯度洗脱条件见表1):表 1、 液相色谱的梯度洗脱条件时间/min
流速;0.3 ml./min;
d)栏温:40℃;
退样量:10#L.
6. 3. 2 质谱条件
让)离了源:电喷雾离子源;
h)扫描方式:正离子扫描:
检测方式:多反应监测(MRM);d)其他参考质谱条件参见附录A,6.3.3液相色谱-质谱/质谱测定
6.3.3.1定性测定
SN/T 2218—2008
每种被测纽分逆择1个呼离子,2个以上子离子.在朴同实验条件下.样品中待测物质的保留时间,与基质标港溶液的保留时间偏关在二5实之内;样品中各组分定性离十的对十度马液度接近的基质混合标准作溶液中对虚的定证离子的相对丰度进行比较-偏关不超过衣2规定的范围.则可判定为样品中存在对应的待测物
表 2定性确证时相对离子丰度的最大允许偏差相对离子丰度:\
允许的最大差/兴
6.3.3.2定量测定
> [0.-- 20
在议器最代1作条件下,对基质混合标准工作溶液进群,以峰面为纵坐标基质混合目作溶液涨度为横坐标绘制标准作也线,用标准!作曲线对样品进行定量,推品溶液中待测物的响应值均应在仪器测定的线性范围内:林可酰胺类药物标准品的多反应监测色谱图参见附录13中的图.1。6.3.4空白试验
除不加标样外,按上述测定步骤进行7 结果计算与表述
按式(I)计算林可霉素、此利霉素、克林藓索残留最,计算结果需扣除空白值。10n
式中:
-试中被测组分残留量,位微克每下克(/kg):从标准工作曲线得到的被测组分溶液浓度,单位为微克每升(/.):样品溶液最终定容体积.单位为毫升(mL):-
样品搭液所代表最终试样的质量,单位为克(g)(1)
SN/T2218—2008
8方法的测定低限与回收率
测定低限
本方法的测定低限均为0.01mg/kg8.2回收率
猪肉、鸡肉、猪肝、牛肝、鸡蛋、牛奶中林可霉素、吡利霉素,克林霉素不同添加水平的回收率数据见表3。
添加水平!
(mg/kg)
林可霉素、吡利霉素、克林霉素不同添加水平的回收率数据化合物名称
林可霉素
吡利霉素
克林素
林可霉素
吡利葡素
克林霉素
林可霉素
吡利霉素
克林霉素
92.7~~103
78.5--104
回收率/%(n—10)
940-113
87/6-112
104e-111
79.2--92.6
5,6~94,4
84.8~96.3
100~110bzxZ.net
76.2--93.4
77.0~89.4
73.4~91.0
70.2~85.8
73,6--89.4
72.9-83,0
80.3~-89.1
65.6--75.9
68.4-~81.3
68.5-82.5
参考质谱条件:
电喷雾电压:3000V
辅助气流速:700L/h;
碰撞气:氩气:
幕帘气流速:50L/h;
离子源温度:105℃
辅助气温度:350℃;
附录A
(资料性附录)
参考质谱条件!
对采集时间、碰撞能量及锥孔电压见表A.1。定性离子对、定量离子对
化合物名称
林可霉素
毗利霉素
克林霉素
定性离子对(m/2)
407/126
4077359
411/112
411/363
425/126
425/378
酰腰类药物测定的质谱参数
定量离子对(
1O7/126
411/112
425/126
采集进间/s
SN/T2218—2008
碰撞气能量/eV
差异,测定前应将质谱参效优化到最住。注:对于不同质谱仪器,仪器参数可能存在锥孔电压/V
非商业性声明:附录A所列参考质谱条件是在WatersQuattroPremier型液质联用仪上完成的,此处列出试验用仪器型号仅为提供参考,并不涉及商业目的.鼓励标准使用者尝试不同厂家或型号的仪器。5
SN/T 2218—2008
407>126
附录H
(资料性附录)
林可酰胺类药物标准的多反应监测色谱图100
Trtimin
a)林霉素
411>363
cl)吡利霉素
407>359
b)林可霉素
+ timin
425>126
-q- tmin
e)克霉素
411>112
c)吡利蒂索
425>78
f)克林素
图 B.110.0 Hg/L林可霉素、吡利霉素和克林霉素标准溶液的多反应监测色谱图t:mm
Foreword
Annex A and B of this standard is an informative annexSN/T2218—2008
This standard was proposed by and is under the charge of the Certification and Accreditation Admin-istration of the People's Republic of China.The standard was drafted by Shenzhen Entry-Exit Inspection and Quarantine Bureau of the People'sRepublic of China, Guangdong Entry-Exit Inspection and Quarantine Bureau of the Peopie's Republicof China, Zhejiang Entry-Exit Inspection and Quarantine Bureau af the Pepple's Republic of China.The main drafters of this standard are Kang Haining. Xiao Feng, Shen Jincan, Lin Feng, Xie Wen,Xie Liqi, Han Ruiyang、Ge Liya.This standard is a professional standard for entry-exit inspection and quarantine promulgated for thefirst time.
Note: This English version, a translation from the Chinese text. ts solely for gcridance.SN/T 2218—2008
Determination of lincosamide residues in foodstuffs ofanimal origin for import and export-L.c-Ms/MS method1Scope
This standard specifies the rnetnods of sampling. cetermiration and corfirmation of lincosamide res-idues.which include lincornycin, pirlirriycin and clindarmyciri. by liquid chromatography tandem massspectrometry(Lc-MS. Ms) in foodstuffs of anirnal origin,This standard is applicable to the determination and confirmation of lincomycin. pirlimycin and clin-damycin in pork. chicken. purcine liver.bovine liver, egg, milk.2Abstract
The lincosamice residues in the test. sample are extracted with phosphate solution ( pH 8, 0), the ex-tract is further cleaneci up by passing through a Ci cartridge or equivalent. The eluate was then con.centratcd , redissolved and determined by Lc-Ms/Ms, using extemal standard method.3Reagents and materials
Unless utherwise specifiec. all reagents should be of analytical grade,\water is deionized water3.1Methanol:HFLC gracde
3.2Formic acid:HPLC grade.
3.3Sodium hydroxide
3.4 Sodiuin hydroxide solition (3 mcl .) : Weigin 120 gj sodium hydroxide i3. 3; and dissolve in800 mL water. then dilute to 1 000 rmil after coul.3. 5Potassitum dilhydroger phosphate3. 6 Phospinate solution (pH 8. 0): Weigh 6. 80 g potassiim dihydrogen phosphate (3. 51. dissolvein 800 mL water: adjust the pH to 8. 0 with sodlium hydroxidle solution (3. 4: anci make up to1 000 mL with water.
3.7 0. 1% formic ncicl solution: Accurately draw 1. 0 rnL formnic acid (3. 2.) into a 1 000 mL volu-metric flask.diute to volume with water. ainri mix to hornogeneity.SN/T2218-—2008
Sampledissolved solvent:Measure 10mLmethanoland90 mL0.1% formic acid (3.7),mix3.8
to homogeneity.
Lincosamidestandards:Lincomycin hydrochloride(C.Ha.N,O,S.HCl,CAsNo.:7179-49-9).3.9
puritymorethan99%;Pirlimycinhydrochloride(CizHa,CIN,O,S·HCl.CASNo.:79548-73-5),purityis86.4%:Clindamycinhydrochloride(C1aHa3CIN2O,SHCl.CASNo.:21462-39-5).purityis94.5%.3.10
Standard stock solutions:Accurately weighadequate lincosamide standard (3.9),whichisequivalentto1o mg lincomycin.pirlimycinand clindamycin,dissolve withmethanol(3.1)tomakea standard stock solution of 100 mg/L in concentration.The solution can bepreserved in thetemper-aturebelow-18fortwelvemonths.3.11
Intermediate standard mixture solution:Accurately draw 1,o mL lincosamide standard stocksolutions(3.10),dilutewithmethanol(3.1)tomediatestandard mixture solution ofmakeaninter
1.O mg/L in concentration. The solution can be preserved in the temperature below 4C for threemonth.
Matrix standard working solutions; According to the requrrement, accurately draw an ade-quate volume of lincosamideintermediate standardmixture solution(3.11),dilute withblank sampleextract solution and prepare a series of matrix standard working.solution of 5. rg/L,10.0 μg/L,20.0μg/L.50.0μg/L,100μg/L,200 μg/L.Thesolutionshouldbeprepared beforeuse.3.13
Ci cartridge:500 mg,6
equivalent. The column is activated with 5mLmethanol.or
beforeuse.Thecolumnshouldbekeptwetalways.5mLwaterand5mLphosphate solution4
Apparatusandequipmen
Liquid chromatography tandem mass spectrometry equipped with electrospray ion source.Analyticalbalance:sensitivity:o.1mg,oo1g.Volumetricflask,100mL1000mL
Polypropylenecentrifugetube:50mLor15mL,withscrewcup.Vortexmixer.
Centrifuge.
Solidphaseextraction.
SN/T 2218——2008
Vacumn pump.
Homogenizer.
Nitrogen evaporator
Membrane filter: 0. 22 μm.
5Samplepreparationandstorage5.1Animal muscle, liver,egg
Choose about 50o g representative sample and prepared it according to analysis requirement in lab.The prepared sample wotuld be devided into two part, and put into sample container, pressurize, anclabel. Sarmple should be kept at - 18 .5.2Milk
Choase about 50o g representative sample, devided into two part, and put into sample container.pressurize,and label.Sample should be kept at 4c.6
Procedure
6.1 Extraction
6.1.1Animalmuscle,liver
Accurately weigh 2 g of the test sample (accurate to 0. o1 g) in a 50 mL polypropylene centrifugetube,add 10 mL phosphate solution (3. 6) : blend for 2 min. centrifuge at 9 000 r/min for 5 min.Transfer the supernate into a 5o mL polypropylene centrifuge tube, Repeat the above extract proce-dure twice with 5 ml. phosphate sofution (3. 6), combine the supernates. mix and prepare for clean-up.
6.1.2 Egg, milk
Accurately weigh 5 g of the test sample (accurate to 0. 01 g) in a 50 mL polypropylene centrifugetube,add 20 mL phosphate solution (3, 6), blend for 2 min. Measure 10 ml blended sample salutioninto a 15 mL polypropylene centrifuge tutbe. centrifuge at 9 000 r/min for 5 min, transfer the super-nate. prepare for cleanup.
6.2 Cleanup
Accurately measure 5 mL extract (6. 1) onto the activated C-s cartridge (3. 13) and keep the flow10
小提示:此标准内容仅展示完整标准里的部分截取内容,若需要完整标准请到上方自行免费下载完整标准文档。
进出口动物源食品中林可酰胺类药物残留量检测方法
液色谱-质谱/质谱法
Determination of lincosamide residues in foodstuffs of animal originfor import and export-LC-MS/MS nethod2008-11-18发布
中华人民共和国
国家质量监督检验检疫总局
2009-06-01实施
本标准的附录A和附录B均为资料性附录本标谁出国家认证认可监督管埋委员会提出并[:SN/T2218—2008
本标推起节单位:中华人民共和国深圳山人境检验检疫局,中华人民共和国广东山人境检验检疫局、中华人民共和国浙渐江出人境检验捡疫局:本际雅主要起草人:康游宁、肖锋、沈金灿、林峰、谢文、谢丽琪、韩瑞阳,葛丽雅。本标准系首次发布的出人境检验检疫行业标准,1范围
进出口动物源食品中林可酰胺类药物残留量检测方法
液相色谱-质谱/质谱法
SN/T 2218—2008
本标准规定了动物源食品中林可霉素、吡利素和克林需素残留量检测的制样和液相色谱-质谱/质谱检测方法。
本标准适用丁猪肉、鸡肉、猪肝、牛肝、鸡蛋,牛奶等动物源食品中林可霉素、吡利霉素和克林霉素残留量的检测和确证。
2方法提要
样品中林可酰胺类药物残留经磷酸盐缓冲溶波(pH80)提取,C1s固相萃取柱净化,浓缩、定容后,用液相色谱质谱/质谱法测定和确证,外标法定量。3试剂材料
除另有说明外,所用试剂均为分析纯.水为去离子水3.1甲醇:色谱纯。
3.2甲酸:色谱纯。
3.3氢氧化钠.
3.4氢氧化钠溶液(3mol/L):称取120g氢氧化钠(33)溶于800mmL去离子水中,待冷却至室温后用去离子水定容至1000ml.
3.5磷酸二氢钾。
氢钾(3.5溶解于800ml.水中.用氢氧化钠溶液3.6磷酸盐缓冲溶液(pH8.0)称取680g磷酸3.4)调节pH值对8.0,加水定容至1000mL3.70.1%甲酸水溶液:准确吸取1.0mL甲酸(3.2)于1000mL容量瓶中,加水定容至刻度线,混合均匀。
3.8甲醇+C.1%甲酸水溶液(1-9.体积比):准确量取10mL甲醇3.1)和90mL0.1%中酸水溶液(3.7),混合均匀:
3.9林可酰胺类药物标准晶:林可霉素盐Bincomycin
drochlorideCi.HN,O.S·HC)纯度大于99%.CASNo.:7179-49-9;吡利霉素盐酸盐(Pirlimycinhydrochloride,Cr.HaCIN,O.S·HCI)纯度为86.4%.CASNo.:79548-73-5;克林霉素盐酸盐(Clindamycinhydrochloride,CaHCIN.O.SHCI)纯度为94.5%CASVo.:21462-39-5.3.10标准储备溶液:100mg/L,分别称取适量(精确至0.1mg)林可酰胺类药物标准品(3.9),经折算相当于101g的林可霉素、吡利霉素和克林霉素,置于100mL容量瓶中,用甲醇(3.1)溶解并定容至刻度,混勾,一18℃保存,可使用12个月。3.11混合标准中间溶液:1.0mg/l。分别吸取1.0ml.标准储备溶液(3.10)于100ml容量瓶中,用甲醇(3.1)定容至刻度,4℃保存,可使用3个月3.12基质混合标准工作溶液:吸取适量的混合标准中间溶液(3.11),用空白样品提取液配成浓度为5.0μg/L、10.0cg/L、20.0μg/L.50.0μg/L、100μg/L.200μg/L的基质混合标准工作溶液。使用前配制。
SN/T 2218—2008
3.13C1固相率取样:500)mg6ml.,或相当者。使用前依次用5ml.甲醇、5ml.水、5ml.磷酸盐缓冲辫液(3.6)活化:保持杜体湿润:4仪器和设备
4.1液相色谱-质谱/质谱仪:配电喷雾离子源,4.2分析天:感量0.1g.0.01。
4.3容量瓶:100mL,1000ml.:
4.4聚闪烯离心管:50ml.和15mL.其塞。4.5旋涡混个器。
4.6离心机.
4.8固相率取装置。
4.9机械真空泵。
4.10均质器。
4.11吹氮浓缩仪
4.12膜:0.22um。
5样品制备与保存
5. 1动物肌肉、内脏、蛋
从所取全部样品中取山有代表性样品可食部分约500名·充分捣均约,均分成两份,分删装入洁净容器中,密封,并标明标记,于一18 ℃以下冷冻存放。5.2牛奶
从所取全部样品中政出有代表性样品约5008,均分成满份,分别装入洁净睿器中.密封.并标明标记,于℃冷藏存敲。
6测定步骤
6.1提取
6.1.1动物肌肉、内脏
称收均勾试样2g(精确到0.01g),置于501ml聚丙烯离心管中,加入10ml磷酸盐缓冲溶液(3,6),旋涡混合2 min,9000 r/mit离心5 Imin.提取液转移至另50 mL聚丙烯离心管中,再加入5mI.磷酸盐级冲溶液(3.6),重复七述操作两次,合并提取液,混匀,待净化,6.1.2蛋、牛奶
称取均勾样品5g(精确到0.0Fg).置下50m.聚内烯离心管中.川人20ml.磷酸就缓冲溶液(3.6),旋涡混个2min,取l0mJ.样液于15mL聚丙烯离心管中.9000r/nin离心5min取上层液,得净化,
6.2净化
滩确移取6,1中提取液5ml.以1涵/s速率过C:固萃取柱(3.13),以5ml.水淋洗小杜,淋洗液完全通过小柱后,抽点空10min以上:以5ml.甲醇(3.1)洗脱洗脱液用15ml.聚丙烯离心管改集,45T下氮气吹至近「,用甲醇一0.1关甲酸水溶液(3.8)定容至1ml.,泥匀。溶液经0.22um滤膜(1.12)过滤.供液相色谱-质谱/质谱测定:6.3测定
6.3.1液相色谱条件
a)色谱柱:c。性1.7μm.0 m×2.1 nm(内径).或当名:2
h)流动和:A:0.1%甲酸水溶液;B:甲醇(梯度洗脱条件见表1):表 1、 液相色谱的梯度洗脱条件时间/min
流速;0.3 ml./min;
d)栏温:40℃;
退样量:10#L.
6. 3. 2 质谱条件
让)离了源:电喷雾离子源;
h)扫描方式:正离子扫描:
检测方式:多反应监测(MRM);d)其他参考质谱条件参见附录A,6.3.3液相色谱-质谱/质谱测定
6.3.3.1定性测定
SN/T 2218—2008
每种被测纽分逆择1个呼离子,2个以上子离子.在朴同实验条件下.样品中待测物质的保留时间,与基质标港溶液的保留时间偏关在二5实之内;样品中各组分定性离十的对十度马液度接近的基质混合标准作溶液中对虚的定证离子的相对丰度进行比较-偏关不超过衣2规定的范围.则可判定为样品中存在对应的待测物
表 2定性确证时相对离子丰度的最大允许偏差相对离子丰度:\
允许的最大差/兴
6.3.3.2定量测定
> [0.-- 20
在议器最代1作条件下,对基质混合标准工作溶液进群,以峰面为纵坐标基质混合目作溶液涨度为横坐标绘制标准作也线,用标准!作曲线对样品进行定量,推品溶液中待测物的响应值均应在仪器测定的线性范围内:林可酰胺类药物标准品的多反应监测色谱图参见附录13中的图.1。6.3.4空白试验
除不加标样外,按上述测定步骤进行7 结果计算与表述
按式(I)计算林可霉素、此利霉素、克林藓索残留最,计算结果需扣除空白值。10n
式中:
-试中被测组分残留量,位微克每下克(/kg):从标准工作曲线得到的被测组分溶液浓度,单位为微克每升(/.):样品溶液最终定容体积.单位为毫升(mL):-
样品搭液所代表最终试样的质量,单位为克(g)(1)
SN/T2218—2008
8方法的测定低限与回收率
测定低限
本方法的测定低限均为0.01mg/kg8.2回收率
猪肉、鸡肉、猪肝、牛肝、鸡蛋、牛奶中林可霉素、吡利霉素,克林霉素不同添加水平的回收率数据见表3。
添加水平!
(mg/kg)
林可霉素、吡利霉素、克林霉素不同添加水平的回收率数据化合物名称
林可霉素
吡利霉素
克林素
林可霉素
吡利葡素
克林霉素
林可霉素
吡利霉素
克林霉素
92.7~~103
78.5--104
回收率/%(n—10)
940-113
87/6-112
104e-111
79.2--92.6
5,6~94,4
84.8~96.3
100~110bzxZ.net
76.2--93.4
77.0~89.4
73.4~91.0
70.2~85.8
73,6--89.4
72.9-83,0
80.3~-89.1
65.6--75.9
68.4-~81.3
68.5-82.5
参考质谱条件:
电喷雾电压:3000V
辅助气流速:700L/h;
碰撞气:氩气:
幕帘气流速:50L/h;
离子源温度:105℃
辅助气温度:350℃;
附录A
(资料性附录)
参考质谱条件!
对采集时间、碰撞能量及锥孔电压见表A.1。定性离子对、定量离子对
化合物名称
林可霉素
毗利霉素
克林霉素
定性离子对(m/2)
407/126
4077359
411/112
411/363
425/126
425/378
酰腰类药物测定的质谱参数
定量离子对(
1O7/126
411/112
425/126
采集进间/s
SN/T2218—2008
碰撞气能量/eV
差异,测定前应将质谱参效优化到最住。注:对于不同质谱仪器,仪器参数可能存在锥孔电压/V
非商业性声明:附录A所列参考质谱条件是在WatersQuattroPremier型液质联用仪上完成的,此处列出试验用仪器型号仅为提供参考,并不涉及商业目的.鼓励标准使用者尝试不同厂家或型号的仪器。5
SN/T 2218—2008
407>126
附录H
(资料性附录)
林可酰胺类药物标准的多反应监测色谱图100
Trtimin
a)林霉素
411>363
cl)吡利霉素
407>359
b)林可霉素
+ timin
425>126
-q- tmin
e)克霉素
411>112
c)吡利蒂索
425>78
f)克林素
图 B.110.0 Hg/L林可霉素、吡利霉素和克林霉素标准溶液的多反应监测色谱图t:mm
Foreword
Annex A and B of this standard is an informative annexSN/T2218—2008
This standard was proposed by and is under the charge of the Certification and Accreditation Admin-istration of the People's Republic of China.The standard was drafted by Shenzhen Entry-Exit Inspection and Quarantine Bureau of the People'sRepublic of China, Guangdong Entry-Exit Inspection and Quarantine Bureau of the Peopie's Republicof China, Zhejiang Entry-Exit Inspection and Quarantine Bureau af the Pepple's Republic of China.The main drafters of this standard are Kang Haining. Xiao Feng, Shen Jincan, Lin Feng, Xie Wen,Xie Liqi, Han Ruiyang、Ge Liya.This standard is a professional standard for entry-exit inspection and quarantine promulgated for thefirst time.
Note: This English version, a translation from the Chinese text. ts solely for gcridance.SN/T 2218—2008
Determination of lincosamide residues in foodstuffs ofanimal origin for import and export-L.c-Ms/MS method1Scope
This standard specifies the rnetnods of sampling. cetermiration and corfirmation of lincosamide res-idues.which include lincornycin, pirlirriycin and clindarmyciri. by liquid chromatography tandem massspectrometry(Lc-MS. Ms) in foodstuffs of anirnal origin,This standard is applicable to the determination and confirmation of lincomycin. pirlimycin and clin-damycin in pork. chicken. purcine liver.bovine liver, egg, milk.2Abstract
The lincosamice residues in the test. sample are extracted with phosphate solution ( pH 8, 0), the ex-tract is further cleaneci up by passing through a Ci cartridge or equivalent. The eluate was then con.centratcd , redissolved and determined by Lc-Ms/Ms, using extemal standard method.3Reagents and materials
Unless utherwise specifiec. all reagents should be of analytical grade,\water is deionized water3.1Methanol:HFLC gracde
3.2Formic acid:HPLC grade.
3.3Sodium hydroxide
3.4 Sodiuin hydroxide solition (3 mcl .) : Weigin 120 gj sodium hydroxide i3. 3; and dissolve in800 mL water. then dilute to 1 000 rmil after coul.3. 5Potassitum dilhydroger phosphate3. 6 Phospinate solution (pH 8. 0): Weigh 6. 80 g potassiim dihydrogen phosphate (3. 51. dissolvein 800 mL water: adjust the pH to 8. 0 with sodlium hydroxidle solution (3. 4: anci make up to1 000 mL with water.
3.7 0. 1% formic ncicl solution: Accurately draw 1. 0 rnL formnic acid (3. 2.) into a 1 000 mL volu-metric flask.diute to volume with water. ainri mix to hornogeneity.SN/T2218-—2008
Sampledissolved solvent:Measure 10mLmethanoland90 mL0.1% formic acid (3.7),mix3.8
to homogeneity.
Lincosamidestandards:Lincomycin hydrochloride(C.Ha.N,O,S.HCl,CAsNo.:7179-49-9).3.9
puritymorethan99%;Pirlimycinhydrochloride(CizHa,CIN,O,S·HCl.CASNo.:79548-73-5),purityis86.4%:Clindamycinhydrochloride(C1aHa3CIN2O,SHCl.CASNo.:21462-39-5).purityis94.5%.3.10
Standard stock solutions:Accurately weighadequate lincosamide standard (3.9),whichisequivalentto1o mg lincomycin.pirlimycinand clindamycin,dissolve withmethanol(3.1)tomakea standard stock solution of 100 mg/L in concentration.The solution can bepreserved in thetemper-aturebelow-18fortwelvemonths.3.11
Intermediate standard mixture solution:Accurately draw 1,o mL lincosamide standard stocksolutions(3.10),dilutewithmethanol(3.1)tomediatestandard mixture solution ofmakeaninter
1.O mg/L in concentration. The solution can be preserved in the temperature below 4C for threemonth.
Matrix standard working solutions; According to the requrrement, accurately draw an ade-quate volume of lincosamideintermediate standardmixture solution(3.11),dilute withblank sampleextract solution and prepare a series of matrix standard working.solution of 5. rg/L,10.0 μg/L,20.0μg/L.50.0μg/L,100μg/L,200 μg/L.Thesolutionshouldbeprepared beforeuse.3.13
Ci cartridge:500 mg,6
equivalent. The column is activated with 5mLmethanol.or
beforeuse.Thecolumnshouldbekeptwetalways.5mLwaterand5mLphosphate solution4
Apparatusandequipmen
Liquid chromatography tandem mass spectrometry equipped with electrospray ion source.Analyticalbalance:sensitivity:o.1mg,oo1g.Volumetricflask,100mL1000mL
Polypropylenecentrifugetube:50mLor15mL,withscrewcup.Vortexmixer.
Centrifuge.
Solidphaseextraction.
SN/T 2218——2008
Vacumn pump.
Homogenizer.
Nitrogen evaporator
Membrane filter: 0. 22 μm.
5Samplepreparationandstorage5.1Animal muscle, liver,egg
Choose about 50o g representative sample and prepared it according to analysis requirement in lab.The prepared sample wotuld be devided into two part, and put into sample container, pressurize, anclabel. Sarmple should be kept at - 18 .5.2Milk
Choase about 50o g representative sample, devided into two part, and put into sample container.pressurize,and label.Sample should be kept at 4c.6
Procedure
6.1 Extraction
6.1.1Animalmuscle,liver
Accurately weigh 2 g of the test sample (accurate to 0. o1 g) in a 50 mL polypropylene centrifugetube,add 10 mL phosphate solution (3. 6) : blend for 2 min. centrifuge at 9 000 r/min for 5 min.Transfer the supernate into a 5o mL polypropylene centrifuge tube, Repeat the above extract proce-dure twice with 5 ml. phosphate sofution (3. 6), combine the supernates. mix and prepare for clean-up.
6.1.2 Egg, milk
Accurately weigh 5 g of the test sample (accurate to 0. 01 g) in a 50 mL polypropylene centrifugetube,add 20 mL phosphate solution (3, 6), blend for 2 min. Measure 10 ml blended sample salutioninto a 15 mL polypropylene centrifuge tutbe. centrifuge at 9 000 r/min for 5 min, transfer the super-nate. prepare for cleanup.
6.2 Cleanup
Accurately measure 5 mL extract (6. 1) onto the activated C-s cartridge (3. 13) and keep the flow10
小提示:此标准内容仅展示完整标准里的部分截取内容,若需要完整标准请到上方自行免费下载完整标准文档。
标准图片预览:




- 热门标准
- 商检行业标准(SN)
- SN/T2051-2008 食品、化妆品和饲料中牛羊猪源性成分检测方法实时PCR法
- SN/T3203-2012 进出口危险化学品检验规程爆炸品基本要求
- SN/T4341-2015 黑颜果实蝇检疫鉴定方法
- SN/T4115-2015 天然气中硫化物的分析方法气相色谱硫化学发光检测器法
- SN/T0239-93 出口钳形表检验规程
- SN/T5138-2019 棉花黄萎病菌检疫鉴定方法
- SN/T0801.6-1999 进出口动植物油脂沉积物检验方法
- SN/T2389.10-2012 进出口商品容器计重规程第10部分:液体化工品船舱静态计重
- SN/T3676-2013 甘蔗凋萎病菌检疫鉴定方法
- SN0158-92 出口水果中螨完锡残留量检验方法
- SN/T3656.2-2013 进出口危险化学品测试技术规范第2部分:气体
- SN/T4877.7-2017 基因条形码筛查方法 第7部分:检疫性轮枝菌
- SN/T3591-2013 实验室标准物质管理指南
- SN/T2925-2011 软体家具耐点燃性试验方法及评价
- SN/T2173-2008 危险品易燃固体自热试验试验方法
- 行业新闻
请牢记:“bzxz.net”即是“标准下载”四个汉字汉语拼音首字母与国际顶级域名“.net”的组合。 ©2025 标准下载网 www.bzxz.net 本站邮件:bzxznet@163.com
网站备案号:湘ICP备2025141790号-2
网站备案号:湘ICP备2025141790号-2