- 您的位置:
- 标准下载网 >>
- 标准分类 >>
- 医药行业标准(YY) >>
- YY/T 91141-1999 骨科凿类通用技术条件
标准号:
YY/T 91141-1999
标准名称:
骨科凿类通用技术条件
标准类别:
医药行业标准(YY)
标准状态:
现行出版语种:
简体中文下载格式:
.zip .pdf下载大小:
2.48 MB
点击下载
标准简介:
YY/T 91141-1999.
抽取双倍数量进行检验,若仍不符合本标准要求时,该批产品应全部退回,重新分类整理。
3.5经分类整理后, 可再提交检验。 复验时,按3.2条的规定抽取双倍数量进行检验,若不符合3.4条规定时,该批产品不予验收。
3.6在验收过程中, 双方对产品质量是否合格产生争论时,可由有关单位进行仲裁。
4标志、包装、运输、贮存
4.1 每把骨凿应按WS2-2-74《手术器械标志》的规定有下列标志:
a.制造厂 代号或商标
b.出厂 “年代(最后两字) ;
4Cr 13不锈钢骨凿应有材料标志“Cr”,9 C r18MoV不锈钢骨凿应有材料标志“MoV”。每把骨凿经防锈处理后,装入中性塑料袋,袋内应有检验合格证,并须密封。
4.2.1 检验合格证上应有下列标志:
a.制造厂名称;
b.检验员代号。
4.3
同一型号和规格应装人一盒内,盒上应有下列标志:制造厂名称和商标;
b. 产品名称;
c.规格;
d." 数量;
e. 标准号。
4.4 盒上应贴有封签,封签上应有下列标志:
a.'封贴日 期;
b. 包装员代号。
4.5装箱和运输 要求按订货合同规定。
4.6包装后的骨凿, 应贮存在相对湿度不超过80%、无腐蚀性气体和通风良好的室内。
部分标准内容:
YYT9L4L-99
骨科凿类通用技术条件
1983-07-23发布
国家医药管理局批准
1984-05-01实施
中华人民共和国卫生部部标准
骨科凿类通用技术条件
本标准适用于骨科器械中平骨凿(单斜面、双斜面)和圆骨凿产品。1技术要求
WS2—302-—83
骨凿的型式和基本尺寸应符合产品标准中的规定。1.1
骨凿应以GB1220-75《不锈耐酸钢技术条件》中规定的4Cr13和9Cr18MoV材料制成。1.2
骨凿应经热处理,其硬度应符合表1的规定。表1
头部20毫米内
产品部位
HRC5055
9Cr18MoV
HRC53~58
HRC35(不低于)
1.4骨凿柄部需滚花的应符合JB2一59《滚花》的规定,柄花应清晰完整,无缺花、烂花。柄部可为无光亮。
1.5骨凿外形应平整、对称。除刃口外,应无锋棱、毛刺、裂纹。1.6骨凿的刃口应有良好的凿切性能,凿切力的大小应按相应产品标准中的规定,凿切后不允许有卷刃、崩刃。
骨凿刃口角度25~35。
骨凿的光洁度应不低于表2的规定。表2
有光亮
无光亮
(圆柄除外)
1.9骨凿应有良好的耐腐蚀性能。部
凿切刃面
骨凿经包装后,在遵守贮存规则的条件下,应保证在一年半内不生锈。1.10
2试验方法
2.1外观
2.1.1以目力观察。
国家医药管理局1983-07-23发布其
1984-05-01实施
WS2-302—83
2.1.2光洁度按WS2/Z—7—65《表面光洁度检验方法样块比较法》检验。2.2尺寸
以通用或专用量具测量。
2.3性能
2.3.1硬度检验:按GB230一63《金属洛氏硬度试验法》测定。在头部20毫米内的平面上(或测试块上)各测三点,取其三点的算术平均值。2.3.2刃口凿切性能试验:根据相应的测试方法标准的要求,在专用骨凿刃口凿切性能测试仪上进行。
2.3.3耐腐蚀性试验:将去掉油脂的骨凿放到蒸馏水中清洗,清洗吹干后放人一装满蒸馏水的玻璃或防锈容器中煮沸30分钟,然后随蒸馅水自然冷却至室温,再从中取出骨凿放入密闭容器内,二小时后取出,用纱布措擦,以目力观察不应有锈迹。检验规则
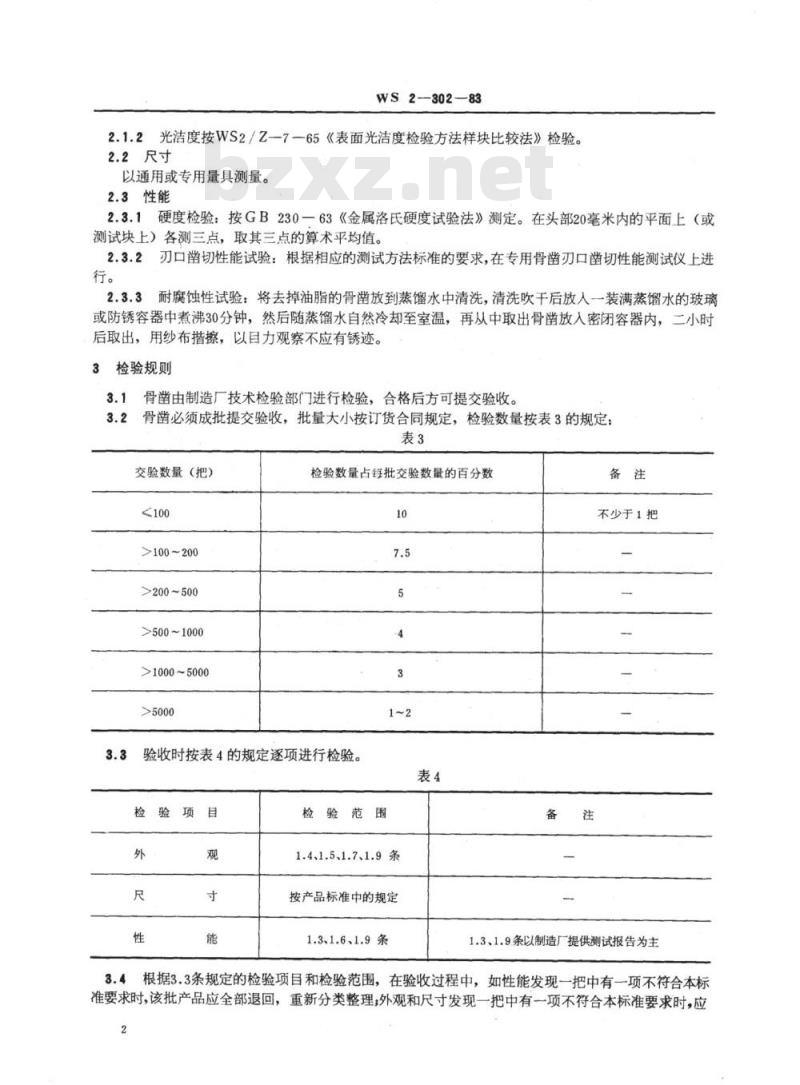
骨凿由制造厂技术检验部门进行检验,合格后方可提交验收。骨凿必须成批提交验收,批量大小按订货合同规定,检验数量按表3的规定:3.2
交验数量 (把)
>100~200
>200~500
>500~1000
>1000~5000
检验数量占每批交验数量的百分数10
验收时按表4的规定逐项进行检验表4下载标准就来标准下载网
检验范围
1.4、1.5、1.7、1.9条
按产品标准中的规定
1.3、1.6、1.9条
不少于1把
1.3、1.9条以制造厂提供测试报告为主根据3.3条规定的检验项目和检验范围,在验收过程中,如性能发现一把中有一项不符合本标3.4
准要求时,该批产品应全部退回,重新分类整理,外观和尺寸发现一把中有一项不符合本标准要求时,应2
WS2-302-83
抽取双倍数量进行检验,若仍不符合本标准要求时,该批产品应全部退回,重新分类整理。3.5经分类整理后,可再提交检验。复验时,按3.2条的规定抽取双倍数量进行检验,若不符合3.4条规定时,该批产品不予验收。3.6在验收过程中,双方对产品质量是否合格产生争论时,可由有关单位进行仲裁。4标志、包装、运输、贮存
每把骨凿应按WS2一2一74《手术器械标志》的规定有下列标志:a.
制造厂代号或商标;
出厂年代(最后两字);
4Cr13不锈钢骨凿应有材料标志“Cr”;9Cr18MoV不锈钢骨凿应有材料标志“MoV”。c.
每把骨凿经防锈处理后,装人中性塑料袋,袋内应有检验合格证,并须密封。4.2
检验合格证上应有下列标志:
制造厂名称;
检验员代号。
同一型号和规格应装人一盒内,盒上应有下列标志:制造厂名称和商标;
产品名称;
规格,
数量;
标准号。
盒上应贴有封签,封签上应有下列标志:封贴日期;
包装员代号。
装箱和运输要求按订货合同规定。包装后的骨凿,应贮存在相对湿度不超过80%、无腐蚀性气体和通风良好的室内。附加说明:
本标准由国家医药管理局提出,由上海医疗器械研究所归口。本标准由天津市医疗器械研究所负责起草。本标准主要起草人武光新、项兰生。9
中华人民共和国卫生部
部标准
骨科凿类通用技术条件
WS2—302—83
中国标准出版社出版
(北京复外三里河)
中国标准出版社秦皇岛印刷厂印刷新华书店北京发行所发行各地新华书店经售开本880×12301/16印张1/2
2字数6.000
1984年6月第一版1984年6月第一次印刷印数1-3,000
书号:15169·2-5392
定价0.20元
标目3—79
小提示:此标准内容仅展示完整标准里的部分截取内容,若需要完整标准请到上方自行免费下载完整标准文档。
标准图片预览:




- 其它标准
- 热门标准
- YY医药标准
- YY/T1523-2017 二氧化碳测定试剂盒(PEPC酶法)
- YY/T0735.1-2009 ISO 9360-1 :2000 麻醉和呼吸设备湿化人体呼吸气体.的热湿交换器(HME) 第1部分:用于最小潮气量为250 mL的HME
- YY/T0652-2008 ISO 17853 :2003 植入物材料的磨损聚合物和金属材料磨屑分离、表征和定量分析方法
- YY/T1636-2018 组织工程医疗器械产品再生膝关节软骨的体内磁共振评价方法
- YY0762-2009 眼科光学囊袋张力环
- YY0004-1990 普通胸腔镊
- YY/T0211-1995 药用中间体 青霉素钾
- YY/T1574-2017 组织工程医疗器械产品海藻酸盐凝胶固定或微囊化指南
- YY/T0703-2008 IEC 61390: 1996 超声实时脉冲回波系统性能试验方法
- YY0476-2004 眼内冲洗灌注液
- YY/T0663-2008 无源外科植入物 心脏和血管植入物的特殊要求 动脉支架的专用要求
- YY0781-2010 血压传感器
- YY/T0916.1-2014 医用液体和气体用小孔径连接件 第1部分:通用要求
- YY/T1268-2015 环氧乙烷灭菌的产品追加和过程等效
- YY0286.6-2009 专用输液器 第6部分:-次性使用流量设定微调式输液器
- 行业新闻
网站备案号:湘ICP备2025141790号-2