- 您的位置:
- 标准下载网 >>
- 标准分类 >>
- 医药行业标准(YY) >>
- YY 0079.1-1992 银夹
标准号:
YY 0079.1-1992
标准名称:
银夹
标准类别:
医药行业标准(YY)
标准状态:
已作废-
实施日期:
1992-07-01 -
作废日期:
2007-05-01 出版语种:
简体中文下载格式:
.rar.pdf下载大小:
55.32 KB
中标分类号:
医药、卫生、劳动保护>>医疗器械>>C36其他专科器械
部分标准内容:
中华人民共和国医药行业标准
主题内容与适用范围
YY0079.1-92
代替WS2-196-75
本标准规定了银夹的产品分类、技术要求、试验方法、检验规则、标志、包装、运输、贮存的要求。本标准适用于银夹,该产品供脑部手术时卖持小血管,作止血用。引用标准
GB191·包装储运图示标志
GB2828逐批检查计数抽样程序及抽样表(适用于连续批的检查)GB4342金属显微维氏硬度试验方法3产品分类
银夹的型式和基本尺寸应符合下列图样的规定。4技术要求
4.1银夹应符合本标准的要求,并按规定程序所批准的图样及文件制造。4.2银夹应以含银量不低于99.9%的纯银制成。4.3银夹表面可经钝化处理,表面粗糙度参数R,最大值为0.80μm。4.4银夹的外形应平整,不允许有毛刺、裂纹、斑疤和锋边等缺陷。4.5银夹内侧而应有横纹,横纹应清晰,完整,但不应有溢角或锋棱存在4.6银夹的硬度应为60~100HV。1。4.7银夹合拢后应平齐,两片长短之差不得超过允差总和的二分之试验方法
表面粗糙度按样块比较法比对或电测法进行。5.1
国家医药管理局1992-01-20批准1992-07-01实施
YY 0079.1—92
5.2硬度试验:按GB4342的规定,测三点,取其三点的算术平均值。6检验规则此内容来自标准下载网
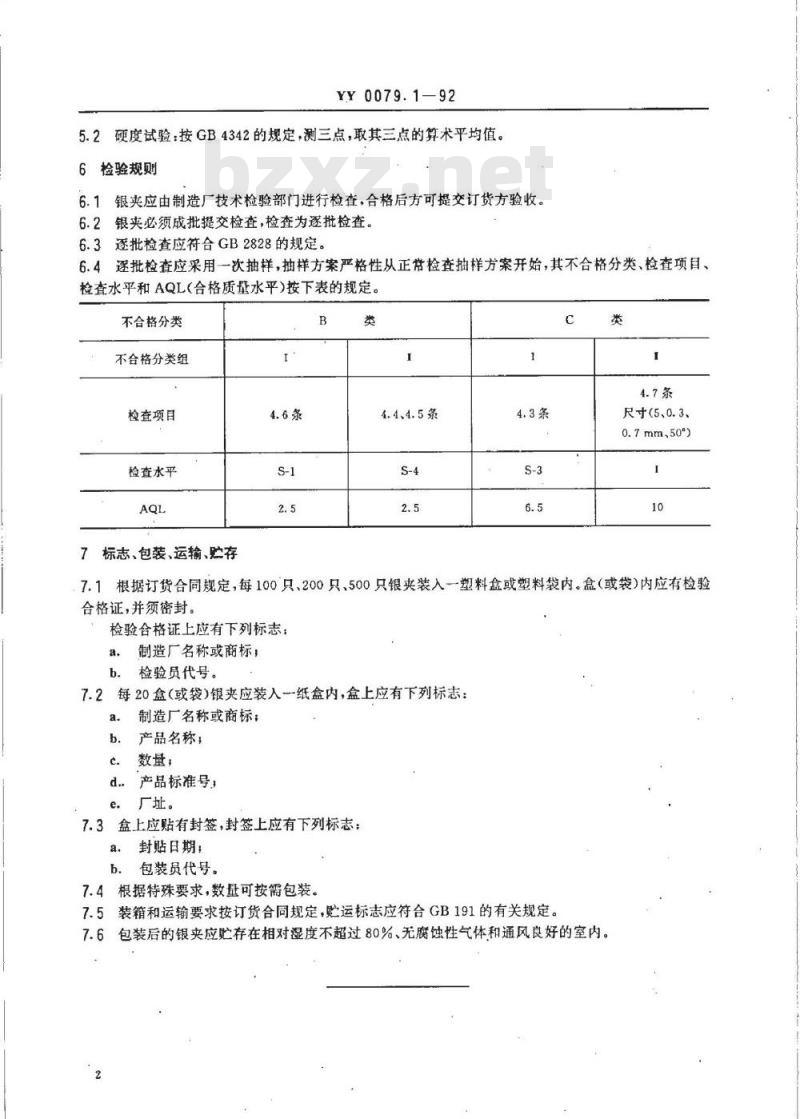
6.1银夹应由制造厂技术检验部门进行检查,合格后方可提交订货方验收,6.2银夹必须成批提交检查,检查为逐批检查。6.3逐批检查应符合GB2828的规定。6.4逐批检查应采用一次抽样,抽样方案严格性从正常检查抽样方案开始,其不合格分类、检查项目、检查水平和AQL(合格质量水平)按下表的规定。不合格分类
不合格分类组
检查项目
检查水平
标志、包装、运输、踪存
4.4、4.5条
尺寸(5、0.3、
0.7mm,50*)
7.1根据订货合同规定,每100只、200只,500只银夹装入一塑料盒或塑料袋内。盒(或袋)内应有检验合格证,并须密封。
检验合格证上应有下列标志:
制造厂名称或商标;
检验员代号。
7.2每20盒(或袋)银夹应装入-纸盒内,盒上应有下列标志:a.
制造厂名称或商标;
产品名称;
数量;
d.产品标准号
e:厂址。
7.3盒上应贴有封签,封签上应有下列标志:封贴日期:
包装员代号。
7.4根据特殊要求,数量可按需包装。7.5装箱和运输要求按订货合同规定,贮运标志应符合GB191的有关规定。7.6包装后的银夹应贮存在相对湿度不超过80%、无腐蚀性气体和通风良好的室内。附加说明:
YY0079.1-92
本标准由全国外科器械标准化技术委员会提出。本标准由全国外科器械标准化技术委员会归口。本标准由中国上海医疗器械检测中心负责起草。本标准主要起草人姚映红、傅国宝。
小提示:此标准内容仅展示完整标准里的部分截取内容,若需要完整标准请到上方自行免费下载完整标准文档。
主题内容与适用范围
YY0079.1-92
代替WS2-196-75
本标准规定了银夹的产品分类、技术要求、试验方法、检验规则、标志、包装、运输、贮存的要求。本标准适用于银夹,该产品供脑部手术时卖持小血管,作止血用。引用标准
GB191·包装储运图示标志
GB2828逐批检查计数抽样程序及抽样表(适用于连续批的检查)GB4342金属显微维氏硬度试验方法3产品分类
银夹的型式和基本尺寸应符合下列图样的规定。4技术要求
4.1银夹应符合本标准的要求,并按规定程序所批准的图样及文件制造。4.2银夹应以含银量不低于99.9%的纯银制成。4.3银夹表面可经钝化处理,表面粗糙度参数R,最大值为0.80μm。4.4银夹的外形应平整,不允许有毛刺、裂纹、斑疤和锋边等缺陷。4.5银夹内侧而应有横纹,横纹应清晰,完整,但不应有溢角或锋棱存在4.6银夹的硬度应为60~100HV。1。4.7银夹合拢后应平齐,两片长短之差不得超过允差总和的二分之试验方法
表面粗糙度按样块比较法比对或电测法进行。5.1
国家医药管理局1992-01-20批准1992-07-01实施
YY 0079.1—92
5.2硬度试验:按GB4342的规定,测三点,取其三点的算术平均值。6检验规则此内容来自标准下载网
6.1银夹应由制造厂技术检验部门进行检查,合格后方可提交订货方验收,6.2银夹必须成批提交检查,检查为逐批检查。6.3逐批检查应符合GB2828的规定。6.4逐批检查应采用一次抽样,抽样方案严格性从正常检查抽样方案开始,其不合格分类、检查项目、检查水平和AQL(合格质量水平)按下表的规定。不合格分类
不合格分类组
检查项目
检查水平
标志、包装、运输、踪存
4.4、4.5条
尺寸(5、0.3、
0.7mm,50*)
7.1根据订货合同规定,每100只、200只,500只银夹装入一塑料盒或塑料袋内。盒(或袋)内应有检验合格证,并须密封。
检验合格证上应有下列标志:
制造厂名称或商标;
检验员代号。
7.2每20盒(或袋)银夹应装入-纸盒内,盒上应有下列标志:a.
制造厂名称或商标;
产品名称;
数量;
d.产品标准号
e:厂址。
7.3盒上应贴有封签,封签上应有下列标志:封贴日期:
包装员代号。
7.4根据特殊要求,数量可按需包装。7.5装箱和运输要求按订货合同规定,贮运标志应符合GB191的有关规定。7.6包装后的银夹应贮存在相对湿度不超过80%、无腐蚀性气体和通风良好的室内。附加说明:
YY0079.1-92
本标准由全国外科器械标准化技术委员会提出。本标准由全国外科器械标准化技术委员会归口。本标准由中国上海医疗器械检测中心负责起草。本标准主要起草人姚映红、傅国宝。
小提示:此标准内容仅展示完整标准里的部分截取内容,若需要完整标准请到上方自行免费下载完整标准文档。
标准图片预览:


- 其它标准
- 上一篇: YY 0078-1992 气管异物钳通用技术条件
- 下一篇: YY 0079.2-1992 银夹台
- 热门标准
- 医药行业标准(YY)
- YY/T1523-2017 二氧化碳测定试剂盒(PEPC酶法)
- YY/T0735.1-2009 ISO 9360-1 :2000 麻醉和呼吸设备湿化人体呼吸气体.的热湿交换器(HME) 第1部分:用于最小潮气量为250 mL的HME
- YY/T0652-2008 ISO 17853 :2003 植入物材料的磨损聚合物和金属材料磨屑分离、表征和定量分析方法
- YY/T1636-2018 组织工程医疗器械产品再生膝关节软骨的体内磁共振评价方法
- YY0762-2009 眼科光学囊袋张力环
- YY0004-1990 普通胸腔镊
- YY/T0703-2008 IEC 61390: 1996 超声实时脉冲回波系统性能试验方法
- YY/T0211-1995 药用中间体 青霉素钾
- YY/T1574-2017 组织工程医疗器械产品海藻酸盐凝胶固定或微囊化指南
- YY0476-2004 眼内冲洗灌注液
- YY/T0663-2008 无源外科植入物 心脏和血管植入物的特殊要求 动脉支架的专用要求
- YY0781-2010 血压传感器
- YY/T0916.1-2014 医用液体和气体用小孔径连接件 第1部分:通用要求
- YY/T1268-2015 环氧乙烷灭菌的产品追加和过程等效
- YY/T1533-2017 全自动时间分辨荧光免疫分析仪
- 行业新闻
请牢记:“bzxz.net”即是“标准下载”四个汉字汉语拼音首字母与国际顶级域名“.net”的组合。 ©2025 标准下载网 www.bzxz.net 本站邮件:bzxznet@163.com
网站备案号:湘ICP备2025141790号-2
网站备案号:湘ICP备2025141790号-2