- 您的位置:
- 标准下载网 >>
- 标准分类 >>
- 农业行业标准(NY) >>
- NY/T 555-2002 动物产品中大肠菌群、粪大肠菌群和大肠杆菌的检测方法
标准号:
NY/T 555-2002
标准名称:
动物产品中大肠菌群、粪大肠菌群和大肠杆菌的检测方法
标准类别:
农业行业标准(NY)
标准状态:
现行-
发布日期:
2002-08-27 -
实施日期:
2002-12-01 出版语种:
简体中文下载格式:
.rar.pdf下载大小:
228.28 KB
点击下载
标准简介:
标准下载解压密码:www.bzxz.net
本标准规定了动物产品中大肠菌群、粪大肠菌群和大肠杆菌的检测方法。本标准适用于动物产品中大肠菌群、粪大肠菌群和大肠杆菌的检测。 NY/T 555-2002 动物产品中大肠菌群、粪大肠菌群和大肠杆菌的检测方法 NY/T555-2002
部分标准内容:
ICS11.220
中华人民共和国农业行业标准
NY/T555—2002
动物产品中大肠菌群、粪大肠菌群和大肠杆菌的检测方法
Detection methods for coliform group,faecal coliform group coliform bacteria in animal products2002-08-27发布
2002-12-01实施
中华人民共和国农业部
NY/T 555--2002
大肠菌群、粪大肠菌群和大肠杆菌是食品卫生的三项重要的卫生指标。当前国际上采用的方法有美国公职分析化学家协会(AOAC)方法及日本人介绍的煌绿乳糖胆盐肉汤(BGLB)和EC试管发酵法。为满足要求,依照日本采用的BGI.B和EC试管发酵法并进行适当改进,建立了本检测方法。本方法用BGLB发酵管检测大肠菌群并计算最大可能数(MPN)值,用EC肉汤发酵管检测粪大肠菌群并计算MPN值,在检测粪大肠菌群的基础上通过生化鉴定检测大肠杆菌并计算MPN值,鉴定中省去了革兰氏染色。这些重要改进缩短了检验时间,简化了操作程序,而且经对比试验证明结果可靠,适合于动物产品中大肠菌群、粪大肠菌群和大肠杆菌的检测。本标准的附录A是规范性附录,附录B是资料性附录。本标准由农业部畜牧兽医局提出。本标准由全国动物检疫标准化技术委员会归口。本标准起草单位:天津动植物检疫局。本标准主要起草人:秦贞奎、张碧波、侯艳梅、杨金良、薛振源。432
1范围
动物产品中大肠菌群、粪大肠菌群和大肠杆菌的检测方法
本标准规定了动物产品中大肠菌群、粪大肠菌群和大肠杆菌的检测方法。本标准适用于动物产品中大肠菌群、粪大肠菌群和大肠杆菌的检测。2术语和定义
下列术语和定义适用于本标准
大肠菌群coliforms;coliform gronp一群能分解乳糖产酸产气、需氧和兼性厌氧的革兰氏阴性无芽胞杆菌。2.2
龚大肠菌群 faecal coliforms ;faecal coliforms gronp44.5C发酵乳糖产气的一群细菌,是用来表示来源于粪便的大肠菌群。2.3
大肠杆菌escherichia coli;coliform bacteriaNY/T555-—2002
符合大肠菌群和粪大肠菌群定义,用IMViC(靛基质、甲基红、维培和西蒙氏柠檬酸盐)生化试验进步鉴定,四种生化反应结果依次为十→和一十一一的细菌。2.4
最大可能数most probable number,MPN采用多次稀释方法所求得的最近似数,是通过概率计算出来的。2.5IMViC
靛基质试验、甲基红试验、维培(VP)试验和构橼酸盐利用试验的缩写。3检测方法
3.1材料准备
3.1.1仪器
吸管,恒温水浴箱,培养箱,匀浆器,100ml、200mL和500mL三角瓶及广口瓶,直径5mm的玻璃珠。
3.1.2培养基及试剂
配制方法见附录A(规范性附录)。3.1.2.1煌绿乳糖胆盐肉汤(BGLB),配制方法见第A.1章。3.1.2.2EC肉汤,配制方法见第A.2章。3.1.2.3伊红美蓝琼脂(EMB),配制方法见第A.3章。3.1.2.4甲基红-维培(MR-VP)培养基,配制方法见第A.4章。3.1.2.5西蒙氏柠檬酸盐培养基,配制方法见第A.5章。433
NY/T 555—2002
3.1.2.6靛基质(吲哚)试验培养基,配制方法见第A.6章。3.1.2.7科瓦克(Kovacs)氏靛基质试剂,配制方法见第A.7章。3.1.2.8甲基红指示剂,配制方法见第A.8章。3.1.2.9维培(VP)试剂,配制方法见第A.9章。3.2检测程序
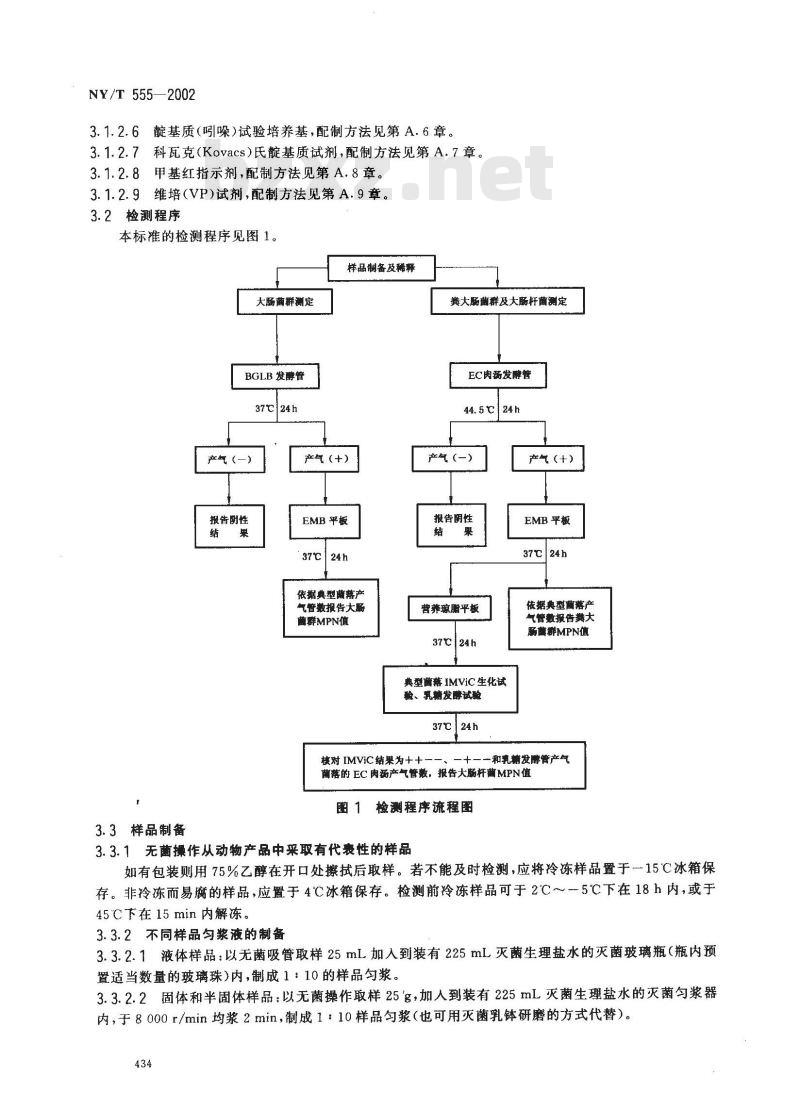
本标准的检测程序见图1。
样品制备及稀释
大肠蘭群测定
BGLB发醇管
37c24h
产气(-)
报告阴性
3.3样品制备
产气(+)
EMB平板
依据典型菌落产
气督数报告大肠
蘑群MPN值
粪大肠菌群及大肠杆菌测定
EC肉汤发醇管
产气(-)
报告阴性
营养琼脂平板
37℃|24h
典型菌蒋IMViC生化试
验、乳糖发醇试验
产气(+)
EMB平板
37℃24h
依据典型菌落产
气管数报告类大
肠菌群MPN值
和乳糖发醇管产气
核对 IMViC结果为++
葡落的 EC 肉产气管数。报告大肠杆菌MPN值图 检测程序流程图
3.3.1无菌操作从动物产品中采取有代衰性的样品如有包装则用75%乙醇在开口处擦拭后取样。若不能及时检测,应将冷冻样品置于一15℃冰箱保存。非冷冻而易腐的样品,应置于4℃冰箱保存。检测前冷冻样品可于 2℃~-5℃下在18h内,或于45℃下在15min内解冻。
3.3.2不同样品匀浆液的制备
3.3.2.1液体样品:以无菌吸管取样25mL加入到装有225mL灭菌生理盐水的灭菌玻璃瓶(瓶内预置适当数量的玻璃珠)内,制成1:10的样品匀浆。3.3.2.2固体和半固体样品:以无菌操作取样25'g,加人到装有225mL灭菌生理盐水的灭菌勾浆器内,于8000r/min均浆2min,制成1:10样品勾浆(也可用灭菌乳钵研磨的方式代替)。434
NY/T 555-2002
3.3.2.3样品稀释液的制备:根据样品污染情况,用灭菌生理盐水将样品勾浆制成一系列十倍递增的样品稀释液(通常采用10-1、10-2和10-3稀释)。从制备样品勾浆至稀释完毕,全过程不得超过15min。3.4大肠菌群的测定
3.4.1大肠菌群MPN值的測定
3.4.1.1每个样品通常选用10-1、10-2和10-3三个连续稀释度的样品稀释液,每个稀释度接种三管BGLB(见第A.1章),每管接种1mL,每接种-个稀释度换一支无菌吸管。3.4.1.2将接种管置于(36±1)℃培养24h。3.4.1.3观察试管的产气情况:检查管内是否有气泡产生,并记录24h内产气的BGLB管数。如所有培养管均未产气,则报告大肠菌群阴性;如有产气管,进一步试验证实。3.4.2大肠菌群的证实试验
3.4.2.1将所有产气管中的培养物用接种环接种到伊红美蓝琼脂平板,(36土1)℃培养24h。3.4.2.2大肠菌群在伊红美蓝琼脂平板上生长,其菌落为有金属光泽、黑紫色或紫色带黑心。3.4.2.3查有金属光泽、黑紫色或紫色带黑心菌落的BGLB产气管数及其稀释倍数。3.4.2.4结果报告:按3.4.2.3检查结果,查MPN检索表(见附录B),报告大肠菌群的MPN/g(mL)值。
3.5粪大肠菌群测定
3.5.1粪大肠菌群MPN值的测定
3.5.1.1每个样品通常选用10-1、10-2和10-3三个连续稀释度的样品稀释液,每个稀释度接种三管EC肉汤,每管接种1mL。
3.5.1.2将所有接种的EC肉汤管于30min内置于温度为(44.5土0.5)℃的带盖水浴箱内,培养(24土2)h。水浴箱的水面应高于肉汤培养基液面。用44.5℃产气阳性的大肠杆菌和44.5℃不产气的大肠杆菌或其他大肠菌群细菌作阳性和阴性对照。3.5.1.3记录EC管的产气情况。EC肉汤管都不产气为粪大肠菌群阴性,产气为粪大肠菌群阳性。将产气管作证实试验。
3.5.2证实试验
3.5.2.1将产气管接种伊红美蓝平板在(36土1)℃培养24h。3.5.2.2查有金属光泽、紫色带黑心菌落的EC产气管数及其稀释倍数。3.5.2.3结果报告:按3.5.2.2结果,查MPN检索表(见附录B)。报告粪大肠菌群的MPN/g(mL)值。3.6大肠杆蘭测定
3.6.1培养
将3.5.2.1中伊红美蓝平板上典型大肠杆菌菌落接种到营养琼脂平板,在(36土1)℃培养18h~24h。每个平板至少挑选2个菌落。3.6.2生化试验
挑取上述菌落纯培养物接种3.6.3生化培养基和乳糖发酵管,(36士1)℃培养24h后观察结果。3.6.3大肠杆菌与非大肠杆菌鉴别试验方法3.6.3.1靛基质试验:
a)滴加Kovacs氏靛基质试剂0.1mL于靛基质试验培养基中混合,静置,观察结果。b)出现红色环的为反应阳性;出现黄色环的为反应阴性。3.6.3.2甲基红(MR)试验:
a)滴加甲基红指示剂0.2mL于MR-VP培养基中混合,观察结果。b)出现红色为阳性反应;出现黄色为阴性反应。3.6.3.3维培(VP)试验:
a)滴加VP试剂甲液0.2mL于MR-VP培养基中混匀,再滴加VP试剂乙液0.1mL混匀,静435
NY/T 555—2002
置,观察结果。
b)在15min内出现红色的为阳性反应;无色变化的为阴性反应。阴性结果1h后再观察一次,出现红色也为阳性反应。
3.6.3.4西蒙氏柠檬酸盐试验:观察培养基颜色变化,出现蓝色为阳性反应;不变色为阴性反应。3.6.4大肠杆菌鉴定结果
应符合表1要求。
表1大肠杆菌鉴定结果
靛基质
西蒙氏柠檬酸盐
鉴定(型别)
典型大肠艾希氏杆菌
非典型大肠艾希氏杆菌
典型柠檬酸盐杆菌
非典型柠檬酸盐杆菌
典型产气肠杆菌
非典型产气肠杆菌
如出现表1以外的生化反应类型,表明培养物可能不纯,应重新划线分离,必要时做重复试验。3.6.5结果报告
IMViC试验结果为++
十一一和乳糖发酵管产气者,查其EC肉汤产气管数及其稀释倍数,对照附录B(资料性附录)中MPN检索表报告样品中大肠埃希氏杆菌MPN/g(mL)值。436
A.1煌绿乳糖胆盐肉汤(BGLB)
A.1.1成分
蛋白豚
牛胆盐
煌绿水溶液
蒸馏水
A.1.2配制方法
附录A
(规范性附录)
培养基和试剂配制方法
NY/T 555—2002
将蛋白陈、乳糖溶于约500mL蒸馏水中,加人牛胆盐后用蒸馏水稀释到970mL,调pH7.4。再加人0.1%煌绿水溶液13.3mL,用蒸馏水补足到1000mL。分装到20×150mm试管中(管内有倒立的小发酵管)。每管10mL。于112kPa灭菌15min,最终 pH(7.2±0.1)。A.2EC肉汤
A.2.1成分
胰蛋白陈或酪蛋白胰消化物
3号胆盐或混合胆盐
磷酸氢二钾(K,HPO,)
磷酸二氢钾(KH,PO,)
氯化钠
蒸馏水
A.2.2配制方法
1 000 mL
将以上成分溶解于蒸馏水中,分装16×150mm试管(试管内有倒立的小发酵管),每管8mL,于112kPa灭菌15min,最终pH(6.9士0.1)。A.3伊红美蓝琼脂(EMB)
A.3.1成分
蛋白陈
伊红Y
磷酸氢二钾
蒸馏水
0.4g(或2%水溶液20mL)
0.065g(或0.5%水溶液13mL)
1000mL
A.3.2配制方法
将蛋白陈、磷酸盐和琼脂加到1000mL蒸馏水中,并加热使其溶解。并分装于三角瓶中。每瓶100mL或200mL,75kPa灭菌15min,最终pH(7.1±0.2)。使用前将琼脂溶化,于每100mL琼脂中437
NY/T 555--2002
加5mL灭菌的20%乳糖水溶液,2mL的2%伊水溶液和1.3mL0.5%的美蓝水溶液,摇勾,冷至45~50℃后倾注平血。
A.4MR-VP培养基
A.4.1成分
葡萄糖
磷酸氢二钾
蒸馏水
A.4.2配制方法
1000 mL
将各成分溶解于蒸馏水中,分装试管中,于是112kPa灭菌15min,最终pH(6.9士0.2)。A.5西蒙氏柠檬酸盐培养基
A.5.1成分
氯化钠
硫酸镁(MgSO·7H20)
磷酸氢二铵
2%溴麝香草酚蓝溶液
磷酸氢二钾
柠檬酸钠
蒸馏水
A.5.2配制方法
1000mL
先将盐类溶解于水,调整pH6.8,再加琼脂,加温溶化后,加入指示剂,混合均匀后装入试管,112kPa灭菌15min,摆成斜面。
A.6 靛基质试验培养基
A.6.1成分
胰陈或胰酪陈
蒸馏水
A.6.2配制方法
1000mL
加热搅拌溶解胰陈或胰酪陈于蒸馏水中。分装试管,每管5mL。112kPa灭菌15min。最终pH(6. 9±0.2)。
A.7Kovacs氏靛基质试剂
A.7.1成分
对-二甲胺基苯甲醛
盐酸(浓)
A.7.2配制方法
将对-二甲胺基溶于戊醇中,然后慢慢加人浓盐酸即可。438
3甲基红指示剂
A.8.1成分
甲基红
95%乙醇
A.8.2配制方法
将甲基红溶解于300ml乙醇中,加水稀释500mL。A.9
Voges-Pros Kauer(V-P)试剂
A.9.1成分
A.9.1.1甲液
α-萘酚
无水乙醇
A.9.1.2乙液
氢氧化钾
蒸馏水
配制方法
A.9.2.1甲液:将α-萘酚溶解于无水乙醇中。2乙液:将氢氧化钾溶解于蒸馏水中。A.9.2.2
1 000 mL
1000 mL
NY/T555--2002
NY/T 555-2002
附录B
(资料性附录)
MPN检索表
表 B.1 MPN 检索表
95%可信限
阳性管数
[mL(g)]
0. 001 ml(g)×3
10. 01 mL(g)×3
0. 1 mL(g)X3
NY/T555—2002
表B.1(续)
95%可信限
阳性管数bzxZ.net
[mL(g)]
0.001mL(g)×3
0. 01 mL(g)×3
0. 1 ml.b(g)x3
≥2400
*本表采用三管法三个稀释度[0.1g(mL)、0.01g(mL)和0.001(mL)]每个稀释度接种三管。表内所列检样量如改用1g(mL)、0.1g(mL)和0.01g(mL)时。表内数字应相应降低10倍;如改用0.01g(ml.)、0.001g(mL)和0.0001g(mL)时,则表内数字应相应增加10倍,其余类推。441
小提示:此标准内容仅展示完整标准里的部分截取内容,若需要完整标准请到上方自行免费下载完整标准文档。
中华人民共和国农业行业标准
NY/T555—2002
动物产品中大肠菌群、粪大肠菌群和大肠杆菌的检测方法
Detection methods for coliform group,faecal coliform group coliform bacteria in animal products2002-08-27发布
2002-12-01实施
中华人民共和国农业部
NY/T 555--2002
大肠菌群、粪大肠菌群和大肠杆菌是食品卫生的三项重要的卫生指标。当前国际上采用的方法有美国公职分析化学家协会(AOAC)方法及日本人介绍的煌绿乳糖胆盐肉汤(BGLB)和EC试管发酵法。为满足要求,依照日本采用的BGI.B和EC试管发酵法并进行适当改进,建立了本检测方法。本方法用BGLB发酵管检测大肠菌群并计算最大可能数(MPN)值,用EC肉汤发酵管检测粪大肠菌群并计算MPN值,在检测粪大肠菌群的基础上通过生化鉴定检测大肠杆菌并计算MPN值,鉴定中省去了革兰氏染色。这些重要改进缩短了检验时间,简化了操作程序,而且经对比试验证明结果可靠,适合于动物产品中大肠菌群、粪大肠菌群和大肠杆菌的检测。本标准的附录A是规范性附录,附录B是资料性附录。本标准由农业部畜牧兽医局提出。本标准由全国动物检疫标准化技术委员会归口。本标准起草单位:天津动植物检疫局。本标准主要起草人:秦贞奎、张碧波、侯艳梅、杨金良、薛振源。432
1范围
动物产品中大肠菌群、粪大肠菌群和大肠杆菌的检测方法
本标准规定了动物产品中大肠菌群、粪大肠菌群和大肠杆菌的检测方法。本标准适用于动物产品中大肠菌群、粪大肠菌群和大肠杆菌的检测。2术语和定义
下列术语和定义适用于本标准
大肠菌群coliforms;coliform gronp一群能分解乳糖产酸产气、需氧和兼性厌氧的革兰氏阴性无芽胞杆菌。2.2
龚大肠菌群 faecal coliforms ;faecal coliforms gronp44.5C发酵乳糖产气的一群细菌,是用来表示来源于粪便的大肠菌群。2.3
大肠杆菌escherichia coli;coliform bacteriaNY/T555-—2002
符合大肠菌群和粪大肠菌群定义,用IMViC(靛基质、甲基红、维培和西蒙氏柠檬酸盐)生化试验进步鉴定,四种生化反应结果依次为十→和一十一一的细菌。2.4
最大可能数most probable number,MPN采用多次稀释方法所求得的最近似数,是通过概率计算出来的。2.5IMViC
靛基质试验、甲基红试验、维培(VP)试验和构橼酸盐利用试验的缩写。3检测方法
3.1材料准备
3.1.1仪器
吸管,恒温水浴箱,培养箱,匀浆器,100ml、200mL和500mL三角瓶及广口瓶,直径5mm的玻璃珠。
3.1.2培养基及试剂
配制方法见附录A(规范性附录)。3.1.2.1煌绿乳糖胆盐肉汤(BGLB),配制方法见第A.1章。3.1.2.2EC肉汤,配制方法见第A.2章。3.1.2.3伊红美蓝琼脂(EMB),配制方法见第A.3章。3.1.2.4甲基红-维培(MR-VP)培养基,配制方法见第A.4章。3.1.2.5西蒙氏柠檬酸盐培养基,配制方法见第A.5章。433
NY/T 555—2002
3.1.2.6靛基质(吲哚)试验培养基,配制方法见第A.6章。3.1.2.7科瓦克(Kovacs)氏靛基质试剂,配制方法见第A.7章。3.1.2.8甲基红指示剂,配制方法见第A.8章。3.1.2.9维培(VP)试剂,配制方法见第A.9章。3.2检测程序
本标准的检测程序见图1。
样品制备及稀释
大肠蘭群测定
BGLB发醇管
37c24h
产气(-)
报告阴性
3.3样品制备
产气(+)
EMB平板
依据典型菌落产
气督数报告大肠
蘑群MPN值
粪大肠菌群及大肠杆菌测定
EC肉汤发醇管
产气(-)
报告阴性
营养琼脂平板
37℃|24h
典型菌蒋IMViC生化试
验、乳糖发醇试验
产气(+)
EMB平板
37℃24h
依据典型菌落产
气管数报告类大
肠菌群MPN值
和乳糖发醇管产气
核对 IMViC结果为++
葡落的 EC 肉产气管数。报告大肠杆菌MPN值图 检测程序流程图
3.3.1无菌操作从动物产品中采取有代衰性的样品如有包装则用75%乙醇在开口处擦拭后取样。若不能及时检测,应将冷冻样品置于一15℃冰箱保存。非冷冻而易腐的样品,应置于4℃冰箱保存。检测前冷冻样品可于 2℃~-5℃下在18h内,或于45℃下在15min内解冻。
3.3.2不同样品匀浆液的制备
3.3.2.1液体样品:以无菌吸管取样25mL加入到装有225mL灭菌生理盐水的灭菌玻璃瓶(瓶内预置适当数量的玻璃珠)内,制成1:10的样品匀浆。3.3.2.2固体和半固体样品:以无菌操作取样25'g,加人到装有225mL灭菌生理盐水的灭菌勾浆器内,于8000r/min均浆2min,制成1:10样品勾浆(也可用灭菌乳钵研磨的方式代替)。434
NY/T 555-2002
3.3.2.3样品稀释液的制备:根据样品污染情况,用灭菌生理盐水将样品勾浆制成一系列十倍递增的样品稀释液(通常采用10-1、10-2和10-3稀释)。从制备样品勾浆至稀释完毕,全过程不得超过15min。3.4大肠菌群的测定
3.4.1大肠菌群MPN值的測定
3.4.1.1每个样品通常选用10-1、10-2和10-3三个连续稀释度的样品稀释液,每个稀释度接种三管BGLB(见第A.1章),每管接种1mL,每接种-个稀释度换一支无菌吸管。3.4.1.2将接种管置于(36±1)℃培养24h。3.4.1.3观察试管的产气情况:检查管内是否有气泡产生,并记录24h内产气的BGLB管数。如所有培养管均未产气,则报告大肠菌群阴性;如有产气管,进一步试验证实。3.4.2大肠菌群的证实试验
3.4.2.1将所有产气管中的培养物用接种环接种到伊红美蓝琼脂平板,(36土1)℃培养24h。3.4.2.2大肠菌群在伊红美蓝琼脂平板上生长,其菌落为有金属光泽、黑紫色或紫色带黑心。3.4.2.3查有金属光泽、黑紫色或紫色带黑心菌落的BGLB产气管数及其稀释倍数。3.4.2.4结果报告:按3.4.2.3检查结果,查MPN检索表(见附录B),报告大肠菌群的MPN/g(mL)值。
3.5粪大肠菌群测定
3.5.1粪大肠菌群MPN值的测定
3.5.1.1每个样品通常选用10-1、10-2和10-3三个连续稀释度的样品稀释液,每个稀释度接种三管EC肉汤,每管接种1mL。
3.5.1.2将所有接种的EC肉汤管于30min内置于温度为(44.5土0.5)℃的带盖水浴箱内,培养(24土2)h。水浴箱的水面应高于肉汤培养基液面。用44.5℃产气阳性的大肠杆菌和44.5℃不产气的大肠杆菌或其他大肠菌群细菌作阳性和阴性对照。3.5.1.3记录EC管的产气情况。EC肉汤管都不产气为粪大肠菌群阴性,产气为粪大肠菌群阳性。将产气管作证实试验。
3.5.2证实试验
3.5.2.1将产气管接种伊红美蓝平板在(36土1)℃培养24h。3.5.2.2查有金属光泽、紫色带黑心菌落的EC产气管数及其稀释倍数。3.5.2.3结果报告:按3.5.2.2结果,查MPN检索表(见附录B)。报告粪大肠菌群的MPN/g(mL)值。3.6大肠杆蘭测定
3.6.1培养
将3.5.2.1中伊红美蓝平板上典型大肠杆菌菌落接种到营养琼脂平板,在(36土1)℃培养18h~24h。每个平板至少挑选2个菌落。3.6.2生化试验
挑取上述菌落纯培养物接种3.6.3生化培养基和乳糖发酵管,(36士1)℃培养24h后观察结果。3.6.3大肠杆菌与非大肠杆菌鉴别试验方法3.6.3.1靛基质试验:
a)滴加Kovacs氏靛基质试剂0.1mL于靛基质试验培养基中混合,静置,观察结果。b)出现红色环的为反应阳性;出现黄色环的为反应阴性。3.6.3.2甲基红(MR)试验:
a)滴加甲基红指示剂0.2mL于MR-VP培养基中混合,观察结果。b)出现红色为阳性反应;出现黄色为阴性反应。3.6.3.3维培(VP)试验:
a)滴加VP试剂甲液0.2mL于MR-VP培养基中混匀,再滴加VP试剂乙液0.1mL混匀,静435
NY/T 555—2002
置,观察结果。
b)在15min内出现红色的为阳性反应;无色变化的为阴性反应。阴性结果1h后再观察一次,出现红色也为阳性反应。
3.6.3.4西蒙氏柠檬酸盐试验:观察培养基颜色变化,出现蓝色为阳性反应;不变色为阴性反应。3.6.4大肠杆菌鉴定结果
应符合表1要求。
表1大肠杆菌鉴定结果
靛基质
西蒙氏柠檬酸盐
鉴定(型别)
典型大肠艾希氏杆菌
非典型大肠艾希氏杆菌
典型柠檬酸盐杆菌
非典型柠檬酸盐杆菌
典型产气肠杆菌
非典型产气肠杆菌
如出现表1以外的生化反应类型,表明培养物可能不纯,应重新划线分离,必要时做重复试验。3.6.5结果报告
IMViC试验结果为++
十一一和乳糖发酵管产气者,查其EC肉汤产气管数及其稀释倍数,对照附录B(资料性附录)中MPN检索表报告样品中大肠埃希氏杆菌MPN/g(mL)值。436
A.1煌绿乳糖胆盐肉汤(BGLB)
A.1.1成分
蛋白豚
牛胆盐
煌绿水溶液
蒸馏水
A.1.2配制方法
附录A
(规范性附录)
培养基和试剂配制方法
NY/T 555—2002
将蛋白陈、乳糖溶于约500mL蒸馏水中,加人牛胆盐后用蒸馏水稀释到970mL,调pH7.4。再加人0.1%煌绿水溶液13.3mL,用蒸馏水补足到1000mL。分装到20×150mm试管中(管内有倒立的小发酵管)。每管10mL。于112kPa灭菌15min,最终 pH(7.2±0.1)。A.2EC肉汤
A.2.1成分
胰蛋白陈或酪蛋白胰消化物
3号胆盐或混合胆盐
磷酸氢二钾(K,HPO,)
磷酸二氢钾(KH,PO,)
氯化钠
蒸馏水
A.2.2配制方法
1 000 mL
将以上成分溶解于蒸馏水中,分装16×150mm试管(试管内有倒立的小发酵管),每管8mL,于112kPa灭菌15min,最终pH(6.9士0.1)。A.3伊红美蓝琼脂(EMB)
A.3.1成分
蛋白陈
伊红Y
磷酸氢二钾
蒸馏水
0.4g(或2%水溶液20mL)
0.065g(或0.5%水溶液13mL)
1000mL
A.3.2配制方法
将蛋白陈、磷酸盐和琼脂加到1000mL蒸馏水中,并加热使其溶解。并分装于三角瓶中。每瓶100mL或200mL,75kPa灭菌15min,最终pH(7.1±0.2)。使用前将琼脂溶化,于每100mL琼脂中437
NY/T 555--2002
加5mL灭菌的20%乳糖水溶液,2mL的2%伊水溶液和1.3mL0.5%的美蓝水溶液,摇勾,冷至45~50℃后倾注平血。
A.4MR-VP培养基
A.4.1成分
葡萄糖
磷酸氢二钾
蒸馏水
A.4.2配制方法
1000 mL
将各成分溶解于蒸馏水中,分装试管中,于是112kPa灭菌15min,最终pH(6.9士0.2)。A.5西蒙氏柠檬酸盐培养基
A.5.1成分
氯化钠
硫酸镁(MgSO·7H20)
磷酸氢二铵
2%溴麝香草酚蓝溶液
磷酸氢二钾
柠檬酸钠
蒸馏水
A.5.2配制方法
1000mL
先将盐类溶解于水,调整pH6.8,再加琼脂,加温溶化后,加入指示剂,混合均匀后装入试管,112kPa灭菌15min,摆成斜面。
A.6 靛基质试验培养基
A.6.1成分
胰陈或胰酪陈
蒸馏水
A.6.2配制方法
1000mL
加热搅拌溶解胰陈或胰酪陈于蒸馏水中。分装试管,每管5mL。112kPa灭菌15min。最终pH(6. 9±0.2)。
A.7Kovacs氏靛基质试剂
A.7.1成分
对-二甲胺基苯甲醛
盐酸(浓)
A.7.2配制方法
将对-二甲胺基溶于戊醇中,然后慢慢加人浓盐酸即可。438
3甲基红指示剂
A.8.1成分
甲基红
95%乙醇
A.8.2配制方法
将甲基红溶解于300ml乙醇中,加水稀释500mL。A.9
Voges-Pros Kauer(V-P)试剂
A.9.1成分
A.9.1.1甲液
α-萘酚
无水乙醇
A.9.1.2乙液
氢氧化钾
蒸馏水
配制方法
A.9.2.1甲液:将α-萘酚溶解于无水乙醇中。2乙液:将氢氧化钾溶解于蒸馏水中。A.9.2.2
1 000 mL
1000 mL
NY/T555--2002
NY/T 555-2002
附录B
(资料性附录)
MPN检索表
表 B.1 MPN 检索表
95%可信限
阳性管数
[mL(g)]
0. 001 ml(g)×3
10. 01 mL(g)×3
0. 1 mL(g)X3
NY/T555—2002
表B.1(续)
95%可信限
阳性管数bzxZ.net
[mL(g)]
0.001mL(g)×3
0. 01 mL(g)×3
0. 1 ml.b(g)x3
≥2400
*本表采用三管法三个稀释度[0.1g(mL)、0.01g(mL)和0.001(mL)]每个稀释度接种三管。表内所列检样量如改用1g(mL)、0.1g(mL)和0.01g(mL)时。表内数字应相应降低10倍;如改用0.01g(ml.)、0.001g(mL)和0.0001g(mL)时,则表内数字应相应增加10倍,其余类推。441
小提示:此标准内容仅展示完整标准里的部分截取内容,若需要完整标准请到上方自行免费下载完整标准文档。
标准图片预览:




- 其它标准
- 热门标准
- 农业行业标准(NY)
- NY/T456-2001 茉莉花茶
- NY/T889-2004 土壤速效钾和缓效钾含量的测定
- NY/T1153.4-2013 农药登记用白蚁防治剂药效试验方法及评价 第4部分农药木材处理预防白蚁
- NY/T598-2002 食用绿豆
- NY5086-2002 无公害食品 鲜食葡萄
- NY/T797-2004 硅肥
- NY/T1378-2007 土壤氯离子含量的测定
- NY/T1597-2008 动植物油脂 紫外吸光值的测定
- NY/T1858.2-2010 番茄主要病害抗病性鉴定技术规程 第2部分:番茄抗叶霉病鉴定技术规程
- NY/T423-2000 绿色食品 鲜梨
- NY5187-2002 无公害食品 罐装金针菇
- NY/T749-2003 绿色食品 食用菌
- NY/T680-2003 禽白血病病毒p27抗原酶联免疫吸附试验方法
- NY/T847-2004 水稻产地环境技术条件
- NY/T1364-2007 温室齿条开窗机
- 行业新闻
请牢记:“bzxz.net”即是“标准下载”四个汉字汉语拼音首字母与国际顶级域名“.net”的组合。 ©2025 标准下载网 www.bzxz.net 本站邮件:bzxznet@163.com
网站备案号:湘ICP备2025141790号-2
网站备案号:湘ICP备2025141790号-2