- 您的位置:
- 标准下载网 >>
- 标准分类 >>
- 国家标准(GB) >>
- GB 8276-1987 食品添加剂 糖化酶制剂
标准号:
GB 8276-1987
标准名称:
食品添加剂 糖化酶制剂
标准类别:
国家标准(GB)
标准状态:
已作废-
发布日期:
1987-10-19 -
实施日期:
1988-02-01 -
作废日期:
2007-05-01 出版语种:
简体中文下载格式:
.rar.pdf下载大小:
170.25 KB
手机扫码下载更方便
标准ICS号:
食品技术>>香料和调料、食品添加剂>>67.220.20食品添加剂中标分类号:
食品>>食品添加剂与食用香料>>X41天然食品添加剂
替代情况:
被GB 8276-2006代替
部分标准内容:
中华人民共和国国家标准
食品添加剂
糖化酶制剂
Food additive
Glucoamvlase preperation
UDC 661.733
8276—87
本标准适用于由发酵法生产,经提纯制取,供食品生产作添加剂用的糖化酶制剂。1技术要求
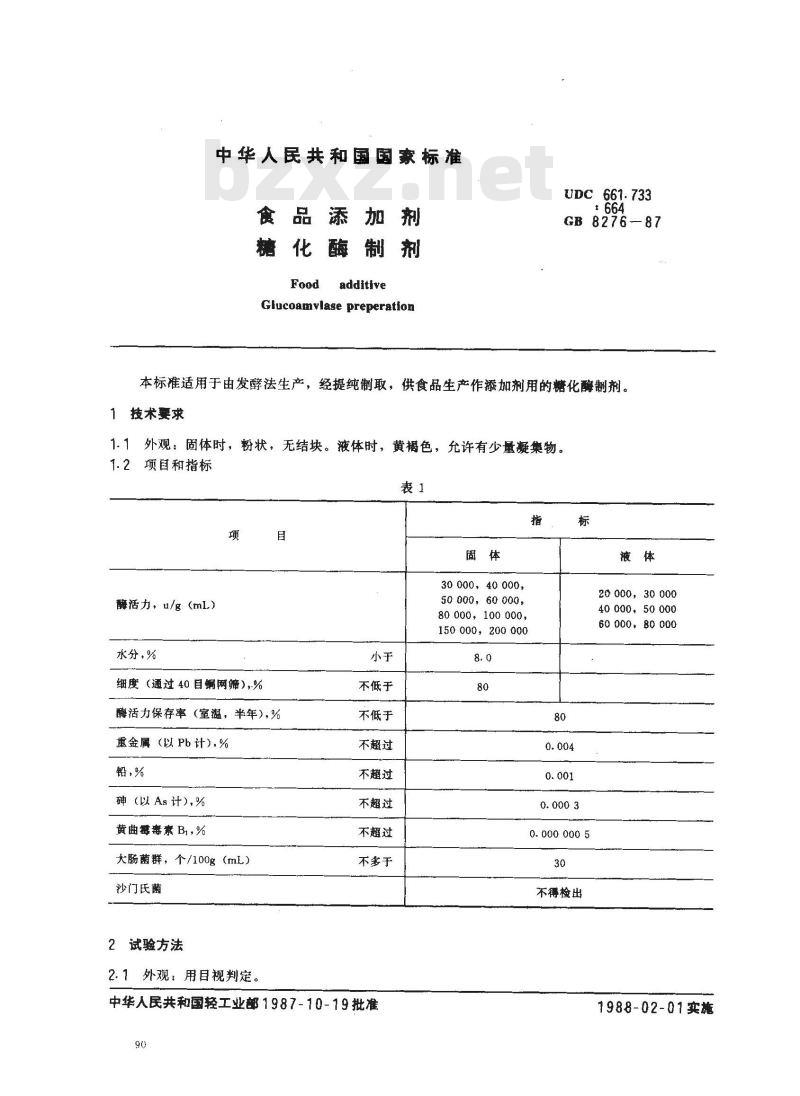
1.1外观:固体时,粉状,无结块。液体时,黄褐色,允许有少量凝集物。1.2 项目和指标
酶活力,u/g(mL)
水分,%
细度(通过 40 目铜网筛),%
酶活力保存率(室温,半年),%重金属(以Pb计),%
铅,%
砷(以As计),%
黄曲霉毒素 B1,%
大肠菌群,个/100g(mL)
沙门氏菌下载标准就来标准下载网
2试验方法
2.1外观:用目视判定。
不低于
不低于
不超过
不超过
不超过
不超过
不多于
中华人民共和国轻工业部1987-10-19批准90
30 000,40 000,
50 000, 60 000,
80 000, 100 000,
150 000, 200 000
20 000, 30 000
40 000,50 000
60 000, 80 000
0.000 000 5
不得检出
1988-02-01实施
2.2酶活力测定
2-2.1试剂
GB 8276--87
2.2.1.10.1N乙酸-乙酸钠缓冲溶液(pH4.6):称取6.7g乙酸钠(CH,COONa·3HzO),吸取冰乙酸2.6mL,用蒸馏水溶解定容至1000mL,上述缓冲溶液应以酸度计校正pH值。2.2.1.20.05N硫代碗酸钠溶液:按GB601《化学试剂标准溶液制备方法》中2.7执行。2.2.1.30.1N碘液:按GB601《化学试剂标准溶液备方法》中2.10执行。2.2.1.40.1N氢氧化钠溶液:按GB601《化学试剂标准溶液制备方法》中2.2执行。2.2.1.52N硫酸溶液:量取分析纯浓硫酸(比重1.84)5.6mL缓缓加入适量蒸馏水中,冷却后用蒸馏水定容至100mL,摇匀。
2.2.1.620%氢氧化钠溶液:称取20g分析纯氢氧化钠,用蒸馏水溶解定容至100mL。2.2.1.72%可溶性淀粉溶液:称取可溶性淀粉2.00g,然后用少量蒸馏水调匀,徐徐倾入已沸的蒸馏水中,煮沸至透明,冷却,用蒸馏水定容至100mL,此溶液需当天配制。注:可溶性淀粉应符合HG3—3095质量标准要求。2.2.2测定程序
2.2.2.1待测酶液的制备;称取酶粉2.0000g(或1.00mL酶液),倒入50mL烧杯中,用少量的乙酸~乙酸钠缓冲溶液(pH4.6)溶解,并用玻璃棒捣碎,将上层清液小心倾入适当的容量瓶中,沉渣再加入少量上述缓冲溶液。如此反复捣研3~4次,最后全部移入容量瓶中,用缓冲溶液定容至刻度,摇匀,用4层纱布过滤。再用滤纸滤清,滤液供测定用。浓缩酶液可直接吸取一定量于容量瓶中,用缓冲溶液稀释定容室刻度。
注:制备酶液时,酶液浓度最好控制在消耗0.05N硫代硫酸钠(空白--样品)的差数为3~6mL左右(以每毫升酶活力约50~90单位为宜)。
2.2.2.2测定:于甲、乙两支50mL比色管中、分别加入2%可溶性淀粉溶液25mL,0.1M乙酸-乙酸钠缓冲溶液(pH4.6)5ml.,摇勺。于40士0.2℃的恒温水浴中预热5~10min。在甲管中加入酶制备液2.0ml(酶的总活力约110170单位)立即记时,摇匀。在此温度下准确反应1h后,立即在甲、乙两管各加20%氢氧化钠溶液0.2mL,摇匀、将两管取出迅速用水冷却,并于乙管中补加酶制备液2.0mL(作为对照)取两管中上述反应液各5mL放入碘量瓶中,准确加入0.1N碘液10mL,再加0.1N氢氧化钠溶液15mL(边加边摇冕),放置暗处15min,加人2N硫酸2mL,用0.05N硫代硫酸钠溶液滴定至无色为终点。
2.2.2.3计算
1g酶粉或1mL酶液在40℃、pH4.6的条件下,1h分解可溶性淀粉产生1mg葡萄糖的酶量为一个酶活力单位。
1 ×32.2×n
X= (AB) ×N×90.05X-
式中:X-酶活力单位,u/g(mL);A-——空白试验消耗硫代硫酸钠溶液的毫升数;B-—样品消耗硫代硫酸钠溶液的毫升数;N-—硫代硫酸钠溶液的当量浓度:n稀释倍数;
90.05-—-1mL1N硫代硫酸钠相当葡葡糖毫克数;1 /2-折算成 1mL 酶液的量:
32.2---反应液总体积.毫升数;5-——吸取反应液的毫升数。
(1)
为计算方便,可按稀释倍数参考表计算,系数乘以滴定空自和样品所消耗0.05N硫代硫酸钠溶液91
的差值(A一B)为酶活力单位。表 2 为稀释倍数参考表。
稀释倍数
2.3水分
2.3.1测定程序
GB 8276-87
稀释倍数参考表
栅释倍数
于已知恒重的40mm×25mm称量皿中,称取酶粉约2.0000g,在105~~110℃恒温干燥箱内烘2h,移至干燥器中冷却,称重,再在干燥箱内烘干,直至恒重,2.3.2计算
样品中水分的含量,%;
式中:X,
W—称量血质量,g;
W,---烘干前血加样品质量,g,
W2—烘干后血加样品质量,g。
2.4细度
2.4.1测定程序
2×100
称取100g酶粉用40目标准分样筛(铜筛)筛分,称其未通过的酶粉质量。2.4.2计算
式中:X,
酶粉样品细度,%;
~原酶粉质量,gt
m筛后留存酶粉质量,g。
2.5酶活力保存率
M-m、
式中:X,酶活力保存率%;
E原酶粉(液)活力:
E检测酶活力
2.6重金属
2.6.1试剂
2.6.1.1硝酸:分析纯、
2.6.1.2硫酸:分析纯。
(3)
(4)
2.6.1.3盐酸:分析纯。
GB 8276—87
2.6.1.3.16N盐酸:量取500mL盐酸,用蒸馏水稀释至1000mL。2.6.1.3.21N盐酸:量取83mL盐酸,用蒸馏水稀释至1000mL。2.6.1.4氨水:分析纯。
2.6.1.4.15N氨水,量取333mL氨水,用蒸馏水稀至1000mL。2.6.1.4.21N氨水:量取66mL氨水,用蒸馏水稀释至1000mL。2.6.1.5pH3.5的乙酸盐缓冲液:称取25.0g乙酸铵溶于25mL蒸馏水中,加6N盐酸45mL,用稀盐酸或稀氨水调节pH至3.5,用蒸馅水稀释至100mL。2.6.1.61%酚酥指示液:按GB603.配制。2.6.1.7饱和硫化氢水;按GB603配制(此溶液于使用前制备)。2.6.1.8铅标准溶液(每毫升含0.01mg铅):按GB602配制,临用前用蒸馏水稀释10倍。2.6.2测定程序
2.6.2.1样品处理
称取5.0g样品置于250mL凯氏烧瓶或三角烧瓶中,加10~15mL硝酸漫润样品放置片刻(或过夜)后,缓缓加热,待作用缓和后稍冷,沿瓶壁加入5mL硫酸再缓缓加热,至瓶中溶液开始变成棕色,不断滴加硝酸(如有必要可滴加些高氯酸)至有机质分解完全,继续加热,至生成大量的二氧化硫白色烟雾。最后溶液应呈无色或微带黄色。冷却后将溶液移入50mL容量瓶中,用水洗涤三角烧瓶,将洗液并入容量瓶中,加蒸馏水至刻度,混勾,每10mL该溶液相当于1g样品。取同样重的硝酸、硫酸按上述方法作试剂空白试验。2.6.2.2样品测定
2.6.2.2.1溶液A:吸取含铅标准液1mL于50mL纳氏比色管中,加水至25mL混匀,加1滴1%酚指示液;用稀盐酸或稀氨水调节pH至中性(酚懿红色褪去)。加入pH3.5的乙酸盐缓冲液5mL,用蒸馅水稀释至40mL,混勾备用。2.6.2.2.2溶液B:取一支与溶液A所配套的纳氏比色管,加入20mL样品液,加蒸馏水至25mL混匀,加1滴1%酚酸指示液,用稀盐酸或稀氨水调节pH至中性(酚红色褪去),加入pH3.5的乙酸盐缓冲液5mL,用蒸馏水稀释至40mL,混匀备用。2.6.2.2.3溶液C:取一支与溶液A、B所配套的纳氏比色管,加人与溶液B相同量的样品液,再加入与溶液A相同量的铅标准液,加蒸馏水至25mL,混勾,加1滴1%酚酸指示液,用稀盐酸或稀氨水调节pH至中性(酚红色刚褪去),加入pH3.5的乙酸盐缓冲液5mL,用蒸馏水稀释至40mL,混匀备用。
2.6.2.2.4向各管中加入10mL新鲜制备的硫化氢饱和液,混匀,放置10min后在白色背景下观,溶液B的色度不得深于溶液A的色度,溶液C的色度应与溶液A的色度相当或深于溶液A的色度。2.7铅
按GB5009.12《食品中铅的测定方法》中的双硫踪单色法执行。样品处理采用硝酸-硫酸法。2.8砷
按GB5009.11《食品中总碑的测定方法》中的银盐法执行。样品处理采用硝酸-硫酸法。2.9黄曲霉毒素B,
按GB5009.22《食品中黄曲霉毒素Bi的测定方法》执行。2.10大肠菌群
按GB4789.3《食品卫生微生物学检验大肠菌群测定》执行。2.11沙门氏菌
按GB4789.3《食品卫生微生物学检验沙门氏菌检验》执行。93
3检验规则
GB 8276-87
3.1产品需经生产厂技术部门检验,并签发合格证方可出厂。生产厂以每一生产班次或每一髓进库的量为同一批次的产品。
3.2订货单位若需抽样检验,应从该酶制剂中抽取两份,按本标准规定的试验方法进行检验。若有一个样品或一项指标不符合标准的要求,应与生产厂协商,再取一倍量的同批样品共同进行复验,如仍不合格时,则全批产品作为不合格品,退交生产厂处理。若产品经复验合格,订货方应承担试验费用。如不合格,应由生产厂家承担试验费用。4标志、包装、运输、贮存
4.1酶制剂的外包装箱,除注明品名、生产厂名、规格、注册商标外,还应注明食品添加剂,箱里并应附有产品检验合格证,合格证上印有品名、批号、数量、规格、生产日期、检验员等。4.2内包装为食品用塑料袋,包装分为2kg、3kg,应印有注册商标、产品名称、规格、重量、生产厂名。
4.3本品含有生物活性物质,对光线、温度、湿度易引起失活。在运输途中应避免日光曝晒和雨淋。贮存仓库应保持清洁、阴凉、干燥、通风。附加说明:
本标准由中华人民共和国轻工业部、卫生部提出。本标准由轻工业部食品发酵工业科学研究所、卫生部食品卫生监督检验所归口。本标准由无锡酶制剂厂、轻工业部食品发酵工业科学研究所、天津市卫生防病中心、无锡市卫生防疫站负责起草。
食品添加剂
糖化酶制剂
Food additive
Glucoamvlase preperation
UDC 661.733
8276—87
本标准适用于由发酵法生产,经提纯制取,供食品生产作添加剂用的糖化酶制剂。1技术要求
1.1外观:固体时,粉状,无结块。液体时,黄褐色,允许有少量凝集物。1.2 项目和指标
酶活力,u/g(mL)
水分,%
细度(通过 40 目铜网筛),%
酶活力保存率(室温,半年),%重金属(以Pb计),%
铅,%
砷(以As计),%
黄曲霉毒素 B1,%
大肠菌群,个/100g(mL)
沙门氏菌下载标准就来标准下载网
2试验方法
2.1外观:用目视判定。
不低于
不低于
不超过
不超过
不超过
不超过
不多于
中华人民共和国轻工业部1987-10-19批准90
30 000,40 000,
50 000, 60 000,
80 000, 100 000,
150 000, 200 000
20 000, 30 000
40 000,50 000
60 000, 80 000
0.000 000 5
不得检出
1988-02-01实施
2.2酶活力测定
2-2.1试剂
GB 8276--87
2.2.1.10.1N乙酸-乙酸钠缓冲溶液(pH4.6):称取6.7g乙酸钠(CH,COONa·3HzO),吸取冰乙酸2.6mL,用蒸馏水溶解定容至1000mL,上述缓冲溶液应以酸度计校正pH值。2.2.1.20.05N硫代碗酸钠溶液:按GB601《化学试剂标准溶液制备方法》中2.7执行。2.2.1.30.1N碘液:按GB601《化学试剂标准溶液备方法》中2.10执行。2.2.1.40.1N氢氧化钠溶液:按GB601《化学试剂标准溶液制备方法》中2.2执行。2.2.1.52N硫酸溶液:量取分析纯浓硫酸(比重1.84)5.6mL缓缓加入适量蒸馏水中,冷却后用蒸馏水定容至100mL,摇匀。
2.2.1.620%氢氧化钠溶液:称取20g分析纯氢氧化钠,用蒸馏水溶解定容至100mL。2.2.1.72%可溶性淀粉溶液:称取可溶性淀粉2.00g,然后用少量蒸馏水调匀,徐徐倾入已沸的蒸馏水中,煮沸至透明,冷却,用蒸馏水定容至100mL,此溶液需当天配制。注:可溶性淀粉应符合HG3—3095质量标准要求。2.2.2测定程序
2.2.2.1待测酶液的制备;称取酶粉2.0000g(或1.00mL酶液),倒入50mL烧杯中,用少量的乙酸~乙酸钠缓冲溶液(pH4.6)溶解,并用玻璃棒捣碎,将上层清液小心倾入适当的容量瓶中,沉渣再加入少量上述缓冲溶液。如此反复捣研3~4次,最后全部移入容量瓶中,用缓冲溶液定容至刻度,摇匀,用4层纱布过滤。再用滤纸滤清,滤液供测定用。浓缩酶液可直接吸取一定量于容量瓶中,用缓冲溶液稀释定容室刻度。
注:制备酶液时,酶液浓度最好控制在消耗0.05N硫代硫酸钠(空白--样品)的差数为3~6mL左右(以每毫升酶活力约50~90单位为宜)。
2.2.2.2测定:于甲、乙两支50mL比色管中、分别加入2%可溶性淀粉溶液25mL,0.1M乙酸-乙酸钠缓冲溶液(pH4.6)5ml.,摇勺。于40士0.2℃的恒温水浴中预热5~10min。在甲管中加入酶制备液2.0ml(酶的总活力约110170单位)立即记时,摇匀。在此温度下准确反应1h后,立即在甲、乙两管各加20%氢氧化钠溶液0.2mL,摇匀、将两管取出迅速用水冷却,并于乙管中补加酶制备液2.0mL(作为对照)取两管中上述反应液各5mL放入碘量瓶中,准确加入0.1N碘液10mL,再加0.1N氢氧化钠溶液15mL(边加边摇冕),放置暗处15min,加人2N硫酸2mL,用0.05N硫代硫酸钠溶液滴定至无色为终点。
2.2.2.3计算
1g酶粉或1mL酶液在40℃、pH4.6的条件下,1h分解可溶性淀粉产生1mg葡萄糖的酶量为一个酶活力单位。
1 ×32.2×n
X= (AB) ×N×90.05X-
式中:X-酶活力单位,u/g(mL);A-——空白试验消耗硫代硫酸钠溶液的毫升数;B-—样品消耗硫代硫酸钠溶液的毫升数;N-—硫代硫酸钠溶液的当量浓度:n稀释倍数;
90.05-—-1mL1N硫代硫酸钠相当葡葡糖毫克数;1 /2-折算成 1mL 酶液的量:
32.2---反应液总体积.毫升数;5-——吸取反应液的毫升数。
(1)
为计算方便,可按稀释倍数参考表计算,系数乘以滴定空自和样品所消耗0.05N硫代硫酸钠溶液91
的差值(A一B)为酶活力单位。表 2 为稀释倍数参考表。
稀释倍数
2.3水分
2.3.1测定程序
GB 8276-87
稀释倍数参考表
栅释倍数
于已知恒重的40mm×25mm称量皿中,称取酶粉约2.0000g,在105~~110℃恒温干燥箱内烘2h,移至干燥器中冷却,称重,再在干燥箱内烘干,直至恒重,2.3.2计算
样品中水分的含量,%;
式中:X,
W—称量血质量,g;
W,---烘干前血加样品质量,g,
W2—烘干后血加样品质量,g。
2.4细度
2.4.1测定程序
2×100
称取100g酶粉用40目标准分样筛(铜筛)筛分,称其未通过的酶粉质量。2.4.2计算
式中:X,
酶粉样品细度,%;
~原酶粉质量,gt
m筛后留存酶粉质量,g。
2.5酶活力保存率
M-m、
式中:X,酶活力保存率%;
E原酶粉(液)活力:
E检测酶活力
2.6重金属
2.6.1试剂
2.6.1.1硝酸:分析纯、
2.6.1.2硫酸:分析纯。
(3)
(4)
2.6.1.3盐酸:分析纯。
GB 8276—87
2.6.1.3.16N盐酸:量取500mL盐酸,用蒸馏水稀释至1000mL。2.6.1.3.21N盐酸:量取83mL盐酸,用蒸馏水稀释至1000mL。2.6.1.4氨水:分析纯。
2.6.1.4.15N氨水,量取333mL氨水,用蒸馏水稀至1000mL。2.6.1.4.21N氨水:量取66mL氨水,用蒸馏水稀释至1000mL。2.6.1.5pH3.5的乙酸盐缓冲液:称取25.0g乙酸铵溶于25mL蒸馏水中,加6N盐酸45mL,用稀盐酸或稀氨水调节pH至3.5,用蒸馅水稀释至100mL。2.6.1.61%酚酥指示液:按GB603.配制。2.6.1.7饱和硫化氢水;按GB603配制(此溶液于使用前制备)。2.6.1.8铅标准溶液(每毫升含0.01mg铅):按GB602配制,临用前用蒸馏水稀释10倍。2.6.2测定程序
2.6.2.1样品处理
称取5.0g样品置于250mL凯氏烧瓶或三角烧瓶中,加10~15mL硝酸漫润样品放置片刻(或过夜)后,缓缓加热,待作用缓和后稍冷,沿瓶壁加入5mL硫酸再缓缓加热,至瓶中溶液开始变成棕色,不断滴加硝酸(如有必要可滴加些高氯酸)至有机质分解完全,继续加热,至生成大量的二氧化硫白色烟雾。最后溶液应呈无色或微带黄色。冷却后将溶液移入50mL容量瓶中,用水洗涤三角烧瓶,将洗液并入容量瓶中,加蒸馏水至刻度,混勾,每10mL该溶液相当于1g样品。取同样重的硝酸、硫酸按上述方法作试剂空白试验。2.6.2.2样品测定
2.6.2.2.1溶液A:吸取含铅标准液1mL于50mL纳氏比色管中,加水至25mL混匀,加1滴1%酚指示液;用稀盐酸或稀氨水调节pH至中性(酚懿红色褪去)。加入pH3.5的乙酸盐缓冲液5mL,用蒸馅水稀释至40mL,混勾备用。2.6.2.2.2溶液B:取一支与溶液A所配套的纳氏比色管,加入20mL样品液,加蒸馏水至25mL混匀,加1滴1%酚酸指示液,用稀盐酸或稀氨水调节pH至中性(酚红色褪去),加入pH3.5的乙酸盐缓冲液5mL,用蒸馏水稀释至40mL,混匀备用。2.6.2.2.3溶液C:取一支与溶液A、B所配套的纳氏比色管,加人与溶液B相同量的样品液,再加入与溶液A相同量的铅标准液,加蒸馏水至25mL,混勾,加1滴1%酚酸指示液,用稀盐酸或稀氨水调节pH至中性(酚红色刚褪去),加入pH3.5的乙酸盐缓冲液5mL,用蒸馏水稀释至40mL,混匀备用。
2.6.2.2.4向各管中加入10mL新鲜制备的硫化氢饱和液,混匀,放置10min后在白色背景下观,溶液B的色度不得深于溶液A的色度,溶液C的色度应与溶液A的色度相当或深于溶液A的色度。2.7铅
按GB5009.12《食品中铅的测定方法》中的双硫踪单色法执行。样品处理采用硝酸-硫酸法。2.8砷
按GB5009.11《食品中总碑的测定方法》中的银盐法执行。样品处理采用硝酸-硫酸法。2.9黄曲霉毒素B,
按GB5009.22《食品中黄曲霉毒素Bi的测定方法》执行。2.10大肠菌群
按GB4789.3《食品卫生微生物学检验大肠菌群测定》执行。2.11沙门氏菌
按GB4789.3《食品卫生微生物学检验沙门氏菌检验》执行。93
3检验规则
GB 8276-87
3.1产品需经生产厂技术部门检验,并签发合格证方可出厂。生产厂以每一生产班次或每一髓进库的量为同一批次的产品。
3.2订货单位若需抽样检验,应从该酶制剂中抽取两份,按本标准规定的试验方法进行检验。若有一个样品或一项指标不符合标准的要求,应与生产厂协商,再取一倍量的同批样品共同进行复验,如仍不合格时,则全批产品作为不合格品,退交生产厂处理。若产品经复验合格,订货方应承担试验费用。如不合格,应由生产厂家承担试验费用。4标志、包装、运输、贮存
4.1酶制剂的外包装箱,除注明品名、生产厂名、规格、注册商标外,还应注明食品添加剂,箱里并应附有产品检验合格证,合格证上印有品名、批号、数量、规格、生产日期、检验员等。4.2内包装为食品用塑料袋,包装分为2kg、3kg,应印有注册商标、产品名称、规格、重量、生产厂名。
4.3本品含有生物活性物质,对光线、温度、湿度易引起失活。在运输途中应避免日光曝晒和雨淋。贮存仓库应保持清洁、阴凉、干燥、通风。附加说明:
本标准由中华人民共和国轻工业部、卫生部提出。本标准由轻工业部食品发酵工业科学研究所、卫生部食品卫生监督检验所归口。本标准由无锡酶制剂厂、轻工业部食品发酵工业科学研究所、天津市卫生防病中心、无锡市卫生防疫站负责起草。
小提示:此标准内容仅展示完整标准里的部分截取内容,若需要完整标准请到上方自行免费下载完整标准文档。
标准图片预览:




- 其它标准
- 热门标准
- 国家标准(GB)
- GB/T38627-2020 信息技术 实时定位 磁定位数据接口
- GB/T8878—2014 棉针织内衣
- GB/T1182-2018 产品几何技术规范(GPS) 几何公差 形状、方向、位置和跳动公差标注
- GB175-2023 通用硅酸盐水泥
- GB/T12949-1991 滑动轴承覆有减摩塑料层的双金属轴套
- GB/T15349-1994 化学试剂 溴甲酚绿
- GB/T97.1-2002 平垫圈A级
- GB/T10125-2021 人造气氛腐蚀试验 盐雾试验
- GB/T228.1-2021 金属材料 拉伸试验 第1部分:室温试验方法
- GB/T43802-2024 绿色产品评价 物流周转箱
- GB/T42970-2023 半导体集成电路 视频编解码电路测试方法
- GB31094-2014 防爆电梯制造与安装安全规范
- GB50300-2013 建筑工程施工质量验收统一标准
- GB/T38987-2020 硬质合金螺旋孔棒材
- GB9178-1988 集成电路术语
- 行业新闻
请牢记:“bzxz.net”即是“标准下载”四个汉字汉语拼音首字母与国际顶级域名“.net”的组合。 ©2025 标准下载网 www.bzxz.net 本站邮件:wymp4wang@gmail.com