- 您的位置:
- 标准下载网 >>
- 标准分类 >>
- 医药行业标准(YY) >>
- YY/T 0142-1994 一次性使用输液、输血器具用空气过滤器
标准号:
YY/T 0142-1994
标准名称:
一次性使用输液、输血器具用空气过滤器
标准类别:
医药行业标准(YY)
标准状态:
现行出版语种:
简体中文下载格式:
.zip .pdf下载大小:
167.58 KB
点击下载
标准简介:
YY/T 0142-1994.
1主题内容 与适用范围
YY/T 0142规定了-次性使用输液、输血器具用空气过滤器的技术婴求、试验方法.检验规则.标志.包装.运输和贮存。
YY/T 0142主要适用于一次性使用输液、输血器具用空气过滤器(以下简称“空气过滤器")。该产品供一次性使用输液、输血器具配套用。
2引用标准
GB 2828连批检查计数抽样 程序及抽样表(适用于连续批的检查)
GB2829周期检查计数抽样程序及抽样表(适用于生产过程稳定性的检查)
GB8664输血、输液及配套用针
GB/T 14233.2医用输液 、输血、注射器具检验方法,第二部分 :生物试验方法
ZB C48 006医用高分子产品包装、标志运输和贮存
YY/T 0033无菌医疗 器具生产管理规范
3技术要求
3.1空叽过虑器的材料必须适合于-次性使用医疗器具所采用的灭菌方法,灭菌后不应变形。
3.2空气过滤器的生产应执行YY/T 0033的规定。
3.3空气过滤器外表面应光洁无毛刺,不应有明显的气泡杂质、裂痕等缺陷。
3.4空气过滤器应无急性仝身赤性。
3.5空气过滤 器滤除空气中0. 5 pm以上微粒的滤除率应不小于90%。
3.6空气过滤器在干燥状态下应保证良好的透气性;在没湿状态下,仍应保证透气.输出1000 mL浓度为9g/L的狐化钠溶液所需时间应不超过10min.
3.7向医院供应的空气过滤器应无菌。
4试验方法
4.1 外观
以目力观察。
4.2急性全身毒性试验
4.2.1供试液制备:取空气过滤器5只咒于无菌无热原容器中,每只过滤器加入无菌无热原生理盐水10mI.,加益振摇5min,使其浸没,咒60C没泡8h.
4.2.2试验方法按 GB/T 14233. 2第5章规定的方法进行。
4.3 滤除率试验
部分标准内容:
YY/T0142--94
一次性使用输液、输血器具用
空气过滤器
1994-05-13发布
国家医药管理局发布
1994-07-01实施
中华人民共和国医药行业标准
一次性使用输液、输血器具用
空气过滤器
1主题内容与适用范围
YY/T0142—94
本标准规定了一次性使用输液、输血器具用空气过滤器的技术要求、试验方法.检验规则、标志、包装、运输和存。
本标准主要适用于一次性使用输液、输血器具用空气过滤器(以下简称“空气过滤器”)。该产品供一次性使用输液、输血器具配套用。2引用标准
GB2828逐批检查计数抽样程序及抽样表(适用于连续批的检查)GB2829周期检查计数抽样程序及抽样表(适用于生产过程稳定性的检查)GB8664输血、输液及配套用针
GB/T14233.2医用输液、输血、注射器具检验方法第二部分:生物试验方法ZBC48006医用高分子产品包装、标志,运输和贮存YY/T0033无菌医疗器具生产管理规范3技术要求
3.1空气过滤器的材料必须适合于一次性使用医疗器具所采用的灭菌方法,灭菌后不应变形。3.2空气过滤器的生产应执行YY/T0033的规定。3.3空气过滤器外表面应光洁、无毛刺,不应有明显的气泡、杂质、裂痕等缺陷。3.4空气过滤器应无急性全身毒性。3.5空气过滤器滤除空气中0.5um以上微粒的滤除率应不小于90%。3.6空气过滤器在干燥状态下应保证良好的透气性:在浸湿状态下,仍应保证透气.输出1000mL浓度为9g/1.的氮化钠溶液所需时间应不超过10min。3.7向医院供应的空气过滤器应无菌。4试验方法
4.1外观
以目力观察。
4.2急性全身毒性试验
4.2.1供试液制备:取空气过滤器5只置于无菌无热原容器中,每只过滤器加入无菌无热原生理盐水10ml,加盖振摇5min,使其浸没,置60℃没泡8h。4.2.2试验方法按GB/T14233.2第5章规定的方法进行。4.3滤除率试验
国家医药管理局1994-05-13批准1994-07-01实施
4.3.1试验仪器
YY/T0142—94
尘埃粒子计数器,采样管长度为1m,采样次数为1次/min。转子流量计,量程为80mL/min或100mL/min。4.3.2试验步骤
在静态环境条件下,将尘埃粒子计数器与流量计相连,在空气流量为50mL/min下,测定1min内采集的空气中0.5μm以上的微粒数,连续读取五个数据。另取空气过滤器按使用方向使其与流抵计进气口相连,在相同空气流量下,测定1min内流经空气过滤器后的空气中0.5um以上的微粒数。连续读取五个数据。将五个数据中的最大值和最小值去掉,取其余三个值的平均值。4.3.3结果表示
空气过滤器的滤除率按下式计算:滤除率(%)
式中:N。空气中0.5μm以上的微粒数,100
N,-流经空气过滤器后的空气中0.5μm以上的微粒数。4.4流量试验
4.4.1试验装置
流量试验装置如下图所示。
输减售
编液管
试剂瓶
9g/LNaC1游液
进气针
空气过滤器
选气管
容置瓶
本试验所用的输液管、进气管是内径为3.0士0.2mm的聚筑乙烯管,输液针及进气针为符合GB8664的16号针,试剂瓶为1000mL小口试剂瓶,初始落差为1m。4.4.2试验方法
将1000mL试剂瓶中装满9g/L氯化钠溶液,按上图装罩进行试验,常温下,测量流出1000ml溶液所需要的时间。
4.5无菌检验
按GB/T14233.2第2章中小型配件器具的无菌试验方法进行。2
5检验规则
YY/T0142-94
5.1空气过滤器须经制造厂技术检验部门进行检验,合格后方可提交验收。5.2空气过滤器必须成批提交检查,检查分为逐批检查(出厂检查)和周期检查(型式试验或例行试验)。
5.3逐批检查
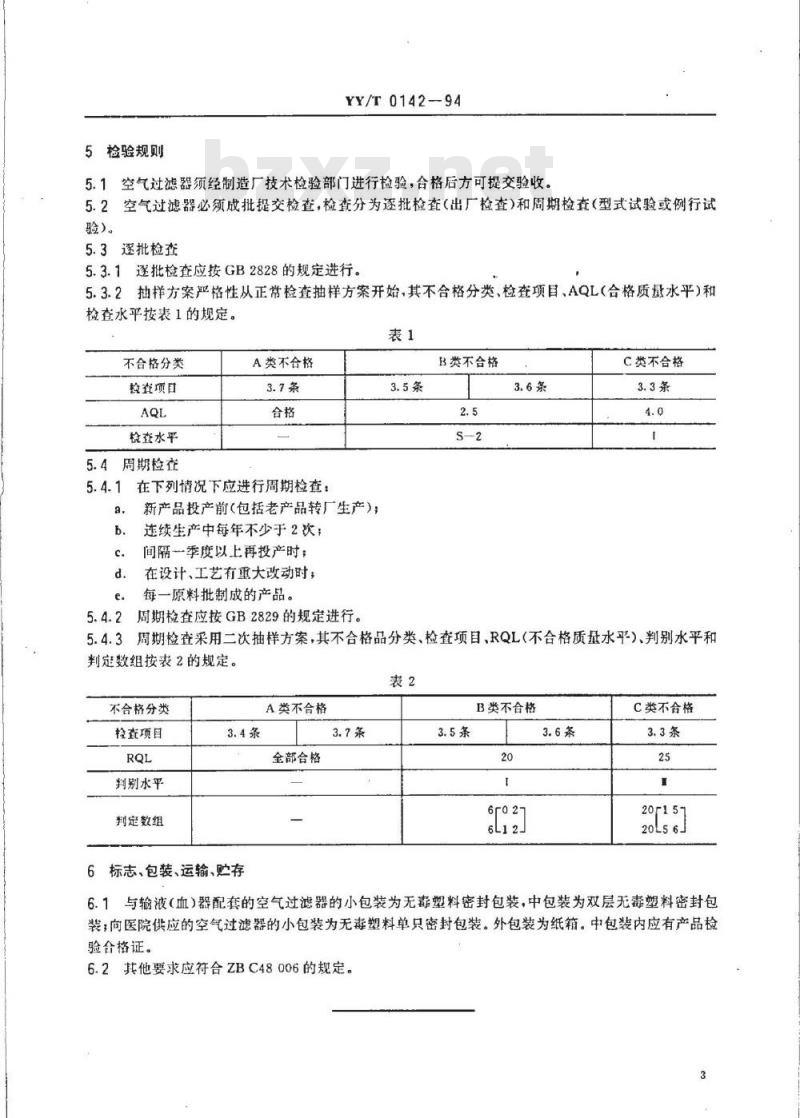
5.3.1逐批检查应按GB2828的规定进行。5.3.2抽样方案严格性从正常检查抽样方案开始,其不合格分类、检查项目、AQL(合格质量水平)和检查水平按表1的规定。
不合格分类
检查项目
检查水平
周期检在
A类不合格
在下列情况下应进行周期检查:5.4.1
新产品投产前(包括老产品转厂生产)连续生产中每年不少于2次;
间隔一季度以上再投产时;
在设计、工艺有重大改动时
每一原料批制成的产品。
周期检查应按GB2829的规定进行。3.5条
B类不合格
C类不合格
5.4.3周期检查采用二次抽样方案,其不合格品分类、检查项目、RQL(不合格质量水平)、判别水平和判定数组按表2的规定。
不合格分类
检查项目
判别水平
判定数组
A类不合格
金部合格
6标志、包装、运输、贮存
B类不合格
C类不合格
20r157
20L561
6.1与输液(血)器配套的空气过滤器的小包装为无毒塑料密封包装,中包装为双层无毒塑料密封包装;向医院供应的空气过滤器的小包装为无毒塑料单只密封包装。外包装为纸箱。中包装内应有产品检验合格证。
6.2其他要求应符合ZBC48006的规定。3
附加说明:
YY/T0142-94免费标准bzxz.net
本标准由全国医用输液器具标准化技术委员会提出。本标准由国家医药管理局医用高分子产品质量检测中心归口。本标准由国家医药管理局医用商分子产品质量检测中心、国家技术监督局沈阳培训中心综合技术开发公司负责起草。
本标准主要起草人施燕平、林红、惠瑞宁、王占第。(京)新登字023号
中华人民共和国医药
行业标准
一次性使用输液、输血器具用
空气过滤器
YY/T0142-94
中国标准出版社出版
北京复兴门外三里河北街16号
邮政编码:100045
话:8522112
中国标准出版社北京印刷厂印刷新华书店北京发行所发行各地新华书店经售版权专有不得翻印
开本880×12301/16印张1/2字数8千字1994年11月第一版1994年11月第一次印刷印数1-2000
标目252—41
小提示:此标准内容仅展示完整标准里的部分截取内容,若需要完整标准请到上方自行免费下载完整标准文档。
标准图片预览:




- 其它标准
- 热门标准
- YY医药标准
- YY/T0873.3-2014 ISO 6360-3: 2005 牙科旋转器械的数字编码系统 第3部分:车针和刃具的特征
- YY/T0454-2008 无菌塑柄手术刀
- YY/T0643-2008 IEC/TR 60854: 198G 超声脉冲回波诊断设备性能测试方法
- YY0581-2005 输液用肝素帽
- YY0574.3-2005 ISO 9703-3: 1992 麻醉和呼吸护理报警信号 第3部分:报警应用指南
- YY0449-2003 超声多普勒胎儿监护仪
- YY/T0917-2014 神经外科植入物可塑型预制颅骨板
- YY/T0870.4-2014 医疗器械遗传毒性试验 第4部分:哺乳动物骨髓红细胞微核试验
- YY/T0150-1993 医药工业企业能量平衡规则
- YY0310-1998 X射线计算机体层摄影设备通用技术条件
- YY/T0704-2008 IEC 61895: 1999 超声脉冲多普勒诊断系统性能试验方法
- YY0801.2-2010 ISO 9170-2 :2008 医用气体管道系统终端 第2部分:用于麻醉气体净化系统的终端
- YY/T0127.15-2018 口腔医疗器械生物学评价 第15部分:亚急性和亚慢性全身毒性试验:经口途径
- YY/T0915-2015 ISO 27020:2010 牙科学正畸用托槽和颊面管
- YY/T1586-2018 肿瘤个体化治疗相关基因突变检测试剂盒(荧光PCR法)
- 行业新闻
网站备案号:湘ICP备2025141790号-2