- 您的位置:
- 标准下载网 >>
- 标准分类 >>
- 医药行业标准(YY) >>
- YY 1301-2016 激光治疗设备铒激光治疗机
标准号:
YY 1301-2016
标准名称:
激光治疗设备铒激光治疗机
标准类别:
医药行业标准(YY)
标准状态:
现行出版语种:
简体中文下载格式:
.zip .pdf下载大小:
3.26 MB
点击下载
标准简介:
YY 1301-2016.Therapeutic laser equipment-Er : YAG laser equipment for therapy.
YY 1301规定了铒(Er:YAG)激光治疗机的基本参数和产品组成.技术要求.试验方法以及标志标签、包装等要求。
YY 1301适用于波长为2.94 pm的铒(Er: YAG)激光治疗机(以下简称治疗机)。该治疗机通过铒激光脉冲对人体组织的汽化、碳化和凝固,达到治疗的目的。
2规范性引用文件
下列文件对于本文件的应用是必不可少的。凡是注8期的引用文件,仅注日期的版本适用于本文件。凡是不注日期的引用文件,其最新版本(包括所有的修改单)适用于本文件。
GB/T191包装储运图示标志
GB 7247.1激光产 品的安全第1部分:设备分类、要求
GB 9706.1医用电气设备 第1 部分:安全通用要求
GB9706.20医用电气设备第2部分:诊断和治疗激光设备安全专用要求
GB/T 14710医用电 器环境要求及试验方法
GB/T 16886.1医疗器械生物学评价第1部分:医疗器械生物评价
GB/T 17736- -1999激光防 护镜主要参数测试方法
YY/T 0758治疗 用激光光纤通用要求
YY 1057医用脚踏开关通用技术条件
ISO 1146-1激光和激光相关设备 激光光束宽度 、发散角和光東传输比的试验方法第1部分:无像散和简单像散光東(Lasers and laser -related equipment test methods for laser beam widths,divergence angles and beam propagation ratios- Part 1 :Stigmatic and simple astigmatic beams)
ISO 11146-2激光和激光 相关设备激光光東宽度.发散角和光東传输比的测试方法第2部分:广义像散光東(Lasers and laser related equipment test methods for laser beam widths , divergence angles and beam propagation ratios- Part 2:General astigmatic beams)
ISO/TR 11146-3激光和激光相关设备 激光光束宽度 、发散角和光東传输比的试验方法第 3部分:本征和几何激光光東分类、传输和详细的试验方法(Lasers and laser -related equipment- Test methods for laser beam widths , divergence angles and beam propagation ratios-- Part 3: Intrinsic and geometrical laser beam classification, propagation and details of test methods)
3产品 组成和基本参数
3.1治疗机的组成 部分
治疗机的组成部分:
部分标准内容:
中华人民共和国医药行业标准
YY1301—2016
激光治疗设备
镇激光治疗机
Therapeutic laser equipment-Er: YAG laser equipment for therapy2016-03-23发布
国家食品药品监督管理总局
2018-01-01实施
本标准的全部技术内容为强制性前言
本标准按照GB/T1.1一2009给出的规则起草。YY1301-2016
请注意本文件的某些内容可能涉及专利。本文件的发布机构不承担识别这些专利的责任。本标准由国家食品药品监督管理总局提出。本标准由全国医用光学和仪器标准化分技术委员会(SAC/TC103/SC1)归口。本标准起草单位:浙江省医疗器械检验院。本标准主要起草人:叶岳顺、杜垫、贾晓航、韩坚城、孙瑜。I
1范围
激光治疗设备
镇激光治疗机
YY1301—2016
本标准规定了饵(Er:YAG)激光治疗机的基本参数和产品组成、技术要求、试验方法以及标志标签,包装等要求。
本标准适用于波长为2.94μm的饵(Er:YAG)激光治疗机(以下简称治疗机)。该治疗机通过饵激光脉冲对人体组织的汽化、碳化和凝固,达到治疗的目的。2规范性引用文件
下列文件对于本文件的应用是必不可少的。凡是注日期的引用文件,仅注日期的版本适用于本文件。凡是不注日期的引用文件,其最新版本(包括所有的修改单)适用于本文件。GB/T191包装储运图示标志
GB7247.1激光产品的安全第1部分:设备分类、要求GB9706.1医用电气设备第1部分:安全通用要求GB9706.20医用电气设备第2部分:诊断和治疗激光设备安全专用要求GB/T14710医用电器环境要求及试验方法GB/T16886.1医疗器械生物学评价第1部分:医疗器械生物评价GB/T17736—1999激光防护镜主要参数测试方法YY/T0758治疗用激光光纤通用要求YY1057医用脚踏开关通用技术条件ISO11146-1激光和激光相关设备激光光束宽度、发散角和光束传输比的试验方法第1部分:无像散和简单像散光束(Lasersandlaser-relatedequipmenttestmethodsforlaserbeamwidths,divergence angles and beam propagation ratios-Part 1,Stigmatic and simple astigmatic beams)ISO11146-2激光和激光相关设备激光光束宽度、发散角和光束传输比的测试方法第2部分:广义像散光束(Lasers and laser-related equipment test methodsforlaserbeamwidths,divergenceangles and beam propagation ratios-Part 2:General astigmatic beams)ISO/TR11146-3激光和激光相关设备激光光束宽度、发散角和光束传输比的试验方法第3部分:本征和几何激光光束分类、传输和详细的试验方法(Lasersandlaser-relatedequipment一Testmethods for laser beam widths,divergence angles and beam propagation ratios-Part 3:Intrinsic andgeometrical laser beam classification,propagation and details of test methods)3产品组成和基本参数
3.1治疗机的组成部分
治疗机的组成部分:
a)饵(Er:YAG)激光器:
激光电源和控制系统;
激光传输系统
HiiKAoNiKAca
YY1301—2016
脚踏开关;
激光防护眼镜;
冷却系统;
应用附件。
治疗机基本参数
制造商应在注册产品标准中列出下列基本参数:a)
治疗激光波长和模式;
治疗激光终端最大单脉冲能量;治疗激光脉冲能量(适用时);治疗激光最大脉冲功率P和最大平均功率P激光治疗面光斑尺寸;
激光治疗面能量密度/功率密度;治疗激光脉冲持续时间,参见图1;治疗激光脉冲串持续时间T1参见图1(适用时);治疗激光脉冲重复频率于或脉冲间隔T。治疗激光脉冲串重复频率于或脉冲间隔T.参见图1适用时);治疗激光终端发散角;
瞄准光波长;
m)瞄准光功率;
输出方式:单脉冲/脉冲重复/脉冲串单次/脉冲串重复,参见图1。安全类别
制造商应在注册产品标准中列出下列安全类别:按照GB9706.1规定的类和型:
b)按照GB7247.1规定的激光辐射类别。iiKAoNiKAca
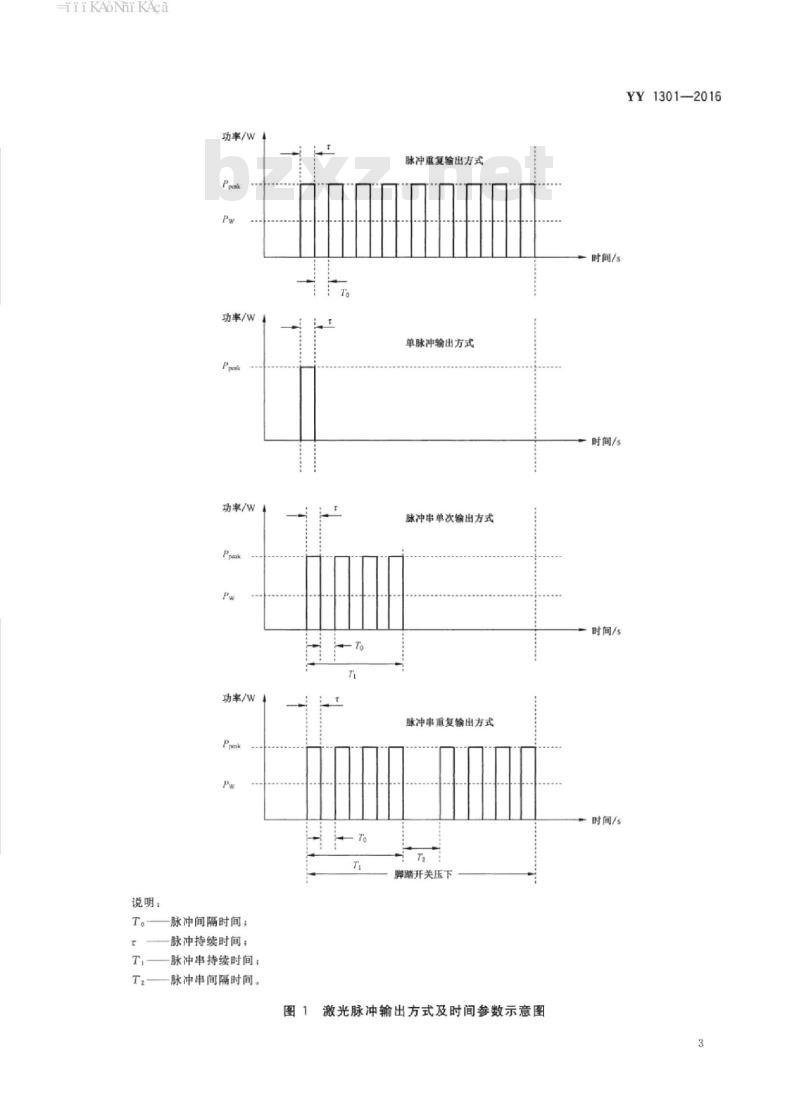
说明:
功率/W
功率/W
功率/W
功率/W
脉冲间隔时间:
脉冲持续时间;
一脉冲串持续时间;
脉冲串间隔时间。
脉冲重复输出方式
单脉冲输出方式
脉冲串单次输出方式
脉冲串重复输出方式
脚踏开关压下
图1激光脉冲输出方式及时间参数示意图时间/s
时间/s
时间/s
时间/s
YY1301-2016
TiiKAoNhi KAca
YY1301—2016
4要求
4.1正常工作条件
制造商应给出治疗机的正常工作条件,至少包括以下内容:a)环境温度:
b)相对湿度;
c)大气压力;
d)使用电源。
4.2治疗激光
4.2.1激光波长
激光波长2.94μm,允差为士0.1μm。4.2.2激光模式
基模或多模。
4.2.3激光脉冲持续时间
制造商应给出激光脉冲持续时间的标称值,若脉冲持续时间可以设置,应给出设置范围,标称值或设置范围的允差应不超过土20%。4.2.4激光脉冲串的持续时间(适用时)制造商应给出激光脉冲串持续时间的标称值,若脉冲串持续时间可以设置,应给出设置范围,标称值或设置范围的允差应不超过士20%。4.2.5激光脉冲重复频率或脉冲间隔制造商应给出激光脉冲重复频率或脉冲间隔的标称值,若脉冲重复频率或脉冲间隔可以设置,应给出设置范围,标称值或设置范围的允差应不超过士20%。4.2.6激光脉冲串重复频率或脉冲串间隔(适用时)制造商应给出激光脉冲串重复频率或脉冲串间隔的标称值,若脉冲串重复频率或脉冲串间隔可以设置,应给出设置范围,标称值或设置范围的允差应不超过士20%。4.2.7激光终端输出最大脉冲功率制造商应给出激光终端输出最大脉冲功率的标称值,其允差应不超过士20%。4.2.8激光终端输出最大平均功率制造商应给出激光终端输出最大平均功率的标称值,其允差应不超过士20%。4.2.9激光终端最大单脉冲能量及对应的脉冲持续时间制造商应给出激光终端最大单脉冲能量的标称值及对应的脉冲持续时间,其充差应不超过士20%。4.2.10激光终端脉冲能量(适用时)制造商应给出终端脉冲能量的标称值,若脉冲能量可以设置,应给出设置范围,标称值或设置范围4
HiiKAoNiKAca
的允差应为士20%。
4.2.11激光治疗面光斑尺寸
制造商应给出激光治疗面光斑尺寸的标称值,其允差应不超过土20%。4.2.12激光治疗面能量密度/功率密度YY1301—2016
制造商应给出激光治疗面能量密度/功率密度的设置范围,其充差应不超过士20%。4.2.13激光终端输出发散角
制造商应规定终端输出发散角的标称值,其允差应为士20%。4.2.14激光输出能量不稳定度S,激光输出能量不稳定度S.应优于士10%。4.2.15激光输出能量复现性R
激光输出能量复现性R,应优于士10%。4.2.16
输出附件
治疗机有输出附件时,制造商应规定各种激光输出附件的特性参数及其允差,允差应不超过±20%。
4.3瞄准系统
4.3.1瞄准光波长
制造商应规定瞄准光中心波长的标称值及允差,或中心波长的范围。4.3.2瞄准光的功率
瞄准光的功率不得大于5mW。
4.4激光传输系统
4.4.1激光光纤
治疗机采用激光光纤作为传输系统,应符合YY/T0758中适用项目的要求。4.4.2导光臂系统
治疗机采用导光臂作为传输系统,则其关节数应不少于3节,在其自由度范围内应无死角和/或碰壁现象。
4.5冷却系统
采用液体冷却的冷却系统,需满足以下要求:a)采用液体冷却的冷却系统应无渗漏现象:b)采用液体冷却的冷却系统发生故障时,应能自动切断激光电源4.6激光防护眼镜
治疗机应配置激光防护眼镜,需满足以下要求:5
TiiKAoNhi KAca
YY1301—2016
激光防护眼镜上应标明防护的波长范围和光密度值:防护镜对激光输出波长的光密度:≥4:b)
c)司
可见光透射比:≥40%。
4.7脚踏开关
脚踏开关应符合YY1057的要求
4.8与患者接触部分的生物学评价预计与患者接触的部分,应按照GB/T16886.1的要求进行生物学评价。4.9外观
外观应整洁、色泽均匀,无腐蚀,涂覆层剥落,伤痕,划痕,变形等缺陷4.9.2文字和标记应清晰可见。
4.9.3控制调节机构应灵活可靠、紧固部位无松动,按钮开关手感清晰,动作可靠。4.10安全
治疗机应符合GB9706.1,GB9706.20.GB7247.1的要求。制造商应分别按照GB9706.1GB9706.20,GB7247.1规定其安全特征(包括绝缘图)和适用章条。4.11环境适应性
治疗机的环境适应性应符合GB/T14710的要求;制造商应给出具体试验条件和检验项目。检验项目至少应包含4.2.8激光终端最大输出单脉冲能量及对应的脉冲宽度。5试验方法
5.1探测仪器要求
试验仪器应选用波长、测量范围和测量不确定度合适的测量仪器。5.2治疗激光试验
激光波长检验
用波长仪或光谱仪进行测量,并计算误差,结果应符合4.2.1的要求。5.2.2激光模式
用激光光束分析仪检查,应符合4.2.2的要求。5.2.3激光脉冲/脉冲串持续时间的检验用光电探测器和示波器测量,取输出波形半峰值功率点的时间差,测量.10次取平均值,若脉冲/脉冲串持续时间可以设置,则在设置范围内等间隔选取测量点,每个测量点测量10次取平均值,其结果应符合4.2.3和4.2.4的要求。
5.2.4激光脉冲/脉冲串重复频率或脉冲间隔的检验用光电探测器和示波器测量,测量10次取平均值,若脉冲/脉冲串重复频率或脉冲间隔可以设置,6
HiiKAoNiKAca
YY1301-2016
则在设置范围内等间隔选取测量点,每个测量点测量10次取平均值,其结果应符合4.2.5和4.2.6的要求。
5.2.5激光终端输出最大脉冲功率的检验按使用说明书中的方法进行设置,用能量计测量脉冲能量,脉冲持续时间按5.2.3的方法进行测量并计算,结果应符合4.2.7的要求。5.2.6激光终端输出最大平均功率按使用说明书中的方法进行设置,用功率计测量其功率,结果应符合4.2.8的要求。5.2.7激光终端最大输出单脉冲能量及对应的脉冲持续时间的检验按使用说明书中的规定,将能量调节到最大输出状态,按图2进行测量:激光源
光电探测器
激光能量计
测量激光最大输出单脉冲能量的同时按5.2.3的方法测对应的脉冲持续时间,测量10次,每次脉冲能量按式(1)计算,求出平均值,结果应符合4.2.9的要求:E。
式中:
E。—能量计测量的能量;
——分束器的分光比。
5.2.8激光终端脉冲能量的检验
按图2进行测量,若能设置脉冲能量,则在能量设置范围内等间隔选取测量点,测量激光终端脉冲能量和脉冲宽度,每个测量点测量10次取平均值,结果应符合4.2.10的要求。5.2.9治疗端面光斑尺寸的检验
按ISO11146中规定的方法进行测量,结果应符合4.2.11的要求。5.2.10激光终端输出能量密度/功率密度的检验按照使用说明书的规定,设置能量密度/功率密度及治疗端面光斑尺寸,能量/功率按图2进行测量,治疗端面光斑尺寸按ISO11146方法进行测量并计算其能量密度,结果应符合4.2.12的要求,5.2.11终端发散角的检验
按ISO11146,用激光光束分析仪测量,其结果应符合4.2.13的要求。7
HiiKAoNiKAca
YY1301—2016
5.2.12激光输出能量不稳定度的检验将治疗机终端激光输出能量调至额定工作状态,按制造商规定时间或将治疗时间规定为10min,按图3测量,在记录仪上等间隔读取100点E,(i=1,2,3...·100),找出E,中最大值Ex与最小值Emin,按式(2)计算激光输出能量不稳定度S.,应符合4.2.14的要求。Em-E×100%
式中:
测量次数:
第元次测量功率值:
E.的最大值:
E,的最小值。
治疗机
交流稳压器免费标准下载网bzxz
5.2.13激光输出能量复现性的检验TE
终端输出
光探测器
酶数记录仪
·.·..+*·(2)
将治疗机终端激光输出能量调至额定工作状态,用激光能量计进行测量;断开治疗机电源,间隔1min,再接通电源并在额定工作状态下,用激光能量计进行测量。如此重复5次,得5次测量值E:(i=1,2,3,4,5),找出E;中最大值Emx与最小值Emia。按式(3)计算终端输出激光能量复现性R,,结果应符合4.2.15的要求。
式中:
测量次数:
第i次测量功率值;
Emax——E:的最大值;
Emin—E,的最小值。
5.2.14输出附件的检验
Em-E×100%
R,=士
制造商应给出输出附件特性参数的检查方法。按此规定的方法测量并检查输出附件的特性参数,其结果符合4.2.16的要求。5.3瞄准系统检验
5.3.1瞄准光波长检验
用波长仪或光谱仪进行测量,并计算误差,结果应符合4.3.1的要求。8
5.3.2瞄准光的激光功率检验
用激光功率计进行测量,结果应符合4.3.2的要求。5.4激光传输系统检验
激光光纤检验
按照YY/T0758规定的方法进行,结果应符合4.4.1的要求。5.4.2导光臂系统检验
YY1301-2016
检查关节臂的关节数,并检查导光系统在X、Y、Z三个轴向的自由度及有无死角、碰壁现象。其结果应符合4.4.2的要求。
5冷却系统检验
采用液体冷却的冷却系统按以下方法检验:a)手感目测检查采用液体冷却的冷却系统是否有渗漏;b)使冷却系统停止工作,此时若激光器无法启动。其结果符合4.5的要求。
5激光防护眼镜检验
激光防护镜的检验应符合下列要求:a)按GB/T17736-1999中5.1的规定试验;b)按GB/T17736—1999中5.3的规定试验;c
目测检查。
其结果应符合4.6的要求。
脚踏开关检验
按YY1057规定的方法试验,结果应符合4.7的要求。5.8与患者接触部分的生物学评价按GB/T16886.1规定的方法进行,结果应符合4.8的要求。5.9
外观检验
手感目测,结果应符合4.9的要求。0安全项目检验
按照GB9706.1.GB9706.20.GB7247.1规定的方法试验,其结果应符合4.10的要求。5.11环境适应性
按照GB/T14710规定的方法、制造商给出的具体试验条件和检验项目进行检验,其结果应符合4.11的要求。
YY1301—2016
检验规则
出厂验收
治疗机由制造厂质量检验部门检验合格后并附合格证方可出厂。6.2
检验形式
检验分出厂检验和型式检验。
6.3出厂检验
出厂检验为逐台检验,制造商应在注册产品标准中规定出厂检验项目。6.3.1
检验不合格项可修正后再进行检验。6.4
型式检验
型式检验的要求
在下列情形之一时应进行型式检验:a)
医疗器械注册检验时;
正常生产时,如结构、材料、工艺改变对性能有较大影响时;停产一年以上再恢复生产时;
d)国家监督机构提出型式检验的要求时。6.4.2
型式检验的样品
注册检验时可送样,数量一台;其余型式检验的样品应从出厂检验合格产品中随机抽取一台。3检验项目
型式检验的检验项目为本标准全部项目。7标志、标签、使用说明书
7.1标志
每台治疗机应有下列标记:
制造广名称;
b)型号和名称;
电源电压:
电源频率;
输人功率;
设备安全分类;
g)熔断器型号及额定值(适用时):h)产品注册号:
GB9706.20及GB7247.1规定的标记。外包装箱上应有下列标志:
制造厂名称;
小提示:此标准内容仅展示完整标准里的部分截取内容,若需要完整标准请到上方自行免费下载完整标准文档。
标准图片预览:




- 热门标准
- YY医药标准
- YY/T1523-2017 二氧化碳测定试剂盒(PEPC酶法)
- YY/T0652-2008 ISO 17853 :2003 植入物材料的磨损聚合物和金属材料磨屑分离、表征和定量分析方法
- YY/T1636-2018 组织工程医疗器械产品再生膝关节软骨的体内磁共振评价方法
- YY0762-2009 眼科光学囊袋张力环
- YY0004-1990 普通胸腔镊
- YY0345-2002 骨接合植入物金属骨针
- YY/T0454-2003 无菌塑柄手术刀
- YY0315-2008 钛及钛合金人工牙种植体
- YY/T0452-2003 止血钳
- YY/T0663-2008 无源外科植入物 心脏和血管植入物的特殊要求 动脉支架的专用要求
- YY0464-2009 一次性使用血液灌流器
- YY/T1268-2015 环氧乙烷灭菌的产品追加和过程等效
- YY0286.6-2009 专用输液器 第6部分:-次性使用流量设定微调式输液器
- YY/T0457.6-2003 医用电气设备 光电X射线影像增强器特性 第6部分:对比度及炫光系数的测定
- YY0460-2003 超声洁牙设备
- 行业新闻
网站备案号:湘ICP备2025141790号-2