- 您的位置:
- 标准下载网 >>
- 标准分类 >>
- 医药行业标准(YY) >>
- YY/T 0188. 7-1995 药品检验操作规程 第7部分:化学原料药含量测定法
标准号:
YY/T 0188. 7-1995
标准名称:
药品检验操作规程 第7部分:化学原料药含量测定法
标准类别:
医药行业标准(YY)
标准状态:
现行出版语种:
简体中文下载格式:
.zip .pdf下载大小:
624.56 KB
手机扫码下载更方便
点击下载
标准简介:
YY/T 0188. 7-1995.Operating methods for the tests and assays of drugs Part 7 :Assays of pharmaceutical chemicals.
5.43适用范围
5.4.3.1在酸性溶液中 ,可用高锰酸钾直接测定还原性物质。
5.4.3.2 Ca2+ 、Ba2+、2n2+ ,Cdl+ 等金属盐可使之与C.0?-形成沉淀,再将沉淀溶于硫酸然后用高锰酸钾液滴定置换出来的荜酸,从而测定金属盐的含量。
5.4.3.3以草酸钠滴定液或硫酸亚铁滴定液配合,采用剩余回滴法,可测定-些强氧化剂。
5.4.4试剂和溶液
a)草酸液(0. 05.0. 25 mol/L)按药 典方法配制、标定、贮救;
b)商锰酸钾液(0.02 ,0.002 mol/L)按药 典方法配制、标定、贮藏;
c)硫酸(分析纯);
d)草酸(分析纯)。
5.4.5仪器 和设备
a)电烘箱;
b)分析天平(万分之- -);
c)滴定管(25、50 mL);
d)锥形瓶(250 mL); .
e)烧杯(200 mL)。
5.4.6操作方法
取供试品适量,精密称定,梢确至0.0001g.按各药品含量测定项下规定方法操作。
5.4.7注意事项
5.4.7.1配制高锰酸钾液应煮沸15min,密塞放暨2日以上,用玻璃垂熔漏斗过滤,指匀,再标定使用。因高锰酸钾中常含有二氧化锰等杂质,水中的有机物和空气中的尘埃等还原性物质都会使高锰酸钾液的浓度改变。
5.4.7.2高锰酸钾和 草酸钠开始反应逮度很慢,应将溶液加热至65C ,但不可过高,高于90C会使部分草酸分解。
5.4.7.3为使反应正常进行,溶液应保持一定的酸度。酸度不足反应产物可能混有二氧化锰沉淀;酸度过商,会促使草酸分解,开始滴定酸度应在0.5~1mol/L.
5.4.7.4配制好的高锰酸钾 液,应贮存于棕色玻璃瓶中,避光保存,以防光的影响。
5.4.7.5在30 s内,溶液颜色不提为滴定终点。因为空气中的还原性气体和尘埃落于溶液中,也能分解高锰酸钾,使其颜色消失。
5.4.7.6用稀高铥酸钾液(0. 002 mol/L)滴定时,为使终点容易观察,可选用氧化还原指示剂。用邻二氮菲为指示剂,终点由红色变浅蓝色,用二苯胺磺酸钠为指示剂,终点由无色变紫色。
5.4.8结果计算
见3.10.
5.4.9允许差
本法的相对偏差不得超过0. 3%。
5.5 铈量法
部分标准内容:
本标准是依据《中华人民共和国药典》(1995年版),对ZBC10004-89《化学原料药的含量测定法》进行修订的。
本标准对化学原料药化学分析法作了详细的说明与规定,是统一药品检验操作的规范化工作指南。本标准对原标准进行较大的改动有:1.对含量计算通式,根据中国药典所选用滴定液的基本单元,将滴定法的原等物质的量规则计算式改为换算因数计算式,并增加了重量法的挥发法和萃取法计算式;2。在氧化还原法中,增加了溴量法;3.在非水溶液滴定法中,对原标准操作法的第一法、第二法合并为一,并增加电位滴定内容,对高氟酸液的使用与标定温差,由原标准5℃改为与中国药典统一10d,并按药典增加了温度校正公式;4.对各种分析方法中的操作方法,鉴于不同样品的操作方法有差异,不宜作具体规定,本标准改为“按各药品项下规定方法操作”,要求遵循法定标准的规定操作;5.在络合滴定中,增加了直接滴定法、回滴定法和间接滴定法的有关内容。本标准从生效之日起,同时代替ZBC10004一89。本标准由国家医药管理局提出并归口。本标准起草单位:山东新华制药厂。本标准主要起草人:谢淼。
本标准于1989年3月首次发布,于1995年7月第一次修订129
1范围
中华人民共和国医药行业标准
药品检验操作规程
第7部分:化学原料药含量测定法Operating methods for the tests and assays of drugsPart 7:Assays of pharmaceutical chemicals本标准规定了化学原料药化学分析法测定含量操作的要求。本标准适用于化学原料药化学分析法的含量测定。2引用标准
中华人民共和国药典(1995年版)3含量测定规则
YY/T0188.7—1995
代替ZBC10004—89
3.1含量测定必须平行测定两份,其结果应在允许相对偏差限度之内,以算术平均值为测定结果,如一份合格,另一份不合格,不得平均计算,应重新测定。3.2如未采用药典规定的含量测定方法,应有比较实验数据,并应在允许相对偏差内,方可采用。仲裁时以药典方法为准。
3.3在记录中必须列出含量测定的计算式。3.4'取供试品量,不得超过药典规定量的士10%。3.5供试品如系挥发性或吸湿性物质,称供试品必须用密封好的容器。3.6重量法恒重系指供试品连续两次炽灼或干燥后的重量之差不得超过0.3mg。3.7滴定液的浓度,以mol/L表示。3.8含量测定,按干品计算,含量(%)后应注明以干品计。3.9供试品为液体,含量(%)后应注明m/m、m/V、V/V。3.10含量计算通式
3.10.1重量法
3.10.1.1沉淀法
供试品含量(%)一称量形戏质量()X换算因数×100供试品质量(g)
被测成分的相对原子量或相对分子量式中:换算因数一聋
称量形式的相对分子量
3.10.1.2挥发法
供试品含量(%)=
减失质最(g)
×100(以减失质量计)
供试品质量(g)
供试品含量(%):
国家医药管理局1995-07-11批准130
残留质量(g)
×100(以残留质量计)
供试品质量(g)
TKAoNiKAca
(2)
1996-05-01实施
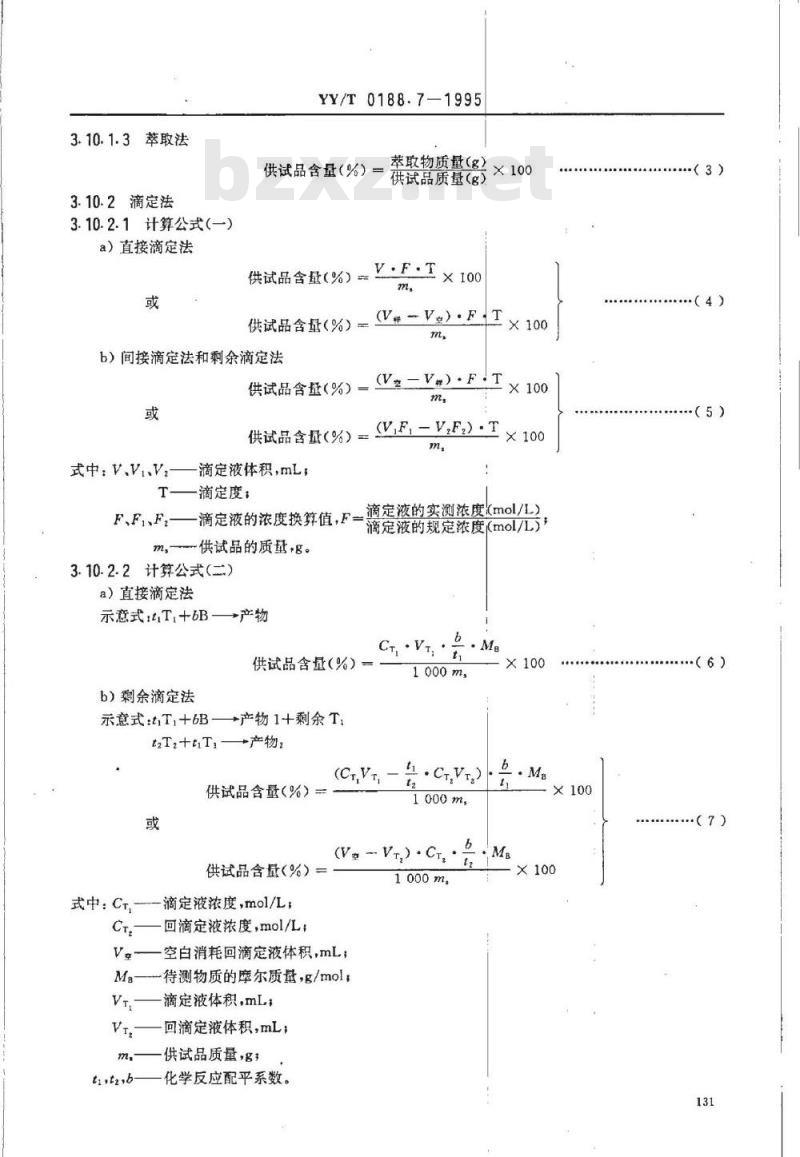
3.10.1.3萃取法
3.10.2滴定法
3.10.2.1计算公式(—)
a)直接滴定法
YY/T0188.7—1995
供试品含量(%)=
萃取物质量(g)
供试品质量(g)
V.F.T×100
供试品含量(%)一
供试品含量(%)=9
b)间接滴定法和剩余滴定法
供试品含量(%)=(V-V#)·FTm
供试品含量(%)=E-VF)T×100
式中:V.ViV2—滴定液体积,mLT—滴定度;
滴定液的实测浓度(mol/L)
F、F,、F,——滴定液的浓度换算值,F滴定液的规定浓度(mol/L)
m,供试品的质量g。
3.10.2.2计算公式(二)
a)直接滴定法
示意式:T+B→产物
供试品含量(%)
b)剩余滴定法
示意式:tT,+6B+产物1+剩余T
tT,+tT
→产物
供试品含量(%):
供试品含量(%):
式中:Ct,滴定液浓度,mol/L
Ct.回滴定液浓度,mol/L;
1000m,
(Va-- VT,) .CT, .
空白消耗回滴定液体积,mL;
Ma—待测物质的摩尔质量,g/mol;Vt.滴定液体积,mL
Vt,回滴定液体积,mL;
tu,tz,b-
供试品质量,g,
化学反应配平系数。
(3)
(4)
(5)
(6)
YY/T0188.7-1995
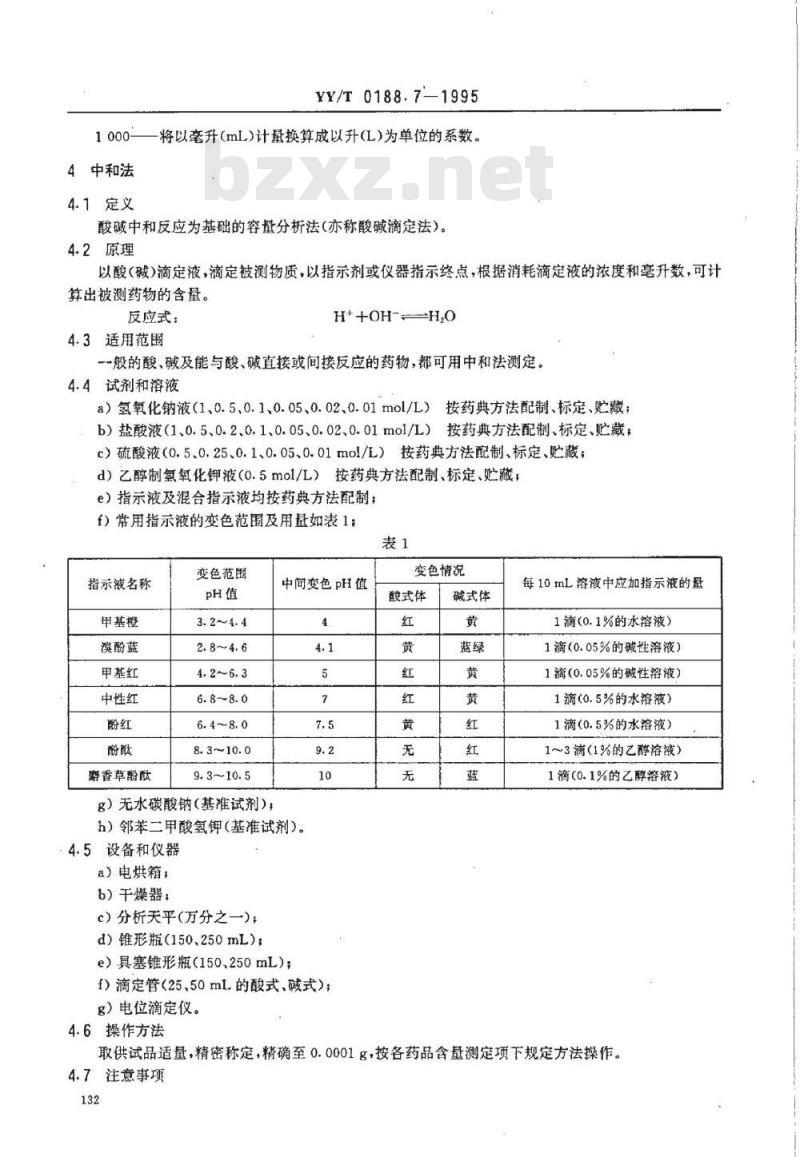
1000—将以毫升(mL)计量换算成以升(L)为单位的系数。4中和法
4.1定义
酸碱中和反应为基础的容量分析法(亦称酸碱滴定法)。4.2原理
以酸(碱)滴定液,滴定被测物质,以指示剂或仪器指示终点,根据消耗滴定液的浓度和毫升数,可计算出被测药物的含量。
反应式:
4.3适用范围
H++OH-H,0
一般的酸、碱及能与酸、碱直接或间接反应的药物,都可用中和法测定。4.4试剂和溶液
a)氢氧化钠液(1、0.5、0.1、0.05、0.02、0.01mol/L)按药典方法配制、标定、贮藏;b)盐酸液(1、0.5、0.2、0.1、0.05、0.02、0.01mo1/L)按药典方法配制、标定、贮藏;c)硫酸液(0.5、0.25、0.1、0.05、0.01mo1/L)按药典方法配制、标定、贮藏;d)乙醇制氢氧化钾液(0.5mol/L)按药典方法配制、标定、贮藏,e)指示液及混合指示液均按药典方法配制:f)常用指示液的变色范围及用量如表1;表1
指示液名称
甲基橙
漠酚蓝
甲基红
中性红
斑香草酚酸
变色范围
g)无水碳酸钠(基准试剂),
中间变色PH值
h)邻苯二甲酸氢钾(基准试剂)。4.5设备和仪器
a)电烘箱;
b)干燥器;
c)分析天平(万分之一);
d)锥形瓶(150、250mL);
e)具塞锥形瓶(150.250mL);f)滴定管(25、50mL的酸式、碱式);g)电位滴定仪。
4.6操作方法
变色情况
酸式体
碱式体
每10mL溶液中应加指示液的量
1滴(0.1%的水溶液)
1滴(0.05%的碱性溶液)
1滴(0.05%的碱性溶液)
1滴(0.5%的水溶液)
1滴(0.5%的水溶液)
1~3滴(1%的乙醇溶液)
1滴(0.1%的乙醇溶液)
取供试品适量,精密称定,精确至0.0001g,按各药品含量测定项下规定方法操作。4.7注意事项
HTYKAONYKAca
4.7.1本法须在常温下进行。
YY/T0188.7--1995
4.7.2用浓盐酸配制各种不同浓度的滴定液和试液时,应在防毒橱内操作。用浓硫酸配制各种不同浓度的滴定液和试液时,应将浓硫酸缓缓倒入蒸馏水中,边倒边搅拌,严禁将水倒入浓硫酸中。
4.7.3基准碳酸钠,应在270~300℃干燥至恒重以除去水分和碳酸氢钠,温度不宜过高,以防碳酸钠分解。已干燥好的碳酸钠应避免与空气接触,以防吸潮。4.7.4以基准碳酸钠标定盐酸或硫酸,近终点时加热2min,为逐去溶液中的二氧化碳。4.7.5中和法在供试品溶解后和滴定过程中,不得有三氧化硫、二氧化硫和氮气等存在。4.7.6所用的指示液,变色范围必须在滴定突跃范围内。4.7.7要按规定量加入指示液,因指示液本身具有酸性或碱性,能影响指示剂的灵敏度。4.8结果计算
见3.10。
4.9允许差
本法的相对偏差不得超过0.3%。5氧化还原法
5.1定义
以氧化还原反应为基础的容量分析法。5.2原理
氧化还原反应是反应物间发生电子转移。示意式:
还原剂1ne氧化剂1
氧化剂2+ne——还原剂2
还原剂1+氧化剂2=一氧化剂1+还原剂2氧化还原反应按照所用氧化剂和还原剂的不同,常用的方法有碘量法、高锰酸钾法和铈量法溴量法等。
5.3碘量法
5.3.1定义
利用碘分子或碘离子进行氧化还原滴定的容量分析法。5.3.2原理
碘量法的反应实质,是碘分子在反应中得到电子,碘离子在反应中失去电子。半反应式:
碘量法分直接碘量法和间接碘量法。5.3.3适用范围
5.3.3.1直接滴定法
I,+2e—21
21-—2e——12
凡能被碘直接氧化的药物,均可用直接滴定法。5.3.3.2剩余滴定法
凡需在过量的碘液中和碘定量反应,剩余的碘用硫代硫酸钠回滴,都可用剩余滴定法。5.3.3.3置换滴定法
凡被测药物能直接或间接定量地将碘化钾氧化成碘,用硫代硫酸钠液滴定生成的碘,均可间接测出其含量。
5.3.4试剂和溶液
YY/T0188.7-1995
硫代硫酸钠液(0.1、0.01、0.005mol/L)按药典方法配制、标定、购藏;碘液(0.1、0.05mol/L)按药典方法配制、标定、贮藏,重铬酸钾(基准试剂),
三氧化二砷(基准试剂);
碘化钾(分析纯);
盐酸(分析纯),
碳酸氢钠(分析纯);
h)甲基橙指示液(配制方法见4.4);i)淀粉指示液取可溶性淀粉0.5g,加水5mL搅匀后缓缓倾入100mL沸水中,随时搅拌,继续煮沸2min,放冷,倾出上层清液,即得。5.3.5仪器和设备
a)电烘箱;
分析天平(万分之一);
c)滴定管(25、50mL),
d)锥形瓶(250mL)
e)碘瓶(250mL),
f)垂熔漏斗。
5.3.6操作方法
取供试品适量,精密称定,精确至0.0001g,按各药品含量测定项下规定方法操作。5.3.7注意事项
5.3.7.1配制硫代硫酸钠液所用的蒸馏水须煮沸并冷却,除去二氧化碳和杀死微生物,然后加入少量无水碳酸钠,使溶液呈弱碱性。5.3.7.2硫代硫酸钠液应放暨1个月后再过滤和标化,因硫代硫酸钠中常含有多硫酸盐,可与OH-反应生成硫代硫酸盐使硫代硫酸钠液浓度改变。5.3.7.3发现硫代硫酸钠液混浊或有硫析出时,不得使用。5.3.7.4碘液应贮存于棕色具塞玻璃瓶中,在暗凉处避光保存。碘液不可与软木塞、橡胶管或其他有机物接触,以防碘浓度改变。
5.3.7.5直接滴定法反应应在中性、弱碱性或酸性溶液中进行。5.3.7.6淀粉指示液的灵敏度随温度的升高而下降,故应在室温下放暨和使用。5.3.7.7剩余滴定法淀粉指示液应在近终点时加入,否则将有较多的碘被淀粉胶粒包住,使蓝色褪去很慢,妨碍终点观察。
5.3.7.8淀粉指示液应在冷处放置,使用时应不超过1周。5.3.8结果计算
见3.10。
5.3.9允许差
本法的相对偏差不得超过0.3%。5.4高锰酸钾法
5.4.1定义
以高锰酸钾液为滴定剂的氧化还原法称为高锰酸钾法。5.4.2原理
在酸性条件下高锰酸钾具有强的氧化性,可与还原剂定量反应。半反应式:
MnO+8H++5eMn2++4H0
HITKAONTKAca
在微酸性、中性和弱碱性溶液中:YY/T 0188.7-1995
MnO+2H,O+3eMnO,+
5.4.3适用范围
5.4.3.1在酸性溶液中,可用高锰酸钾直接测定还原性物质。5.4.3.2Ca2+、Ba2+、Zn2+、Cd2+等金属盐可使之与C,O?-形成沉淀,再将沉淀溶于硫酸然后用高锰酸钾液滴定置换出来的草酸,从而测定金属盐的含量。5.4.3.3以草酸钠滴定液或硫酸亚铁滴定液配合,采用剩余回滴法,可测定一些强氧化剂。5.4.4试剂和溶液
a)草酸液(0.05、0.25mol/L)按药典方法配制、标定、贮藏;b)高锰酸钾液(0.02、0.002mol/L)按药典方法配制、标定、贮藏;c)硫酸(分析纯);
d)草酸(分析纯)。
5.4.5仪器和设备
a)电烘箱:
b)分析天平(万分之一);
c)滴定管(25、50mL);
d)锥形瓶(250mL):
e)烧杯(200mL)。
5.4.6操作方法
敢供试品适量,精密称定,精确至0.0001g,按各药品含量测定项下规定方法操作。5.4.7注意事项
5.4.7.1配制高锰酸钾液应煮沸15min,密塞放置2日以上,用玻璃垂熔漏斗过滤,摇匀,再标定使用。因高锰酸钾中常含有二氧化锰等杂质,水中的有机物和空气中的尘埃等还原性物质都会使高锰酸钾液的浓度改变。
5.4.7.2高锰酸钾和草酸钠开始反应速度很慢,应将溶液加热至65℃,但不可过高,高于90C会使部分草酸分解。
5.4.7.3为使反应正常进行,溶液应保持一定的酸度。酸度不足,反应产物可能混有二氧化锰沉淀;酸度过商,会促使草酸分解,开始滴定酸度应在0.5~1mol/L。5.4.7.4配制好的高锰酸钾液,应贮存于棕色玻璃瓶中,避光保存,以防光的影响。5.4.7.5在30s内,溶液颜色不褪为滴定终点。因为空气中的还原性气体和尘埃落于溶液中,也能分解高锰酸钾,使其颜色消失。
5.4.7.6用稀高锰酸钾液(0.002mol/L)滴定时,为使终点容易观察,可选用氧化还原指示剂。用邻二氮菲为指示剂,终点由红色变浅蓝色,用二苯胺磺酸钠为指示剂,终点由无色变紫色。5.4.8结果计算
见3.10。
5.4.9允许差
本法的相对偏差不得超过0.3%。5.5铈量法
5.5.1定义
以硫酸铈溶液为滴定剂测定还原性药物含量的方法。5.5.2原理
硫酸铺是一种强氧化剂,它可与还原性药物定量反应,四价铺被还原为三价铺,用已知浓度的硫酸铈液与被测还原性药物反应,根据到达终点所消耗的硫酸铈滴定液的浓度和毫升数,可计算出被测药物135
的含量。
半反应式:
5.5.3适用范围
YY/T0188.7-1995
Ce*++eCe'+
本法可在浓盐酸溶液中滴定还原性药物和在蔗糖、淀粉存在下直接滴定糖浆或片剂中的亚铁。5.5.4试剂和溶液
a)硫酸液(0.1、0.01mol/L)按药典方法配制、标定、藏:b)邻二氮菲指示液取硫酸亚铁0.5g,加水100mL使溶解,加硫酸2滴与邻二氮菲0.5g,摇匀,即得;
c)稀硫酸取硫酸57mL,在搅拌下缓缓加入940mL水中,待冷却后,稀释至1000mL,摇勺,即得,
d)一氯化碘试液取碘化钾0.14g与碘酸钾90mg加水125mL,使溶解,再加盐酸125mL,摇匀,即得:
e)三氧化二砷(基准试剂)。
5.5.5仪器和设备
a)电烘箱;
b)分析天平(万分之-);
c)锥形瓶(250mL);
d)滴定管(50mL)。
5.5.6操作方法
取供试品适量,精密称定,精确至0.00018,按各药品含量测定项下规定方法操作。5.5.7注意事项
5.5.7.1硫酸铈液呈黄色,而亚铺盐为无色。故滴定无色溶液可不用指示剂,利用它本身的浅黄色判断终点即可。用邻二氮菲指示液,颜色由浅红色变为浅蓝色即为终点。5.5.7.2铺量法不适用于中性或碱性介质中进行,因Ce+易水解,生成碱式盐沉淀。5.5.7.3有F-离子存在时不能用量法。因F-离子可与Ce+形成稳定的络合物,使Ce*+的黄色消失。
5.5.7.4标定硫酸铈液,所用的一氟化碘试液和邻二氮菲指示液,应于临用前配制。5.5.7.5选用氧化还原指示剂应比被测药物更难氧化,如滴定亚铁选用二苯胺磺酸钠为指示剂,滴定溶液应加入磷酸以免氧化产物Fe3+把指示剂氧化,使终点过早出现。5.5.8结果计算
见3.10。
5.5.9允许差
本法的相对偏差不超过0.3%。
5.6溴量法
5.6.1定义
利用溴液产生漠,进行被测药物定量的容盐分析法。5.6.2原理
利用溴液产生定量的新生态溴,与被测药物作用,并用碘化钾作用于剩余的溴,析出碘用硫化硫酸钠液滴定,即可计算出被测药物的含量。BrO+5Br=+6Ht3Brz+3H,0
Br2+21I2+2Br
1,+2NaSO,→2NaI+NaS.0
5.6.3适用范围
TrKANrKAca
YY/T0188.7-1995
本法可以测定一些还原性药物和能够漠化的有机药物。5.6.4试剂与溶液
a)溴液(0.1mol/L)按药典方法配制、标定、贮藏;b)硫化硫酸钠液(o.1mol/L)按药典方法配制、标定、贮藏:c)盐酸(分析纯);
d)碘化钾试液取碘化钾16.5g,加水使溶解成100mL即得(应临用新制);见5.3.4。
e)淀粉指示液
5.6.5仪器和设备
a)分析天平(万分之一);
b)滴定管(25、50mL);
c)移液管(25、30mL):
d)碘瓶(250mL)。
5.6.6操作方法
取供试品适量,精密称定,精确至0.0001g,按各药品含量测定项下规定方法操作。5.6.7注意事项
5.6.7.1溴极易挥发,碘瓶魔口应严密并水封,操作过程应特别小心,防止漠逸出损失,影响测定结果。5.6.7.2溴液应置有玻塞的棕色玻瓶中,密闭在凉处保存。5.6.7.3其他注意事项见5.3.7有关条文。5.6.8结果计算
见3.10。
5.6.9允许差
本法的相对偏差不得超过0.3%。6络合滴定法
6.1定义
以络合反应为基础的容量分析法,称为络合滴定法。6.2原理
乙二胺四乙酸二钠液(EDTA)能与许多金属离子定量反应,形成稳定的可溶性络合物,依此,可用已知浓度的EDTA液直接或间接滴定某些药物,用适宜的金属指示剂指示终点:根据消耗的EDTA滴定液的浓度和毫升数,可计算出被测药物的含量。反应机理(以二价和三价金属离子的络合物反应为例):与二价金属离子Me2+反应:
CHCOOH
CHCOOH
与三价金属离子Me3+反应:
CHCOOH
6.2.1直接滴定法
YY/T0188.7-~1995
Me\++H,Y2-MeY-)+2H+
与金属离子化合价无关,均以1:1的关系络合6.2.2回滴定法
Me*++H,Y*-(过量)=-MeYa-4)+2H+H,Y2-(剩余)+Zn+—ZnY2-+2H
6.2.3间接滴定法
利用阴离子与某种金属离子的沉淀反应,再用EDTA滴定剩余的金属离子,间接测出阴离子含量。6.3适用范围
EDTA可直接或间接测定40多种金属离子的含量,也可间接测定一些阴离子的含量。在药物分析上,用于测定无机和有机金属盐类药物。6.4试剂和溶液
a)EDTA液(0.05mol/L)按药典方法配制、标定、贮藏:b)锌液(0.05mol/L)按药典方法配制、标定;c)甲基红乙醇溶液0.025%的甲基红乙醇溶液;d)铬黑T指示剂取铬黑To.1g,加氯化钠10g,研磨均匀,即得,e)钙紫红素指示剂取钙紫红素0.1g,加无水硫酸钠10g,研磨均匀,即得,f)钙黄绿素指示剂取钙黄绿素0.1g,加氯化钾10g,研磨均匀,即得;g)氢氧化钠试液取氢氧化钠4.3g,加水使溶解成100mL,即得;h)乙酸-乙酸钠缓冲液(pH4.5)取乙酸钠18g加冰乙酸9.8mL,再加水稀释至1000mL,即得;i)乙酸-乙酸钠缓冲液(pH6)取乙酸钠54.6g加乙酸液(1mol/L)20mL溶解后,加水稀释至500mL,即得;
j)氨-氯化铵缓冲液(pH8.0)取氯化铵1.07g加水使溶解成100mL,再加稀氨溶液(1→30)调节PH值至8.0,即得;
k)氨-氯化铵缓冲液(pH10.0)取氯化铵5.4g加水20mL溶解后,加浓氨溶液35mL,再加水稀释至100mL,即得;
1)稀盐酸取243mL盐酸,加水至1000mL,即得m)氨试液取浓氨溶液400mL,加水使成1000mL,即得。6.5仪器和设备
a)电烘箱;
b)分析天平(万分之一);
c)滴定管(25,50mL)。
6.6操作方法
TKAONLKAC
YY/T0188.7-—1995
取供试品适量,精密称定,精确至0.0001g·按各药品含量测定项下规定方法操作。6.7注意事项
6.7.1酸度对络合反应平衡、金属离子水解,EDTA解离度有影响,为此要调好酸度,并加入适宜的缓冲液,否则将直接影响测定结果。6.7.2金属指示剂为有机染料本身具有颜色。与金属离子络合生成另一种颜色指示终点,但指示剂本身的颜色在不同pH溶液中,有不同颜色故必须按规定控制滴定溶液的pH值。6.7.3当有干扰离子存在时,必须设法排除干扰,否则不能选用本法。6.7.4利用酸度对络合物稳定常数的影响,可调节滴定溶液的pH,有选择的测定共存离子中的某种金属离子。也可加入掩蔽剂或沉淀剂,消除共存离子的干扰。6.7.5滴定速度要适宜,近终点时EDTA液要逐滴加入,并充分振摇,以防终点滴过。6.7.6EDTA滴定液应于具玻璃塞瓶中保存,避免与橡皮塞、橡皮管等接触。6.8结果计算
见3.10。
6.9允许差
本法的相对偏差不得超过0.3%。7重氮化法
7.1定义
以亚硝酸钠为滴定液的容量分析法称为重氮化法(亦称亚硝酸钠法)。7.2原理
芳香伯胺类药物,在盐酸存在下,能定量地与亚硝酸钠产生重氮化反应.依此,用已知浓度的亚硝酸钠液滴定(用永停法指示终点),根据消耗的亚硝酸钠液的浓度和毫升数,可计算出伯胺类药物的含量。反应式:
7.3适用范围
ArNH,+NaNO,+2HCI-[Ar-N+=NJCI-+NaCI+2H,O7.3.1芳香族第一胺类药物。
7.3.2水解后具有芳香第一胺结构的药物。7.3.3还原后具有芳香第一胺结构的药物。7.4试剂和溶液
a)亚硝酸钠液(0.1、0.05mol/L)按药典方法配制、标定、贮藏;b)无水碳酸钠(分析纯);
c)对氨基苯磺酸(基准试剂);
d)氨试液取浓氨溶液400mL,加水使成1000mL,即得;e)盐酸(分析纯)。下载标准就来标准下载网
7.5仪器和设备
a)电烘箱;
b)分析天平(万分之一);
c)永停仪;
d)磁力搅拌器;
e)滴定管(25、50mL),
f)烧杯(200mL)。
7.6操作方法
调节永停仪R(见中国药典附录永停仪装置图),使加于电极上的电压约为50mV。取供试品适量,139
YY/T 0188.7-1995
精密称定,置烧杯中,除另有规定外.可加水40mL与盐酸溶液(1+2)15mL,而后置电磁搅拌器上,搅拌使溶解。再加溴化钾2g,插入铂-铂电极后,将滴定管的尖端插入液面下约2/3处,用亚硝酸钠液(0.1、0.05mo1/L)迅速滴定,随滴随搅拌,至近终点时,将滴定管的尖端提出液面,用小量水淋洗尖端,洗液并入溶液中,继续缓缓滴定,至电流计指针突然偏转,并持续1min不再回复,即为滴定终点。7.7注意事项
7.7.1将滴定管尖端插入液面2/3处进行滴定,是-种快速滴定法。7.7.2重氮化温度应在15~30℃,以防重氮盐分解和亚硝酸逸出。7.7.3重氮化反应须以盐酸为介质,因在盐酸中反应速度快,且芳伯胺的盐酸盐溶解度大。在酸度为1~2mol/L下滴定为宜。
7.7.4近终点时,芳伯胺浓度较稀,反应速度减慢,应缓缓滴定,并不断搅拌。7.7.5永停仪电极易钝化,应常用浓硝酸(加1~2滴三氯化铁试液)温热活化。7.7.6亚硝酸钠液应于棕色玻璃瓶中避光保存。7.8结果计算
见3.10。
7.9允许差
本法的相对偏差不得超过0.3%。8非水溶液滴定法
8.1定义
质子传递反应为基础的在水以外的溶剂中滴定的方法。8.2原理
非水介质中酸碱滴定,主要以质子理论的酸碱概念为基础,凡能放出质子的物质是酸,能接受质子的物质是碱,它们的关系可用下式表示:HZ-A+H+
酸碱质子
在非水溶液中,游离的质子(H+)不能单独存在,而是与溶剂分子结合成溶剂合质子,酸碱中和反应的实质是质子的转移,而质子转移是通过溶剂合质子实现的。溶剂对酸碱的强度影响很大,非水溶液中的酸碱滴定利用这个道理,使原来在水溶液中不能滴定的某些弱酸弱碱,经选择适当溶剂,增强其酸碱性后,便可以进行滴定。8.3适用范围
本法适用于测定有机碱及其氢卤酸盐、磷酸盐、硫酸盐和有机酸盐以及有机酸碱金属盐类药物的含量。也用于测定某些有机弱酸的含盘。8.4仪器和设备
a)自动滴定管(10mL);
b)具塞锥形瓶(50、100.150mL):c)分析天平(万分之一);
d)电位滴定仪。
8.5试剂和溶液
a)高氮酸液(0.1mol/L)按药典方法配制、标定、贮藏;b)甲醇钠液(o.1mol/L)按药典方法配制、标定、贮藏;c)酸性溶剂有机弱碱在酸性溶剂中可显著地增强其相对碱度,最常用的酸性溶剂为冰乙酸(分析纯):
d)碱性溶剂有机弱酸在碱性溶剂中可显著地增强其相对酸度,最常用的碱性溶剂为二甲基甲酰140
YYKAONIKAca
小提示:此标准内容仅展示完整标准里的部分截取内容,若需要完整标准请到上方自行免费下载完整标准文档。
标准图片预览:



- 其它标准
- 热门标准
- YY医药标准
- YY0505-2005 IEC 60601-1-2 :2001 医用电气设备 第1-2部分:安全通用要求并列标准:电磁兼容要求和试验
- YY0117.3-2005 外科植入物 骨关节假体锻、铸件 钴铬钼合金铸件
- YY/T1735-2021 丙型肝炎病毒抗体检测试剂(盒)(化学发光免疫分析法)
- YY/T0280-1995 电热蒸馏水器
- YY0649-2016 电位治疗设备
- YY1080-2009 眼科仪器直接检眼镜
- YY/T1565-2017 外科植入物无损检验铸造金属外科植入物射线照相检验
- YY0622-2008 ISO 6874: 1988 牙科树脂基窝沟封闭剂
- YY/T0095-2004 钨酸钙中速医用增感屏
- YY/T1669-2019 ABO反定型检测卡(柱凝集法)
- YY/T1052-2004 手术器械标志
- YY/T0186~0187-1994 医用中心吸引系统通用技术条件医用中心供氧系统通用技术条件
- YY/T0664-2020 替YY/T 0664-2008 医疗器械软件软件生存周期过程
- YY0450.1-2020 一次性使用无菌血管内导管辅件 第1部分:导引器械
- YY/T0608-2007 医用X射线影像增强器电视系统通用技术条件
- 行业新闻