- 您的位置:
- 标准下载网 >>
- 标准分类 >>
- 医药行业标准(YY) >>
- YY 0325-2016 一次性使用无菌导尿管
标准号:
YY 0325-2016
标准名称:
一次性使用无菌导尿管
标准类别:
医药行业标准(YY)
标准状态:
现行出版语种:
简体中文下载格式:
.zip .pdf下载大小:
22.67 MB
手机扫码下载更方便
点击下载
标准简介:
YY 0325-2016.Sterile urethral catheter for single use.
YY 0325规定了一次性使用无菌导尿管的术语和定义、要求、符号和标志、包装等。
YY 0325适用于一次性使用灭菌有球囊和无球囊导尿管。
2规范性引用文件
下列文件对于本文件的应用是必不可少的。凡是注日期的引用文件,仅注日期的版本适用于本文件。凡是不注日期的引用文件,其最新版本(包括所有的修改单)适用于本文件。
GB/T 1962.1注射器 、注射针和其他医疗器械用6%(鲁尔)圆锥接头第1 部分:一般要求
GB/T 14233.1医用输液 、输血、注射器具检验方法第1 部分:化学分析方法
GB/T 15812.1- -2005非血管内导管 第1部分:一般性能试验方法
GB/T 19633.1最终灭菌医疗器械包装 第 1部分:材料无菌屏障系统和包装系统的要求
YY/T0313医用高分子制品包装和制造商提供信息的要求
YY/T0466.1医疗器械用于医疗器械标签、标记和提供信息的符号第1部分:通用要求
YY/T 0615.1标示“无菌"医疗 器械的要求第1部分:最终灭菌医疗器械的要求
3术语和定义
下列术语和定义适用于本文件。
3.1
导尿管urethral catheter通过尿道插人膀胱腔以排尿和冲洗膀胱为目的的管状器械。
3.2
球囊容积balloon eapacity充人导尿管的充起腔并充起球囊的液体的体积。
3.3
管身shaft导尿管除尖部、球囊.锥口和/或侧孔以外的部分。
3.4
外径outside diameter管身轴向垂直截面上测得的最大尺寸。
3.5
公称球囊容积nominal balloon capacity管身上或包装上标示的球囊额定容积。当以范围的形式标出球囊容积时,以下限作为公称容积。
部分标准内容:
中华人民共和国医药行业标准
YY0325—2016
代替YY0325—2002
一次性使用无菌导尿管
Sterile urethral catheter for single use2016-03-23发布
国家食品药品监督管理总局
2018-01-01实施
本标准的全部技术内容为强制性。前
本标准按照GB/T1.1—2009给出的规则起草。YY0325—2016
本标准代替YY03252002《一次性使用无菌导尿管》。与YY03252005相比,主要技术差异如下:
修改了规范性引用文件(见第2章);增加了术语公称球囊容积(见3.5);“抗扭结”修改为“耐弯曲性”(见4.72002年版4.7);修改了流量的试验方法(见4.8,2002年版4.8);修改了符号和标志的部分内容(见第5章);修改了包装的要求(见第6章)。请注意本文件的某些内容可能涉及专利。本文件的发布机构不承担识别这些专利的责任。本标准由全国医用输液器具标准化技术委员会(SAC/TC106)归口。本标准主要起草单位:山东省医疗器械产品质量检验中心。本标准参加起草单位:广州维力医疗器械股份有限公司,山东福瑞达医疗器械有限公司。本标准主要起草人:万敏、宋金子、王延明、黄开根。本标准首次发布于2002年1月。
1范围
一次性使用无菌导尿管
本标准规定了一次性使用无菌导尿管的术语和定义、要求、符号和标志、包装等。本标准适用于一次性使用灭菌有球囊和无球囊导尿管。2
规范性引用文件
YY0325—2016
下列文件对于本文件的应用是必不可少的。凡是注日期的引用文件,仅注日期的版本适用于本文件。凡是不注日期的引用文件,其最新版本(包括所有的修改单)适用于本文件。GB/T1962.1注射器,注射针和其他医疗器械用6%(鲁尔)圆锥接头第1部分:一般要求GB/T14233.1医用输液、输血、注射器具检验方法第1部分:化学分析方法GB/T15812.1一2005非血管内导管第1部分:一般性能试验方法GB/T19633.1最终灭菌医疗器械包装第1部分:材料,无菌屏障系统和包装系统的要求YY/T0313医用高分子制品包装和制造商提供信息的要求YY/T0466.1
医疗器械用于医疗器械标签,标记和提供信息的符号第1部分:通用要求YY/T0615.1标示“无菌”医疗器械的要求第1部分:最终灭菌医疗器械的要求3术语和定义
下列术语和定义适用于本文件。3.1
导尿管urethral catheter
通过尿道插人膀胱腔以排尿和冲洗膀胱为目的的管状器械。3.2
球囊容积 balloon capacity
充人导尿管的充起腔并充起球囊的液体的体积3.3
管身shaft
导尿管除尖部、球囊、锥口和/或侧孔以外的部分。3.4
外径outside diameter
管身轴向垂直截面上测得的最大尺寸。3.5
公称球囊容积nominalballooncapacity管身上或包装上标示的球囊额定容积。当以范围的形式标出球囊容积时,以下限作为公称容积。3.6
阀valve
控制液体流动的装置。
YY0325—2016
所有试验应在供使用状态下的产品上进行。4.2外观
供使用状态下的导尿管(如,按制造商说明书处理过),当用正常视力或矫正视力在2.5倍放大条件下检验时,管身、尖部、球囊和孔眼应无外来物质,且不应有加工缺陷和表面缺陷、4.3尺寸
4.3.1规格标记
导尿管应用其公称外径(mm)表示其规格,精确到o.1mm。其公差应为士033mm。球囊容积应以毫升(mL)表示。
注:可同时给出其他规格标记。4.3.2长度
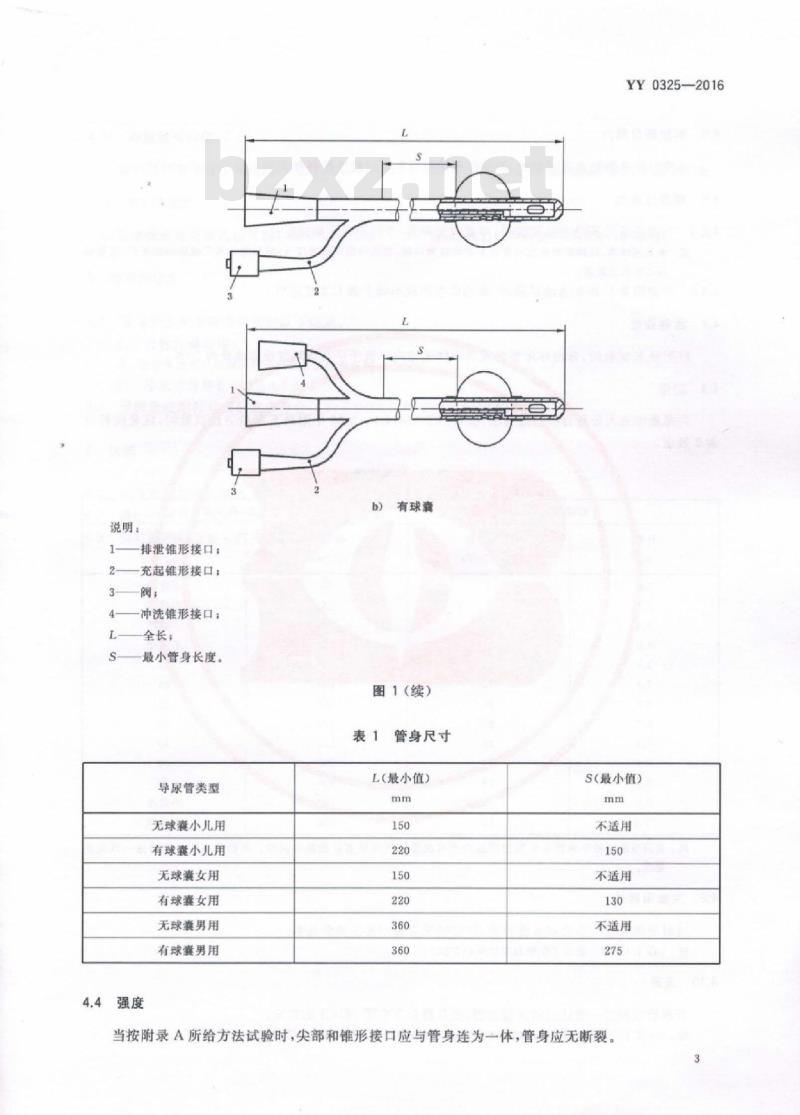
最小全长(L)利最小管身长度(S)应a)无球囊
典型导尿管
说明:
排泄锥形接口:
充起锥形接口:
冲洗锥形接口
全长,
最小管身长度。
导尿管类型
无球囊小儿用
有球囊小儿用
无球囊女用
有球囊女用
无球囊男用
有球囊男用
4.4强度
b)有球囊
图1(续)
管身尺寸
L(最小值)
YY0325—2016
S(最小值)
不适用
不适用
不适用
当按附录A所给方法试验时,尖部和锥形接口应与管身连为一体,管身应无断裂YY0325-2016
连接器分离力
当按附录B所给方法试验时,排泄锥形接口应不与试验连接器分离。4.6
球囊可靠性
当按附录C所给方法试验时,球囊应无泄漏,并且不应影响排泄孔。4.6.1
注,未充起球囊,其两端外形宜与管身平滑地连为一体,在其周围环境温度下,球囊充人水至规定的容积后,宜呈现基本对称地鼓起。
4.6.2当按附录D所给方法试验时,水的回收率应不低于表D.2规定值。4.7www.bzxz.net
耐弯曲性
按附录E试验时,弯曲导尿管各腔的液体流量应不低于平直导尿管液体流量的50%。4.8流量
向球囊中充人公称容积的蒸馏水,按GB/T15812.1—2005中附录E所给方法试验时,流量应符合表2规定。
表2平均流量
标称规格
法国规格
FG/Ch/Fr
排泄腔
mL/min
平均流量(最小值
冲洗腔
mL/min
不适用
不适用
不适用
不造用
不适用
不适用
注:有润滑涂层的导尿管在长期使用过程中有流量降低或堵塞排泄腔的风险。本标准不涉及针对这一风险的要求。
4.9生物相容性
应对导尿管进行生物相容性评价,评价结果应表明无生物学危害。注:GB/T16886.1给出了生物相容性评价方法。4.10无菌
导尿管应经过一确认过的灭菌过程,使其符合YY/T0615.1的规定。注:GB/T14233.2规定了无菌试验方法,但该方法不能用于证实灭菌批的灭菌效果。4
4.11耐腐蚀性试验
YY0325—2016
如导尿管中含有金属器件,则按GB/T15812.1—2005中附录A进行试验时,试样应无腐蚀迹象。4.12EO残留量
导尿管若用环氧乙烷灭菌,按GB/T14233.1检验时,环氧乙烷残留量应不大于10μg/g。5符号和标志
5.1导尿管上至少应清晰给出以下信息:a)公称球囊容积;
注:制造商也可以以范围的形式标示出球囊容积。b)导尿管规格标记(见4.3.1)。2导尿管随附符号或信息应符合YY/T0466.1和YY/T0313的要求。5.2
6包装
制造商应能提供装入导尿管后的包装符合GB/T19633.1要求的证明。6.1
若使用环氧乙烷灭菌,包装应采用透析材料。6.2
包装打开后应留有打开痕迹。
YY0325—2016
A.1原理
附录A
(规范性附录)
测定导尿管强度的试验方法
带球囊导尿管可能长期在原位使用。因此,对有球囊导尿管,试验前先将导尿管浸人模拟尿液中14d。对无球囊导尿管,可省略这一步骤。向导尿管的尖部与管身间的连接处施加一拉力。对于有侧孔眼的导尿管,拉力施加于孔眼上:对无侧孔眼的导尿管,拉力施加于管身和排泄锥形接口之间。卸下拉力后,检查导尿管受破坏迹象。A.2试剂
A.2.1模拟尿液可采用以下两个配方中的任意一个:a)模拟尿液由以下成分组成(pH约为6.6),试剂为分析纯试剂:尿素
氯化钠
无水磷酸氢二钠
氯化铵
无水磷酸二氢钾
肌氨酸酐
亚硫酸钠,无水
蒸馅水
定容至1.0L
警告:该溶液有助于微生物生长,在A.3和C.3所述试验结束时,很可能有大量的微生物存在。这些试验应由经过培训的人员进行,在对浸泡后的导尿管进行操作以及弃去污染的溶液时,应采取相应的预防措施。
b)模拟尿液由以下成分组成(pH约为5.5~7.0),试剂为分析纯试剂:氯化钠
磷酸二氢钠
柠檬酸钠
硫酸镁
硫酸钠
氯化钾
氯化钙
草酸钠
蒸馏水
定容至1.0L
注:用1mol/L的氢氧化铵(NH.OH)或1mol/L的氯化铵(NH,CID)溶液调节pH在5.5~7.0范围内。A.3仪器
A.3.1·有侧孔眼导尿管的悬挂装置,其上有一能穿过导尿管排泄孔眼的销子,销子直径在供试导尿管6
排泄腔内径的50%~70%之间。图A.1a)示出了适宜装置的示例。对没有侧孔眼的导尿管,其管身夹于适宜的夹具上。YY0325—2016
A.3.2砖码与排泄腔的连接装置,对于外径大于3.3mm的导尿管,连接装置与码的总质量为1kg对于外径小于或等于3.3mm的导尿管,连接装置与码的总质量为0.7kg。A.3.3水浴,或其他能将温度控制在(37士2)℃的装置。A.3.4计时器。
A.4步骤
将导尿管浸人新制备的模拟尿液(A.2.1)中,并置于水浴中(A.3.3),控制在(37土2)℃,使球囊和管身全部浸没。
导尿管在模拟尿液中浸泡14d后取出,用自来水冲洗并使其干燥,将导尿管处于(23士2)C温度条件下。
将悬挂装置(A.3.1)上的销子穿过导尿管尖部处的排泄孔眼,将其悬挂(见图A.1);对无侧孔眼的导尿管,则用一适宜的夹具将其悬挂。手持码(A.3.2),接于导尿管的排泄锥形接口上,轻轻向下放码,直至其自由悬挂于导尿管上保持1min
取下码,检验导尿管所有连接处的分离和损坏以及孔眼撕裂现象。A.5试验报告
试验报告应包括以下信息:
a)导尿管的识别;
b)试验后尖部与管身的连接和孔眼的状况。注1:销子直径D在供试导尿管排泄腔内径的50%~注2:尺寸P应足以使销子部顶到导尿管的尖部,当加载70%之间。
a)悬挂装置和销子示例
时,不应使支撑部件与孔眼边缘相接触。b)销子插入导尿管孔眼
图A.1导尿管强度试验的装置和试验布置YY0325—2016
说明:
一充起锥形接口;
排泄锥形接口:
试验力的方向。
e)试验布置
图A.1(续)
B.1原理
附录B
(规范性附录)
测定排泄锥形接口装配分离力的试验方法YY0325—2016
将规定的试验连接器与导尿管的排泄锥形接口连接,施加一轴向拉力,检验其连接处是否分离。B.2仪器
试验连接器,刚性材料制造,其尺寸如图B.1a)所示。B.2.1
夹具或类似装置,供悬挂导尿管。B.2.3砖码试验连接器的连接装置,对于规格小于或等于3.3mm的导尿管,连接装置与码的总质量为0.75kg;对于规格大于3.3mm的导尿管,连接装置与码的总质量为1kg。B.2.4计时器。
B.3步骤
试验在(23士2)℃下进行。
使导尿管的排泄锥形接口和连接器(B.2.1)清洁干燥。将连接器插于排泄锥形接口,插入深度为10mm以上(即达到或超过连接器上的标线)。从排泄锥形接口与管身间的连接处附近选取一点,用夹具(B.2.2)夹持,将导尿管悬挂[见图B.1b)。
手持码(B.2.3),接于导尿管的排泄锥形接口上,轻轻向下放码,直至其悬挂于导尿管上,保持1min并进行观察。
记录试验连接器是否与锥形接口分离。B.4试验报告
试验报告应包括以下信息:
a)导尿管的识别;
b)试验期间试验连接器是否与锥形接口分离。9
YY0325-2016
说明:
50±10
a)试验连接器
环形标记:
公称罐度20%(1:5)
悬挂导尿管的夹具;
冲洗维形接口,
排泄锥形接口;
充起锥形接口:
试验连接器:
试验力方向。
14.0±0.2
试验一般布置
图B.1试验连接器与排泄锥形接口装配分离力的试验布置单位为毫米
小提示:此标准内容仅展示完整标准里的部分截取内容,若需要完整标准请到上方自行免费下载完整标准文档。
标准图片预览:




- 热门标准
- YY医药标准
- YY0505-2005 IEC 60601-1-2 :2001 医用电气设备 第1-2部分:安全通用要求并列标准:电磁兼容要求和试验
- YY0117.3-2005 外科植入物 骨关节假体锻、铸件 钴铬钼合金铸件
- YY1080-2009 眼科仪器直接检眼镜
- YY/T1735-2021 丙型肝炎病毒抗体检测试剂(盒)(化学发光免疫分析法)
- YY/T0280-1995 电热蒸馏水器
- YY/T1669-2019 ABO反定型检测卡(柱凝集法)
- YY0649-2016 电位治疗设备
- YY/T1565-2017 外科植入物无损检验铸造金属外科植入物射线照相检验
- YY/T1052-2004 手术器械标志
- YY/T0095-2004 钨酸钙中速医用增感屏
- YY/T0186~0187-1994 医用中心吸引系统通用技术条件医用中心供氧系统通用技术条件
- YY0622-2008 ISO 6874: 1988 牙科树脂基窝沟封闭剂
- YY/T0664-2020 替YY/T 0664-2008 医疗器械软件软件生存周期过程
- YY/T1670.1-2019 医疗器械神经毒性评价 第1部分:评价潜在神经毒性的试验选择指南
- YY/T0608-2007 医用X射线影像增强器电视系统通用技术条件
- 行业新闻