- 您的位置:
- 标准下载网 >>
- 标准分类 >>
- 国家标准(GB) >>
- GB 4789.43-2016 食品安全国家标准 食品微生物学检验 微生物源酶制剂抗菌活性的测定
标准号:
GB 4789.43-2016
标准名称:
食品安全国家标准 食品微生物学检验 微生物源酶制剂抗菌活性的测定
标准类别:
国家标准(GB)
标准状态:
现行出版语种:
简体中文下载格式:
.rar .pdf下载大小:
点击下载
标准简介:
标准下载解压密码:www.bzxz.net
GB 4789.43-2016 食品安全国家标准 食品微生物学检验 微生物源酶制剂抗菌活性的测定 GB4789.43-2016
部分标准内容:
中华人民共和国国家标准
GB4789.43—2016
食品安全国家标准
食品微生物学检验
微生物源酶制剂抗菌活性的测定2016-12-23发布
2017-06-23实施
中华人民共和国国家卫生和计划生育委员会国家食品药品监督管理总局
1范围
食品安全国家标准
食品微生物学检验
微生物源酶制剂抗菌活性的测定本标准规定了微生物源酶制剂抗菌活性的测定方法。本标准适用于用微生物生产的酶制剂抗菌活性的测定2设备和材料
除微生物实验室常规灭菌及培养设备外,其他设备和材料如下:2.1
生物安全柜。
冰箱:2℃~5℃。
恒温培养箱:36℃士1℃。
恒温水浴箱:46℃土1℃。
天平:感量为0.1g。
振荡器。
GB 4789.43—2016
无菌吸管:1mL(具0.01mL刻度)、10mL(具0.1mL刻度)或微量移液器及吸头。无菌培养血:直径90mm。
无菌锥形瓶:容量250mL、500mL。pH计或精密pH试纸。
无菌纸片:见A.8。
无菌镊子。
游标卡尺:刻度为0.1mm。
培养基和试剂
胰蛋白陈大豆琼脂(TryptoneSoyAgar,TSA):见A.1。胰蛋白陈大豆肉汤(TryptoneSoyBroth,TSB):见A.2。平板计数琼脂(PlateCountAgar):见A.3。0.1mol/L HCl:见A.4。
无菌生理盐水:见A.5。
50.0μg/mL环丙沙星(Ciprofloxacin,CIP)溶液:见A.6。5.0ug/片环丙沙星纸片:见A.7。试验菌株
金黄色葡萄球菌(Staphylococcusaureus)ATCC65381
大肠埃希氏菌(Escherichiacoli)ATCC11229。蜡样芽胞杆菌(Bacilluscereus)ATCC2。环状芽孢杆菌(Bacilluscirculans)ATCC4516。化脓性链球菌(Streptococcuspyogenes)ATCc12344。粘质沙雷菌(Serratiamarcescens)ATCC14041。检验程序
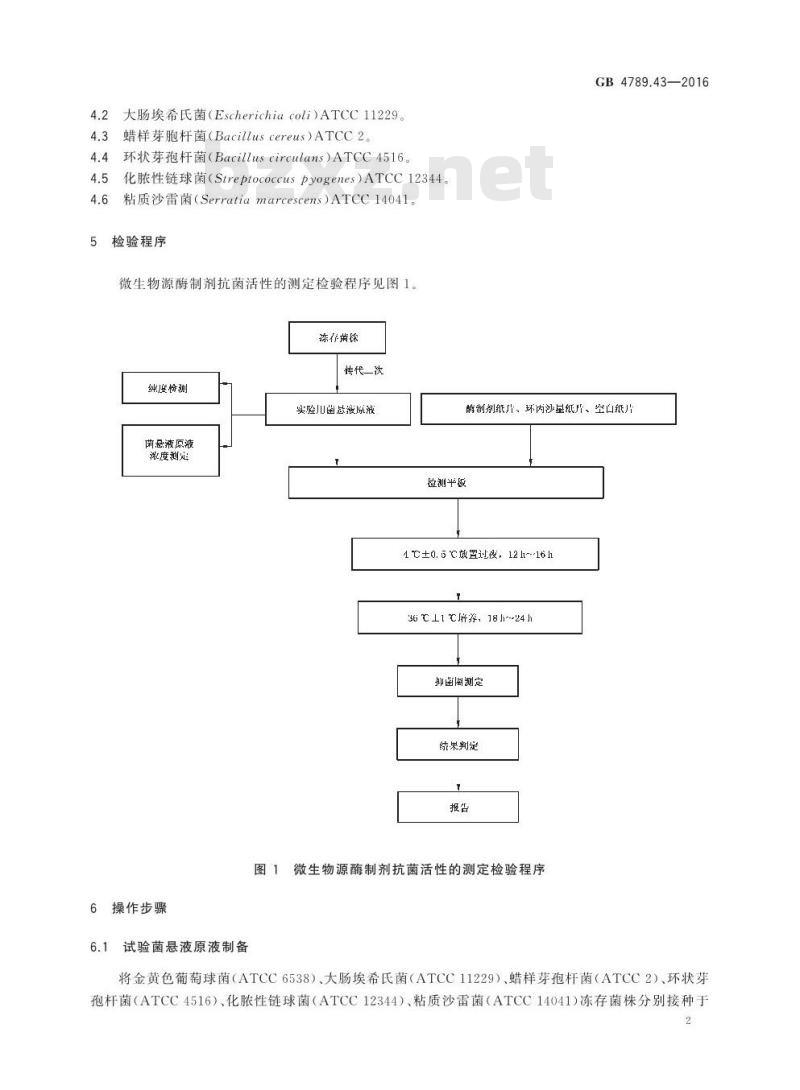
微生物源酶制剂抗菌活性的测定检验程序见图1。冻存菌琛
传代二次
继度份测
实验川菌总液原激
菌岛液原液
浓度测
GB4789.432016
酶制剂纸片、环丙沙星纸片、空白纸片位测半版
4±0.5放置过夜,12h16h
36 ℃11 胖券,18 h24 h
续果判定
图1微生物源酶制剂抗菌活性的测定检验程序6操作步骤
6.1试验菌悬液原液制备
将金黄色葡萄球菌(ATCC6538)、大肠埃希氏菌(ATCC11229)、蜡样芽孢杆菌(ATCC2)、环状芽孢杆菌(ATCC4516)、化脓性链球菌(ATCC12344)、粘质沙雷菌(ATCC14041)冻存菌株分别接种于2
GB4789.43—2016
盛有5mLTSB的试管,置36℃土1℃培养18h~24h进行第一次传代培养,分别挑取第一次传代培养液1~2环转种于5mLTSB肉汤,置36℃士1℃培养18h~24h进行二次传代培养,作为试验菌悬液原液备用。
试验菌悬液原液纯度检测:分别挑取试验菌悬液原液各一环,划线接种于TSA平板,36℃王1℃培养20h~24h,观察纯度。
6.2菌悬液原液浓度测定
6.2.1菌悬液原液稀释
分别取6.1中制备的菌悬液原液依次进行十倍梯度稀释,蜡样芽孢杆菌和环状芽孢杆菌分别制成10-4稀释液,金黄色葡萄球菌、大肠埃希氏菌、化脓性链球菌、粘质沙雷菌分别制成10-\稀释液6.2.2培养计数
分别吸取6.2.1中制备好的各菌稀释液1mL于无菌平皿内,每个稀释度做两个平行,并用无菌牛理盐水作空白对照。向平皿中倾注冷却至46℃左右(可放置于46℃士1℃的恒温水浴箱中保温)的平板计数琼脂15mL~20mL,并转动平血使其混合均匀。待琼脂凝固后,将平板翻转,于36℃土1℃培养24h后计数,各菌悬液原液中菌浓度均大于10°CFU/mL时方可使用、6.3检测平板制备
倾注融化并冷却至46℃土1℃的TSA培养基15mL于无菌培养内,待其凝固后制成TSA平板,备用
将6.1中二次传代后的各菌培养物分别用冷却至46℃士1℃的TSA培养基按1:10的比例稀释(其中化脓性链球菌ATCC12344按1:20的比例稀释),充分混勾后各取10mL至上述已制备好、于46℃土1℃中保温的TSA平板内,轻轻摇动平板使菌液均匀铺平,待其凝固后制成检测平板,备用。注:为防止含菌培养基遇到TSA后马上凝固,引起菌悬液铺板不均勾,菌悬液铺板前应事先将TSA平板置于46℃土1℃条件下保温平衡10min。
6.4酶制剂纸片的制备
准确称(移)取1.0g(mL)酶制剂于9mL无菌生理盐水中,充分混匀后制成10%的酶制剂溶液。将无菌纸片放人无菌平Ⅲ内.在每张纸片上缓缓滴加100μL10%的酶制剂溶液,使其全部吸收,每种酶制剂样品制备12张纸片。
6.5贴纸片及培养
将6.4中制备的含待测酶制剂的纸片、含环丙沙星的阳性对照纸片(见A.7)和含100μL无菌生理盐水的空白阴性对照纸片用无菌镊子分别置6.3中制备的检测平板上,每个平板贴2张纸片(2张含待测酶制剂的纸片或2张含环丙沙星的纸片或2张空白纸片),两纸片圆点的间距大于32mm,每个标准菌株分别设一阳性对照和一阴性对照平板。将平板正置于4℃土0.5℃冰箱内过夜(12h~16h)。第二天转人36℃王1℃C恒温培养箱中培养24h后,测定酶制剂样品、环内沙星和阴性对照纸片形成的抑菌圈。
7抗菌活性结果报告
7.1结果判定
若待测酶制剂对3种或3种以上受试微生物呈现出抗菌活性,即纸片周围出现清晰可见的抑菌圈3
GB 4789.43—2016
(每个抑菌圈直径≥16mm),且阳性对照环丙沙星纸片对金黄色葡萄球菌、蜡样芽孢杆菌、粘质沙雷菌、环状芽孢杆菌、化脓性链球菌5种细菌形成的抑菌圈均>16mm,则判定该酶制剂样品中存在抗菌活性物质。
结果报告
报告样品中检出抗菌活性或未检出抗菌活性4
附录A
培养基与试剂
胰蛋白陈大豆琼脂(TryptoneSoyAgar,TSA)成分
胰蛋白陈
大豆蛋白陈
氯化钠
琼脂粉
蒸馏水
1000mL
GB4789.43—2016
将上述各成分加于蒸馏水中,煮沸溶解,调节pH至7.2士0.2,分装至锥形瓶中,121℃灭菌15min。A.2
胰蛋白陈大豆肉汤(TryptoneSoyBroth,TSB)成分
胰蛋白陈
大豆蛋白陈
氯化钠
蒸馏水
1000mL
将上述各成分加于蒸馏水中,煮沸溶解,调节pH至7.2士0.2.分装试管,121℃灭菌15min。平板计数琼脂(PlateCountAgar,PCA)A.3
胰蛋白陈
酵母浸膏
葡萄糖
蒸馏水
1000mL
上述各成分加于蒸馏水中,煮沸溶解,调节pH至7.2土0.2分装至锥形瓶中,121℃灭菌15min5
A.40.1mol/LHCI
蒸馏水
GB4789.43—2016
移取浓盐酸9mL(质量浓度为36%,密度为1.17g/m*).用无菌蒸馏水稀释至1000mL,0.22um微孔滤膜过滤除菌后备用,
无菌生理盐水
氯化钠
蒸馏水
2制法
1000ml
称取8.5g氯化钠溶于1000mL蒸馏水,121℃灭菌15min。A.650.0μg/mL环丙沙星(Ciprofloxacin,CIP)A.6.1成分
1000μg/mL环丙沙星
无菌生理盐水
按产品说明书(百分比,含水量或效价)称取一定质量的环丙沙星用适量0.1mol/LHCI溶解使其浓度为1000μg/mL,无菌条件下0.22um微孔滤膜过滤后移取0.5mL用无菌生理盐水稀释至10mL,混匀。
5.0μg/片环丙沙星纸片(Ciprofloxacinpaper,CIPpaper)A.7
1成分
50.0μg/ml.环丙沙星
无菌纸片
2制法
100μL
吸取50.0μg/mL环丙沙星溶液100μL缓慢均匀滴加于无菌纸片上,制成5.0μg/片环丙沙星纸片。
A.8无菌纸片
1要求
GB4789.43—2016
纸片外观应整洁、无毛边,无明显变形,无破损,pH为中性,厚度0.3mm0.6mm,60s内吸收100μL蒸馏水。
制备及储存方法免费标准下载网bzxz
制成标准直径为13.0mm士0.1mm的圆形纸片,置玻璃容器内,密封,121℃灭菌15min后,80℃±5℃干燥4h,备用。
小提示:此标准内容仅展示完整标准里的部分截取内容,若需要完整标准请到上方自行免费下载完整标准文档。
GB4789.43—2016
食品安全国家标准
食品微生物学检验
微生物源酶制剂抗菌活性的测定2016-12-23发布
2017-06-23实施
中华人民共和国国家卫生和计划生育委员会国家食品药品监督管理总局
1范围
食品安全国家标准
食品微生物学检验
微生物源酶制剂抗菌活性的测定本标准规定了微生物源酶制剂抗菌活性的测定方法。本标准适用于用微生物生产的酶制剂抗菌活性的测定2设备和材料
除微生物实验室常规灭菌及培养设备外,其他设备和材料如下:2.1
生物安全柜。
冰箱:2℃~5℃。
恒温培养箱:36℃士1℃。
恒温水浴箱:46℃土1℃。
天平:感量为0.1g。
振荡器。
GB 4789.43—2016
无菌吸管:1mL(具0.01mL刻度)、10mL(具0.1mL刻度)或微量移液器及吸头。无菌培养血:直径90mm。
无菌锥形瓶:容量250mL、500mL。pH计或精密pH试纸。
无菌纸片:见A.8。
无菌镊子。
游标卡尺:刻度为0.1mm。
培养基和试剂
胰蛋白陈大豆琼脂(TryptoneSoyAgar,TSA):见A.1。胰蛋白陈大豆肉汤(TryptoneSoyBroth,TSB):见A.2。平板计数琼脂(PlateCountAgar):见A.3。0.1mol/L HCl:见A.4。
无菌生理盐水:见A.5。
50.0μg/mL环丙沙星(Ciprofloxacin,CIP)溶液:见A.6。5.0ug/片环丙沙星纸片:见A.7。试验菌株
金黄色葡萄球菌(Staphylococcusaureus)ATCC65381
大肠埃希氏菌(Escherichiacoli)ATCC11229。蜡样芽胞杆菌(Bacilluscereus)ATCC2。环状芽孢杆菌(Bacilluscirculans)ATCC4516。化脓性链球菌(Streptococcuspyogenes)ATCc12344。粘质沙雷菌(Serratiamarcescens)ATCC14041。检验程序
微生物源酶制剂抗菌活性的测定检验程序见图1。冻存菌琛
传代二次
继度份测
实验川菌总液原激
菌岛液原液
浓度测
GB4789.432016
酶制剂纸片、环丙沙星纸片、空白纸片位测半版
4±0.5放置过夜,12h16h
36 ℃11 胖券,18 h24 h
续果判定
图1微生物源酶制剂抗菌活性的测定检验程序6操作步骤
6.1试验菌悬液原液制备
将金黄色葡萄球菌(ATCC6538)、大肠埃希氏菌(ATCC11229)、蜡样芽孢杆菌(ATCC2)、环状芽孢杆菌(ATCC4516)、化脓性链球菌(ATCC12344)、粘质沙雷菌(ATCC14041)冻存菌株分别接种于2
GB4789.43—2016
盛有5mLTSB的试管,置36℃土1℃培养18h~24h进行第一次传代培养,分别挑取第一次传代培养液1~2环转种于5mLTSB肉汤,置36℃士1℃培养18h~24h进行二次传代培养,作为试验菌悬液原液备用。
试验菌悬液原液纯度检测:分别挑取试验菌悬液原液各一环,划线接种于TSA平板,36℃王1℃培养20h~24h,观察纯度。
6.2菌悬液原液浓度测定
6.2.1菌悬液原液稀释
分别取6.1中制备的菌悬液原液依次进行十倍梯度稀释,蜡样芽孢杆菌和环状芽孢杆菌分别制成10-4稀释液,金黄色葡萄球菌、大肠埃希氏菌、化脓性链球菌、粘质沙雷菌分别制成10-\稀释液6.2.2培养计数
分别吸取6.2.1中制备好的各菌稀释液1mL于无菌平皿内,每个稀释度做两个平行,并用无菌牛理盐水作空白对照。向平皿中倾注冷却至46℃左右(可放置于46℃士1℃的恒温水浴箱中保温)的平板计数琼脂15mL~20mL,并转动平血使其混合均匀。待琼脂凝固后,将平板翻转,于36℃土1℃培养24h后计数,各菌悬液原液中菌浓度均大于10°CFU/mL时方可使用、6.3检测平板制备
倾注融化并冷却至46℃土1℃的TSA培养基15mL于无菌培养内,待其凝固后制成TSA平板,备用
将6.1中二次传代后的各菌培养物分别用冷却至46℃士1℃的TSA培养基按1:10的比例稀释(其中化脓性链球菌ATCC12344按1:20的比例稀释),充分混勾后各取10mL至上述已制备好、于46℃土1℃中保温的TSA平板内,轻轻摇动平板使菌液均匀铺平,待其凝固后制成检测平板,备用。注:为防止含菌培养基遇到TSA后马上凝固,引起菌悬液铺板不均勾,菌悬液铺板前应事先将TSA平板置于46℃土1℃条件下保温平衡10min。
6.4酶制剂纸片的制备
准确称(移)取1.0g(mL)酶制剂于9mL无菌生理盐水中,充分混匀后制成10%的酶制剂溶液。将无菌纸片放人无菌平Ⅲ内.在每张纸片上缓缓滴加100μL10%的酶制剂溶液,使其全部吸收,每种酶制剂样品制备12张纸片。
6.5贴纸片及培养
将6.4中制备的含待测酶制剂的纸片、含环丙沙星的阳性对照纸片(见A.7)和含100μL无菌生理盐水的空白阴性对照纸片用无菌镊子分别置6.3中制备的检测平板上,每个平板贴2张纸片(2张含待测酶制剂的纸片或2张含环丙沙星的纸片或2张空白纸片),两纸片圆点的间距大于32mm,每个标准菌株分别设一阳性对照和一阴性对照平板。将平板正置于4℃土0.5℃冰箱内过夜(12h~16h)。第二天转人36℃王1℃C恒温培养箱中培养24h后,测定酶制剂样品、环内沙星和阴性对照纸片形成的抑菌圈。
7抗菌活性结果报告
7.1结果判定
若待测酶制剂对3种或3种以上受试微生物呈现出抗菌活性,即纸片周围出现清晰可见的抑菌圈3
GB 4789.43—2016
(每个抑菌圈直径≥16mm),且阳性对照环丙沙星纸片对金黄色葡萄球菌、蜡样芽孢杆菌、粘质沙雷菌、环状芽孢杆菌、化脓性链球菌5种细菌形成的抑菌圈均>16mm,则判定该酶制剂样品中存在抗菌活性物质。
结果报告
报告样品中检出抗菌活性或未检出抗菌活性4
附录A
培养基与试剂
胰蛋白陈大豆琼脂(TryptoneSoyAgar,TSA)成分
胰蛋白陈
大豆蛋白陈
氯化钠
琼脂粉
蒸馏水
1000mL
GB4789.43—2016
将上述各成分加于蒸馏水中,煮沸溶解,调节pH至7.2士0.2,分装至锥形瓶中,121℃灭菌15min。A.2
胰蛋白陈大豆肉汤(TryptoneSoyBroth,TSB)成分
胰蛋白陈
大豆蛋白陈
氯化钠
蒸馏水
1000mL
将上述各成分加于蒸馏水中,煮沸溶解,调节pH至7.2士0.2.分装试管,121℃灭菌15min。平板计数琼脂(PlateCountAgar,PCA)A.3
胰蛋白陈
酵母浸膏
葡萄糖
蒸馏水
1000mL
上述各成分加于蒸馏水中,煮沸溶解,调节pH至7.2土0.2分装至锥形瓶中,121℃灭菌15min5
A.40.1mol/LHCI
蒸馏水
GB4789.43—2016
移取浓盐酸9mL(质量浓度为36%,密度为1.17g/m*).用无菌蒸馏水稀释至1000mL,0.22um微孔滤膜过滤除菌后备用,
无菌生理盐水
氯化钠
蒸馏水
2制法
1000ml
称取8.5g氯化钠溶于1000mL蒸馏水,121℃灭菌15min。A.650.0μg/mL环丙沙星(Ciprofloxacin,CIP)A.6.1成分
1000μg/mL环丙沙星
无菌生理盐水
按产品说明书(百分比,含水量或效价)称取一定质量的环丙沙星用适量0.1mol/LHCI溶解使其浓度为1000μg/mL,无菌条件下0.22um微孔滤膜过滤后移取0.5mL用无菌生理盐水稀释至10mL,混匀。
5.0μg/片环丙沙星纸片(Ciprofloxacinpaper,CIPpaper)A.7
1成分
50.0μg/ml.环丙沙星
无菌纸片
2制法
100μL
吸取50.0μg/mL环丙沙星溶液100μL缓慢均匀滴加于无菌纸片上,制成5.0μg/片环丙沙星纸片。
A.8无菌纸片
1要求
GB4789.43—2016
纸片外观应整洁、无毛边,无明显变形,无破损,pH为中性,厚度0.3mm0.6mm,60s内吸收100μL蒸馏水。
制备及储存方法免费标准下载网bzxz
制成标准直径为13.0mm士0.1mm的圆形纸片,置玻璃容器内,密封,121℃灭菌15min后,80℃±5℃干燥4h,备用。
小提示:此标准内容仅展示完整标准里的部分截取内容,若需要完整标准请到上方自行免费下载完整标准文档。
标准图片预览:




- 热门标准
- 国家标准
- GB/T228.1-2021 金属材料 拉伸试验 第1部分:室温试验方法
- GB/T7534-1987 工业用挥发性有机液体沸程的测定
- GB/T4100-2015 陶瓷砖
- GB/T3836.1-2021 爆炸性环境 第1部分:设备 通用要求
- GB/T50772-2012 木结构工程施工规范
- GB/T10125-2021 人造气氛腐蚀试验 盐雾试验
- GB/T30835-2014 锂离子电池用炭复合磷酸铁锂正极材料
- GB5226.1-2019 机械电气安全 机械电气设备 第1部分:通用技术条件
- GB50666-2011 混凝土结构工程施工规范
- GB/T15449-1995 管壳额定开关用场效应晶体管空白详细规范
- GB/T18204.4-2000 公共场所毛巾、床上卧具微生物检验方法细菌总数测定
- GB8552-1987 电子器件详细规范 低功率非线绕固定电阻器 RJ13型金属膜固定电阻器评定水平E(可供认证用)
- GB/T11379-2008 金属覆盖层 工程用铬电镀层
- GB/T23892.3-2009 滑动轴承 稳态条件下流体动压可倾瓦块止推轴承 第3部分:可倾瓦块止推轴承计算的许用值
- GB50303-2015 建筑电气工程施工质量验收规范
- 行业新闻
请牢记:“bzxz.net”即是“标准下载”四个汉字汉语拼音首字母与国际顶级域名“.net”的组合。 ©2025 标准下载网 www.bzxz.net 本站邮件:bzxznet@163.com
网站备案号:湘ICP备2025141790号-2
网站备案号:湘ICP备2025141790号-2