- 您的位置:
- 标准下载网 >>
- 标准分类 >>
- 国家标准(GB) >>
- GB 500933-2010 食品安全国家标准 食品中亚硝酸盐与硝酸盐的测定
标准号:
GB 500933-2010
标准名称:
食品安全国家标准 食品中亚硝酸盐与硝酸盐的测定
标准类别:
国家标准(GB)
标准状态:
现行出版语种:
简体中文下载格式:
.rar .pdf下载大小:
手机扫码下载更方便
部分标准内容:
中华人民共和国国家标准
GB5009.33—2010
食品安全国家标准
食品中亚硝酸盐与硝酸盐的测定Nationalfoodsafetystandard
Determinationof nitriteandnitrateinfoods2010-03-26发布
中华人民共和国卫生部
2010-06-01实施
本标准代替GB/T5009.33-2008
《食品中亚硝酸盐与硝酸盐的测定》。本标准与GB/T5009.33-2008相比,主要变化如下:-第一法中增加粉状婴幼儿配方食品的淋洗条件:GB5009.33—2010
-删除第三法示波极谱法,增加“乳及乳制品中亚硝酸盐与硝酸盐的测定”作为第三法。本标准所代替标准的历次版本发布情况为:GB5009.33-1985、GB/T5009.33-1996、GB/T5009.33-2003、GB/T5009.33-20081范围
食品安全国家标准
食品中亚硝酸盐与硝酸盐的测定本标准规定了食品中亚硝酸盐和硝酸盐的测定方法。本标准适用于食品中亚硝酸盐和硝酸盐的测定。第一法离子色谱法
2原理
GB5009.33—2010
试样经沉淀蛋白质、除去脂肪后,采用相应的方法提取和净化,以氢氧化钾溶液为淋洗液,阴离子交换柱分离,电导检测器检测。以保留时间定性,外标法定量。3试剂和材料
3.1超纯水:电阻率>18.2M2.cm。3.2乙酸(CH;COOH):分析纯。
3.3氢氧化钾(KOH):分析纯。
3.4乙酸溶液(3%):量取乙酸(3.2)3mL于100mL容量瓶中,以水稀释至刻度,混匀。3.5亚硝酸根离子(NO2)标准溶液(100mg/L,水基体)。3.6硝酸根离子(NO3)标准溶液(1000mg/L,水基体)。3.7亚硝酸盐(以NO2计,下同)和硝酸盐(以NO3计,下同)混合标准使用液:准确移取亚硝酸根离子(NO2)和硝酸根离子(NO3)的标准溶液各1.0mL于100mL容量瓶中,用水稀释至刻度,此溶液每1L含亚硝酸根离子1.0mg和硝酸根离子10.0mg4
仪器和设备
4.1离子色谱仪:包括电导检测器,配有抑制器,高容量阴离子交换柱,50μL定量环4.2食物粉碎机。
4.3超声波清洗器。
4.4天平:感量为0.1mg和1mg
4.5离心机:转速≥10000转/分钟,配5mL或10mL离心管。4.60.22μm水性滤膜针头滤器。4.7净化柱:包括Ci8柱、Ag柱和Na柱或等效柱。4.8注射器:1.0mL和2.5mL
GB5009.332010
注:所有玻璃器皿使用前均需依次用2mol/L氢氧化钾和水分别浸泡4h,然后用水冲洗3次~5次,晾干备用。5分析步骤
5.1试样预处理
5.1.1新鲜蔬菜、水果:将试样用去离子水洗净,晾干后,取可食部切碎混匀。将切碎的样品用四分法取适量,用食物粉碎机制成匀浆备用。如需加水应记录加水量5.1.2肉类、蛋、水产及其制品:用四分法取适量或取全部,用食物粉碎机制成匀浆备用。5.1.3乳粉、豆奶粉、婴儿配方粉等固态乳制品(不包括干酪):将试样装入能够容纳2倍试样体积的带盖容器中,通过反复摇晃和颠倒容器使样品充分混匀直到使试样均一化。5.1.4发酵乳、乳、炼乳及其他液体乳制品:通过搅拌或反复摇晃和颠倒容器使试样充分混匀。5.1.5干酪:取适量的样品研磨成均匀的泥浆状。为避免水分损失,研磨过程中应避免产生过多的热量。
5.2提取
5.2.1水果、蔬菜、鱼类、肉类、蛋类及其制品等:称取试样勾浆5g(精确至0.01g,可适当调整试样的取样量,以下相同),以80mL水洗入100mL容量瓶中,超声提取30min,每隔5min振摇一次,保持固相完全分散。于75℃水浴中放置5min,取出放置至室温,加水稀释至刻度。溶液经滤纸过滤后,取部分溶液于10000转/分钟离心15min,上清液备用。5.2.2腌鱼类、腌肉类及其它腌制品:称取试样匀浆2g(精确至0.01g),以80mL水洗入100mL容量瓶中,超声提取30min,每5min振摇一次,保持固相完全分散。于75℃水浴中放置5min,取出放置至室温,加水稀释至刻度。溶液经滤纸过滤后,取部分溶液于10000转/分钟离心15min,上清液备用。
5.2.3乳:称取试样10g(精确至0.01g),置于100mL容量瓶中,加水80mL,摇匀,超声30min加入3%乙酸溶液2mL,于4℃放置20min,取出放置至室温,加水稀释至刻度。溶液经滤纸过滤,取上清液备用。
5.2.4乳粉:称取试样2.5g(精确至0.01g),置于100mL容量瓶中,加水80mL,摇匀,超声30min,加入3%乙酸溶液2mL,于4℃放置20min,取出放置至室温,加水稀释至刻度。溶液经滤纸过滤,取上清液备用。
5.2.5取上述备用的上清液约15mL,通过0.22μum水性滤膜针头滤器、C18柱,弃去前面3mL(如果氯离子大于100mg/L,则需要依次通过针头滤器、C18柱、Ag柱和Na柱,弃去前面7mL),收集后面洗脱液待测。
固相萃取柱使用前需进行活化,如使用OnGuardIIRP柱(1.0mL)、OnGuardⅡIAg柱(1.0mL和OnGuardIINa柱(1.0mL),其活化过程为:OnGuardIRP柱(1.0mL)使用前依次用10mL甲醇、15mL水通过,静置活化30min。OnGuardIIAg柱(1.0mL)和OnGuardIINa柱(1.0mL)用10「给出这一信息是为了方便本标准的使用者,并不表示对该产品的认可,如果其他等效产品具有相同的效果,则可使用这些等效的产品。
mL水通过,静置活化30min。
5.3参考色谱条件
GB5009.33—2010
5.3.1色谱柱:氢氧化物选择性,可兼容梯度洗脱的高容量阴离子交换柱,如DionexIonPacAS11-HC4mm×250mm(带IonPacAG11-HC型保护柱4mmx50mm)1,或性能相当的离子色谱柱。5.3.2淋洗液
5.3.2.1一般试样:氢氧化钾溶液,浓度为6mmol/L~70mmol/L;洗脱梯度为6mmol/L30min,70mmol/L5min,6mmol/L5min;流速1.0mL/min。5.3.2.2粉状婴幼儿配方食品:氢氧化钾溶液,浓度为5mmol/L~50mmol/L;洗脱梯度为5mmol/L33min,50mmol/L5min,5mmol/L5min:流速1.3mL/min。5.3.3抑制器:连续自动再生膜阴离子抑制器或等效抑制装置。5.3.4检测器:电导检测器,检测池温度为35℃。5.3.5进样体积:50uL(可根据试样中被测离子含量进行调整)。5.4测定
5.4.1标准曲线
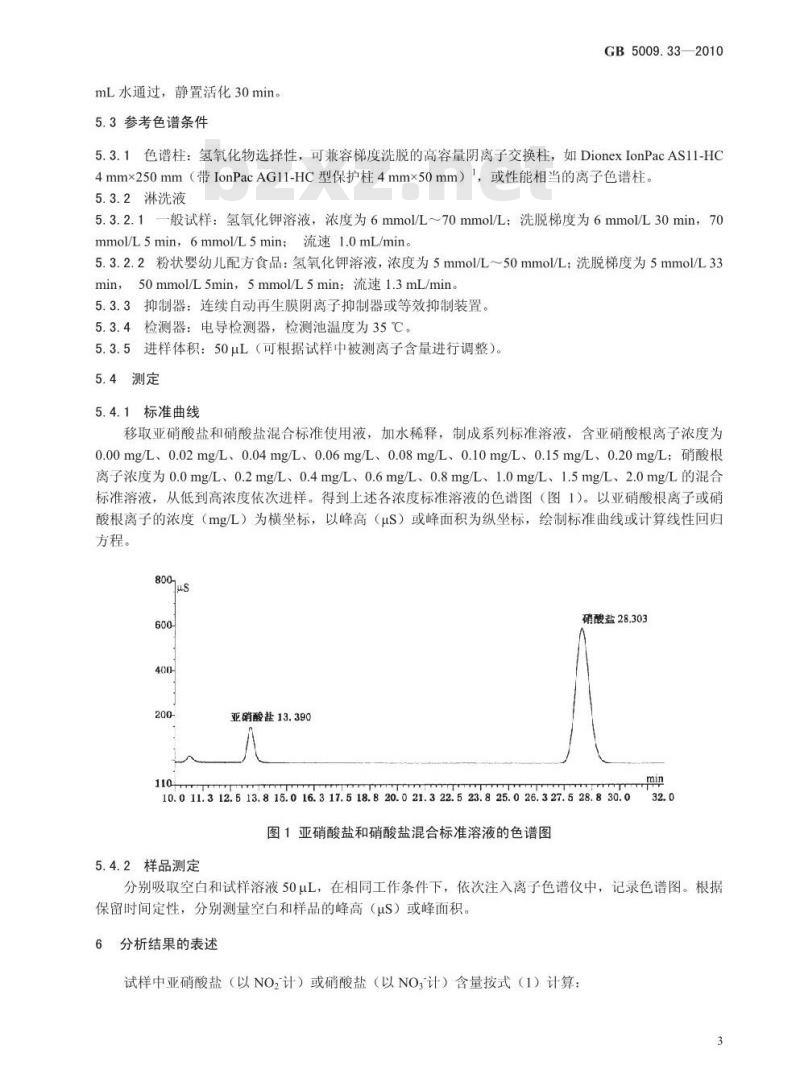
移取亚硝酸盐和硝酸盐混合标准使用液,加水稀释,制成系列标准溶液,含亚硝酸根离子浓度为0.00mg/L、0.02mg/L、0.04mg/L、0.06mg/L、0.08mg/L、0.10mg/L、0.15mg/L、0.20mg/L;硝酸根离子浓度为0.0mg/L、0.2mg/L、0.4mg/L、0.6mg/L、0.8mg/L、1.0mg/L、1.5mg/L、2.0mg/L的混合标准溶液,从低到高浓度依次进样。得到上述各浓度标准溶液的色谱图(图1)。以亚硝酸根离子或硝酸根离子的浓度(mg/L)为横坐标,以峰高(uS)或峰面积为纵坐标,绘制标准曲线或计算线性回归方程。
亚硝酸盐13.390
硝酸盐28.303
10. 0 11. 3 12. 5 13. 8 15. 0 16. 3 17. 5 18. 8 20. 0 21. 3 22. 5 23. 8 25. 0 26. 3 27. 5 28. 8 30. 0图1亚硝酸盐和硝酸盐混合标准溶液的色谱图5.4.2样品测定
分别吸取空白和试样溶液50uL,在相同工作条件下,依次注入离子色谱仪中,记录色谱图。根据保留时间定性,分别测量空白和样品的峰高(uS)或峰面积。分析结果的表述
试样中亚硝酸盐(以NO,计)或硝酸盐(以NO计)含量按式(1)计算:3
式中:
X= (c-c)×V×fx1000
mx1000
GB5009.33—2010
(1)
X一试样中亚硝酸根离子或硝酸根离子的含量,单位为毫克每千克(mg/kg);-测定用试样溶液中的亚硝酸根离子或硝酸根离子浓度,单位为毫克每升(mg/L):C
试剂空白液中亚硝酸根离子或硝酸根离子的浓度,单位为毫克每升(mg/L):co
一试样溶液体积,单位为毫升(mL):F试样溶液稀释倍数;
m试样取样量,单位为克(g)。说明:试样中测得的亚硝酸根离子含量乘以换算系数1.5,即得亚硝酸盐(按亚硝酸钠计)含量;试样中测得的硝酸根离子含量乘以换算系数1.37,即得硝酸盐(按硝酸钠计)含量。以重复性条件下获得的两次独立测定结果的算术平均值表示,结果保留两位有效数字。7
精密度
在重复性条件下获得的两次独立测定结果的绝对值差不得超过算术平均值的10%。第二法分光光度法
8原理
亚硝酸盐采用盐酸萘乙二胺法测定,硝酸盐采用镉柱还原法测定。试样经沉淀蛋白质、除去脂肪后,在弱酸条件下亚硝酸盐与对氨基苯磺酸重氨化后,再与盐酸萘乙二胺偶合形成紫红色染料,外标法测得亚硝酸盐含量。采用柱将硝酸盐还原成亚硝酸盐,测得亚硝酸盐总量,由此总量减去亚硝酸盐含量,即得试样中硝酸盐含量。9试剂和材料
除非另有规定,本方法所用试剂均为分析纯。水为GB/T6682规定的二级水或去离子水。9.1亚铁氰化钾(K4Fe(CN)3H2O)。9.2乙酸锌(Zn(CHCOO)22H2O)。9.3冰醋酸(CHsCOOH)。
9.4硼酸钠(NazB4O-10H20)。
9.5盐酸(p=1.19g/mL)。
9.6氨水(25%)。
9.7对氨基苯磺酸(C6HNO,S)。
9.8盐酸萘乙二胺(Ci2H14N22HCI)。9.9亚硝酸钠(NaNO2)。
9.10硝酸钠(NaNO,)。
9.11锌皮或锌棒。
9.12硫酸镉,
GB5009.33—2010
9.13亚铁氰化钾溶液(106g/L):称取106.0g亚铁氰化钾(9.1),用水溶解,并稀释至1000mL。9.14乙酸锌溶液(220g/L):称取220.0g乙酸锌(9.2),先加30mL冰醋酸(9.3)溶解,用水稀释至1000mL。
9.15饱和硼砂溶液(50g/L):称取5.0g硼酸钠(9.4),溶于100mL热水中,冷却后备用。9.16氨缓冲溶液(pH9.6~9.7):量取30mL盐酸(9.5),加100mL水,混匀后加65mL氨水(9.6)再加水稀释至1000mL,混匀。调节pH至9.6~9.7。9.17氨缓冲液的稀释液:量取50mL氨缓冲溶液(9.16),加水稀释至500mL,混匀。9.18盐酸(0.1mol/L):量取5mL盐酸,用水稀释至600mL。9.19对氨基苯磺酸溶液(4g/L):称取0.4g对氨基苯磺酸(9.7),溶于100mL20%(V/V)盐酸中置棕色瓶中混匀,避光保存。
9.20盐酸萘乙二胺溶液(2g/L):称取0.2g盐酸萘乙二胺(9.8),溶于100mL水中,混匀后,置棕色瓶中,避光保存。
9.21亚硝酸钠标准溶液(200μg/mL):准确称取0.1000g于110℃~120℃干燥恒重的亚硝酸钠,加水溶解移入500mL容量瓶中,加水稀释至刻度,混匀。9.22亚硝酸钠标准使用液(5.0μg/mL):临用前,吸取亚硝酸钠标准溶液5.00mL,置于200mL容量瓶中,加水稀释至刻度。
9.23硝酸钠标准溶液(200μg/mL,以亚硝酸钠计):准确称取0.1232g于110℃~120℃干燥恒重的硝酸钠,加水溶解,移于入500mL容量瓶中,并稀释至刻度。9.24硝酸钠标准使用液(5μg/mL):临用时吸取硝酸钠标准溶液2.50mL,置于100mL容量瓶中,加水稀释至刻度。
仪器和设备
10.1天平:感量为0.1mg和1mg
10.2组织揭碎机。
10.3超声波清洗器。
10.4恒温干燥箱。
10.5分光光度计。
10.6镐柱
GB5009.33—2010
10.6.1海绵状镉的制备:投入足够的锌皮或锌棒于500mL硫酸镉溶液(200g/L)中,经过3h~4h,当其中的镉全部被锌置换后,用玻璃棒轻轻刮下,取出残余锌棒,使镉沉底,倾去上层清液,以水用倾泻法多次洗涤,然后移入组织捣碎机中,加500mL水,捣碎约2S,用水将金属细粒洗至标准筛上,取20目~40目之间的部分。
10.6.2镉柱的装填:如图2。用水装满镉柱玻璃管,并装入2cm高的玻璃棉做垫,将玻璃棉压向柱底时,应将其中所包含的空气全部排出,在轻轻敲击下加入海绵状镉至8cm10cm高,上面用1cm高的玻璃棉覆盖,上置一贮液漏斗,末端要穿过橡皮塞与镉柱玻璃管紧密连接。如无上述镉柱玻璃管时,可以25m酸式滴定管代用,但过柱时要注意始终保持液面在镉层之上,当镉柱填装好后,先用25mL盐酸(0.1mol/L)洗涤,再以水洗两次,每次25mL,镉柱不用时用水封盖,随时都要保持水平面在镐层之上,不得使镉层夹有气泡,6
贮液漏斗,内径35mm,外径37mmS91
进液毛细管,内径0.4mm,外径6mms橡皮塞:
柱豉璃管,内径13mm,外径16mm玻璃棉;
海编状锰:
出液毛细管,内径2mm,外径8mmS8EE
图2镐柱示意图下载标准就来标准下载网
GB5009.33—2010
单位为毫来
10.6.3镉柱每次使用完毕后,应先以25mL盐酸(0.1mol/L)洗涤,再以水洗两次,每次25mL,最后用水覆盖镉柱。
10.6.4镉柱还原效率的测定:吸取20mL硝酸钠标准使用液,加入5mL氨缓冲液的稀释液,混匀后注入贮液漏斗,使流经镐柱还原,以原烧杯收集流出液,当贮液漏斗中的样液流完后,再加5mL水置换柱内留存的样液。取10.0mL还原后的溶液(相当10μg亚硝酸钠)于50mL比色管中,以下按11.4自“吸取0.00mL、0.20mL、0.40mL、0.60mL、0.80mL、1.00mL..”起依法操作,根据标准曲线计算测得结果,与加入量一致,还原效率应大于98%为符合要求。10.6.5还原效率计算
还原效率按式(2)进行计算。
式中:
X—还原效率,%;
A测得亚硝酸钠的含量,单位为微克(ug):测定用溶液相当亚硝酸钠的含量,单位为微克(μg)。10
11分析步骤
11.1试样的预处理
同5.1。
11.2提取
GB5009.33—2010
称取5g(精确至0.01g)制成勾浆的试样(如制备过程中加水,应按加水量折算),置于50mL烧杯中,加12.5mL饱和硼砂溶液(9.15),搅拌均匀,以70℃左右的水约300mL将试样洗入500mL容量瓶中,于沸水浴中加热15min,取出置冷水浴中冷却,并放置至室温。11.3提取液净化
在振荡上述提取液时加入5mL亚铁氰化钾溶液(9.13),摇勾,再加入5mL乙酸锌溶液(9.14),以沉淀蛋白质。加水至刻度,摇匀,放置30min,除去上层脂肪,上清液用滤纸过滤,弃去初滤液30mL,滤液备用。
11.4亚硝酸盐的测定
吸取40.0mL上述滤液于50mL带塞比色管中,另吸取0.00mL、0.20mL、0.40mL、0.60mL、0.80mL、1.00mL、1.50mL、2.00mL、2.50mL亚硝酸钠标准使用液(相当于0.0μg、1.0μg、2.0μg、3.0μg、4.0μg、5.0μg、7.5μg、10.0μg、12.5μg亚硝酸钠),分别置于50mL带塞比色管中。于标准管与试样管中分别加入2mL对氨基苯磺酸溶液(9.19),混匀,静置3min~5min后各加入1mL盐酸萘乙二胺溶液(9.20),加水至刻度,混匀,静置15min,用2cm比色杯,以零管调节零点,于波长538nm处测吸光度,绘制标准曲线比较。同时做试剂空白。11.5硝酸盐的测定
11.5.1镉柱还原
11.5.1.1先以25mL稀氨缓冲液(9.17)冲洗镉柱,流速控制在3mL/min5mL/min(以滴定管代替的可控制在2mL/min~3mL/min)。11.5.1.2吸取20mL滤液于50mL烧杯中,加5mL氨缓冲溶液(9.16),混合后注入液漏斗,使流经镉柱还原,以原烧杯收集流出液,当贮液漏斗中的样液流尽后,再加5m水置换柱内留存的样液。11.5.1.3将全部收集液如前再经镉柱还原一次,第二次流出液收集于100mL容量瓶中,继以水流经镉柱洗涤三次,每次20mL,洗液一并收集于同一容量瓶中,加水至刻度,混匀。11.5.2亚硝酸钠总量的测定
吸取10mL~20mL还原后的样液于50mL比色管中。以下按11.4自*吸取0.00mL、0.20mL、0.40mL、0.60mL、0.80mL、1.00mL...\起依法操作。12分析结果的表述
12.1亚硝酸盐含量计算
亚硝酸盐(以亚硝酸钠计)的含量按式(3)进行计算。Xi=-
Aix1000
≤x1000
式中:
X试样中亚硝酸钠的含量,单位为毫克每千克(mg/kg);Ar—测定用样液中亚硝酸钠的质量,单位为微克(μg);(3)
m试样质量,单位为克(g);
V—测定用样液体积,单位为毫升(mL);Vo—试样处理液总体积,单位为毫升(mL)。GB5009.33—2010
以重复性条件下获得的两次独立测定结果的算术平均值表示,结果保留两位有效数字。12.2硝酸盐含量的计算
硝酸盐(以硝酸钠计)的含量按式(4)进行计算。X2=
式中:
A2x1000
×1000
Xz试样中硝酸钠的含量,单位为毫克每千克(mg/kg);-经镉粉还原后测得总亚硝酸钠的质量,单位为微克(ug);A
-试样的质量,单位为克(g);
-亚硝酸钠换算成硝酸钠的系数:测总亚硝酸钠的测定用样液体积,单位为毫升(mL):V
试样处理液总体积,单位为毫升(mL);Vo
经镉柱还原后样液总体积,单位为毫升(mL);V
-经镉柱还原后样液的测定用体积,单位为毫升(mL):V
Xi一由式(3)计算出的试样中亚硝酸钠的含量,单位为毫克每千克(mg/kg)。(4)
以重复性条件下获得的两次独立测定结果的算术平均值表示,结果保留两位有效数字13精密度
在重复性条件下获得的两次独立测定结果的绝对差值不得超过算术平均值的10%。第三法乳及乳制品中亚硝酸盐与硝酸盐的测定14原理
试样经沉淀蛋白质、除去脂肪后,用镀铜镉粒使部分滤液中的硝酸盐还原为亚硝酸盐。在滤液和已还原的滤液中,加入磺胺和N-1-萘基-乙二胺二盐酸盐,使其显粉红色,然后用分光光度计在538nm波长下测其吸光度。
将测得的吸光度与亚硝酸钠标准系列溶液的吸光度进行比较,就可计算出样品中的亚硝酸盐含量和硝酸盐还原后的亚硝酸总量:从两者之间的差值可以计算出硝酸盐的含量。15试剂和材料
测定用水应是不含硝酸盐和亚硝酸盐的蒸馏水或去离子水。注:为避免镀铜镉柱(16.10)中混入小气泡,柱制备(17.1)、柱还原能力的检查(17.2)和柱再生(17.3)时所用的蒸馏水或去离子水最好是刚沸过并冷却至室温的。15.1亚硝酸钠(NaNO2)。
15.2硝酸钾(KNO3)。
15.3镀铜镐柱
镐粒直径0.3mm~0.8mm。也可按下述方法制备。GB5009.332010
将适量的锌棒放入烧杯中,用40g/L的硫酸镉(CdSO4-8H2O)溶液浸没锌棒。在24h之内,不断将锌棒上的海绵状镉刮下来。取出锌棒,淫出烧杯中多余的溶液,剩下的溶液能浸没镉即可。用蒸馏水冲洗海绵状镉2次~3次,然后把镉移入小型搅拌器中,同时加入400mL0.1mol/L的盐酸。搅拌几秒钟,以得到所需粒度的颗粒。将搅拌器中的镉粒连同溶液一起倒回烧杯中,静置几小时,这期间要搅拌几次以除掉气泡。倾出大部分溶液,立即按17.1.1至17.1.8中叙述的方法镀铜。15.4硫酸铜溶液:溶解20g硫酸铜(CuSO45H2O)于水中,稀释至1000mL。15.5盐酸-氨水缓冲溶液:pH9.60~9.70。用600mL水稀释75mL浓盐酸(质量分数为36%~38%)混匀后,再加入135mL浓氨水(质量分数等于25%的新鲜氨水)。用水稀释至1000mL,混勾。用精密pH计调pH值为9.609.70。
15.6盐酸(2mol/L):160mL的浓盐酸(质量分数为36%~38%)用水稀释至1000mL。15.7盐酸(0.1mol/L):50mL2mol/L的盐酸用水稀释至1000mL。15.8沉淀蛋白和脂肪的溶液:
15.8.1硫酸锌溶液:将53.5g的硫酸锌(ZnSO47H2O)溶于水中,并稀释至100mL。15.8.2亚铁氰化钾溶液:将17.2g的三水亚铁氰化钾[K4Fe(CN)3H2O]溶于水中,稀释至100mL15.9EDTA溶液:用水将33.5g的乙二胺四乙酸二钠(Na2CioHi4N203:2H20)溶解,稀释至1000mL。15.10显色液1:体积比为450:550的盐酸。将450mL浓盐酸(质量分数为36%~38%)加入到550mL水中,冷却后装入试剂瓶中。15.11显色液2:5g/L的磺胺溶液。在75mL水中加入5mL浓盐酸(质量分数为36%~38%),然后在水浴上加热,用其溶解0.5g磺胺(NH2C6H4SO2NH2)。冷却至室温后用水稀释至100mL。必要时进行过滤。
15.12显色液3:1g/L的萘胺盐酸盐溶液。将0.1g的N-1-萘基-乙二胺二盐酸盐(C1oHNHCH2CH2NH22HCI)溶于水,稀释至100mL。必要时过滤。注:此溶液应少量配制,装于密封的棕色瓶中,冰箱中2℃~5℃保存。15.13亚硝酸钠标准溶液:相当于亚硝酸根的浓度为0.001g/L将亚硝酸钠在110℃~120℃的范围内干燥至恒重。冷却后称取0.150g,溶于1000mL容量瓶中,用水定容。在使用的当天配制该溶液。取10mL上述溶液和20mL缓冲溶液(15.5)于1000mL容量瓶中,用水定容。每1mL该标准溶液中含1.00μg的NO2。15.14硝酸钾标准溶液,相当于硝酸根的浓度为0.0045g/L将硝酸钾在110℃~120℃的温度范围内干燥至恒重,冷却后称取1.4580g,溶于1000mL容量瓶中,用水定容。
GB5009.33—2010
食品安全国家标准
食品中亚硝酸盐与硝酸盐的测定Nationalfoodsafetystandard
Determinationof nitriteandnitrateinfoods2010-03-26发布
中华人民共和国卫生部
2010-06-01实施
本标准代替GB/T5009.33-2008
《食品中亚硝酸盐与硝酸盐的测定》。本标准与GB/T5009.33-2008相比,主要变化如下:-第一法中增加粉状婴幼儿配方食品的淋洗条件:GB5009.33—2010
-删除第三法示波极谱法,增加“乳及乳制品中亚硝酸盐与硝酸盐的测定”作为第三法。本标准所代替标准的历次版本发布情况为:GB5009.33-1985、GB/T5009.33-1996、GB/T5009.33-2003、GB/T5009.33-20081范围
食品安全国家标准
食品中亚硝酸盐与硝酸盐的测定本标准规定了食品中亚硝酸盐和硝酸盐的测定方法。本标准适用于食品中亚硝酸盐和硝酸盐的测定。第一法离子色谱法
2原理
GB5009.33—2010
试样经沉淀蛋白质、除去脂肪后,采用相应的方法提取和净化,以氢氧化钾溶液为淋洗液,阴离子交换柱分离,电导检测器检测。以保留时间定性,外标法定量。3试剂和材料
3.1超纯水:电阻率>18.2M2.cm。3.2乙酸(CH;COOH):分析纯。
3.3氢氧化钾(KOH):分析纯。
3.4乙酸溶液(3%):量取乙酸(3.2)3mL于100mL容量瓶中,以水稀释至刻度,混匀。3.5亚硝酸根离子(NO2)标准溶液(100mg/L,水基体)。3.6硝酸根离子(NO3)标准溶液(1000mg/L,水基体)。3.7亚硝酸盐(以NO2计,下同)和硝酸盐(以NO3计,下同)混合标准使用液:准确移取亚硝酸根离子(NO2)和硝酸根离子(NO3)的标准溶液各1.0mL于100mL容量瓶中,用水稀释至刻度,此溶液每1L含亚硝酸根离子1.0mg和硝酸根离子10.0mg4
仪器和设备
4.1离子色谱仪:包括电导检测器,配有抑制器,高容量阴离子交换柱,50μL定量环4.2食物粉碎机。
4.3超声波清洗器。
4.4天平:感量为0.1mg和1mg
4.5离心机:转速≥10000转/分钟,配5mL或10mL离心管。4.60.22μm水性滤膜针头滤器。4.7净化柱:包括Ci8柱、Ag柱和Na柱或等效柱。4.8注射器:1.0mL和2.5mL
GB5009.332010
注:所有玻璃器皿使用前均需依次用2mol/L氢氧化钾和水分别浸泡4h,然后用水冲洗3次~5次,晾干备用。5分析步骤
5.1试样预处理
5.1.1新鲜蔬菜、水果:将试样用去离子水洗净,晾干后,取可食部切碎混匀。将切碎的样品用四分法取适量,用食物粉碎机制成匀浆备用。如需加水应记录加水量5.1.2肉类、蛋、水产及其制品:用四分法取适量或取全部,用食物粉碎机制成匀浆备用。5.1.3乳粉、豆奶粉、婴儿配方粉等固态乳制品(不包括干酪):将试样装入能够容纳2倍试样体积的带盖容器中,通过反复摇晃和颠倒容器使样品充分混匀直到使试样均一化。5.1.4发酵乳、乳、炼乳及其他液体乳制品:通过搅拌或反复摇晃和颠倒容器使试样充分混匀。5.1.5干酪:取适量的样品研磨成均匀的泥浆状。为避免水分损失,研磨过程中应避免产生过多的热量。
5.2提取
5.2.1水果、蔬菜、鱼类、肉类、蛋类及其制品等:称取试样勾浆5g(精确至0.01g,可适当调整试样的取样量,以下相同),以80mL水洗入100mL容量瓶中,超声提取30min,每隔5min振摇一次,保持固相完全分散。于75℃水浴中放置5min,取出放置至室温,加水稀释至刻度。溶液经滤纸过滤后,取部分溶液于10000转/分钟离心15min,上清液备用。5.2.2腌鱼类、腌肉类及其它腌制品:称取试样匀浆2g(精确至0.01g),以80mL水洗入100mL容量瓶中,超声提取30min,每5min振摇一次,保持固相完全分散。于75℃水浴中放置5min,取出放置至室温,加水稀释至刻度。溶液经滤纸过滤后,取部分溶液于10000转/分钟离心15min,上清液备用。
5.2.3乳:称取试样10g(精确至0.01g),置于100mL容量瓶中,加水80mL,摇匀,超声30min加入3%乙酸溶液2mL,于4℃放置20min,取出放置至室温,加水稀释至刻度。溶液经滤纸过滤,取上清液备用。
5.2.4乳粉:称取试样2.5g(精确至0.01g),置于100mL容量瓶中,加水80mL,摇匀,超声30min,加入3%乙酸溶液2mL,于4℃放置20min,取出放置至室温,加水稀释至刻度。溶液经滤纸过滤,取上清液备用。
5.2.5取上述备用的上清液约15mL,通过0.22μum水性滤膜针头滤器、C18柱,弃去前面3mL(如果氯离子大于100mg/L,则需要依次通过针头滤器、C18柱、Ag柱和Na柱,弃去前面7mL),收集后面洗脱液待测。
固相萃取柱使用前需进行活化,如使用OnGuardIIRP柱(1.0mL)、OnGuardⅡIAg柱(1.0mL和OnGuardIINa柱(1.0mL),其活化过程为:OnGuardIRP柱(1.0mL)使用前依次用10mL甲醇、15mL水通过,静置活化30min。OnGuardIIAg柱(1.0mL)和OnGuardIINa柱(1.0mL)用10「给出这一信息是为了方便本标准的使用者,并不表示对该产品的认可,如果其他等效产品具有相同的效果,则可使用这些等效的产品。
mL水通过,静置活化30min。
5.3参考色谱条件
GB5009.33—2010
5.3.1色谱柱:氢氧化物选择性,可兼容梯度洗脱的高容量阴离子交换柱,如DionexIonPacAS11-HC4mm×250mm(带IonPacAG11-HC型保护柱4mmx50mm)1,或性能相当的离子色谱柱。5.3.2淋洗液
5.3.2.1一般试样:氢氧化钾溶液,浓度为6mmol/L~70mmol/L;洗脱梯度为6mmol/L30min,70mmol/L5min,6mmol/L5min;流速1.0mL/min。5.3.2.2粉状婴幼儿配方食品:氢氧化钾溶液,浓度为5mmol/L~50mmol/L;洗脱梯度为5mmol/L33min,50mmol/L5min,5mmol/L5min:流速1.3mL/min。5.3.3抑制器:连续自动再生膜阴离子抑制器或等效抑制装置。5.3.4检测器:电导检测器,检测池温度为35℃。5.3.5进样体积:50uL(可根据试样中被测离子含量进行调整)。5.4测定
5.4.1标准曲线
移取亚硝酸盐和硝酸盐混合标准使用液,加水稀释,制成系列标准溶液,含亚硝酸根离子浓度为0.00mg/L、0.02mg/L、0.04mg/L、0.06mg/L、0.08mg/L、0.10mg/L、0.15mg/L、0.20mg/L;硝酸根离子浓度为0.0mg/L、0.2mg/L、0.4mg/L、0.6mg/L、0.8mg/L、1.0mg/L、1.5mg/L、2.0mg/L的混合标准溶液,从低到高浓度依次进样。得到上述各浓度标准溶液的色谱图(图1)。以亚硝酸根离子或硝酸根离子的浓度(mg/L)为横坐标,以峰高(uS)或峰面积为纵坐标,绘制标准曲线或计算线性回归方程。
亚硝酸盐13.390
硝酸盐28.303
10. 0 11. 3 12. 5 13. 8 15. 0 16. 3 17. 5 18. 8 20. 0 21. 3 22. 5 23. 8 25. 0 26. 3 27. 5 28. 8 30. 0图1亚硝酸盐和硝酸盐混合标准溶液的色谱图5.4.2样品测定
分别吸取空白和试样溶液50uL,在相同工作条件下,依次注入离子色谱仪中,记录色谱图。根据保留时间定性,分别测量空白和样品的峰高(uS)或峰面积。分析结果的表述
试样中亚硝酸盐(以NO,计)或硝酸盐(以NO计)含量按式(1)计算:3
式中:
X= (c-c)×V×fx1000
mx1000
GB5009.33—2010
(1)
X一试样中亚硝酸根离子或硝酸根离子的含量,单位为毫克每千克(mg/kg);-测定用试样溶液中的亚硝酸根离子或硝酸根离子浓度,单位为毫克每升(mg/L):C
试剂空白液中亚硝酸根离子或硝酸根离子的浓度,单位为毫克每升(mg/L):co
一试样溶液体积,单位为毫升(mL):F试样溶液稀释倍数;
m试样取样量,单位为克(g)。说明:试样中测得的亚硝酸根离子含量乘以换算系数1.5,即得亚硝酸盐(按亚硝酸钠计)含量;试样中测得的硝酸根离子含量乘以换算系数1.37,即得硝酸盐(按硝酸钠计)含量。以重复性条件下获得的两次独立测定结果的算术平均值表示,结果保留两位有效数字。7
精密度
在重复性条件下获得的两次独立测定结果的绝对值差不得超过算术平均值的10%。第二法分光光度法
8原理
亚硝酸盐采用盐酸萘乙二胺法测定,硝酸盐采用镉柱还原法测定。试样经沉淀蛋白质、除去脂肪后,在弱酸条件下亚硝酸盐与对氨基苯磺酸重氨化后,再与盐酸萘乙二胺偶合形成紫红色染料,外标法测得亚硝酸盐含量。采用柱将硝酸盐还原成亚硝酸盐,测得亚硝酸盐总量,由此总量减去亚硝酸盐含量,即得试样中硝酸盐含量。9试剂和材料
除非另有规定,本方法所用试剂均为分析纯。水为GB/T6682规定的二级水或去离子水。9.1亚铁氰化钾(K4Fe(CN)3H2O)。9.2乙酸锌(Zn(CHCOO)22H2O)。9.3冰醋酸(CHsCOOH)。
9.4硼酸钠(NazB4O-10H20)。
9.5盐酸(p=1.19g/mL)。
9.6氨水(25%)。
9.7对氨基苯磺酸(C6HNO,S)。
9.8盐酸萘乙二胺(Ci2H14N22HCI)。9.9亚硝酸钠(NaNO2)。
9.10硝酸钠(NaNO,)。
9.11锌皮或锌棒。
9.12硫酸镉,
GB5009.33—2010
9.13亚铁氰化钾溶液(106g/L):称取106.0g亚铁氰化钾(9.1),用水溶解,并稀释至1000mL。9.14乙酸锌溶液(220g/L):称取220.0g乙酸锌(9.2),先加30mL冰醋酸(9.3)溶解,用水稀释至1000mL。
9.15饱和硼砂溶液(50g/L):称取5.0g硼酸钠(9.4),溶于100mL热水中,冷却后备用。9.16氨缓冲溶液(pH9.6~9.7):量取30mL盐酸(9.5),加100mL水,混匀后加65mL氨水(9.6)再加水稀释至1000mL,混匀。调节pH至9.6~9.7。9.17氨缓冲液的稀释液:量取50mL氨缓冲溶液(9.16),加水稀释至500mL,混匀。9.18盐酸(0.1mol/L):量取5mL盐酸,用水稀释至600mL。9.19对氨基苯磺酸溶液(4g/L):称取0.4g对氨基苯磺酸(9.7),溶于100mL20%(V/V)盐酸中置棕色瓶中混匀,避光保存。
9.20盐酸萘乙二胺溶液(2g/L):称取0.2g盐酸萘乙二胺(9.8),溶于100mL水中,混匀后,置棕色瓶中,避光保存。
9.21亚硝酸钠标准溶液(200μg/mL):准确称取0.1000g于110℃~120℃干燥恒重的亚硝酸钠,加水溶解移入500mL容量瓶中,加水稀释至刻度,混匀。9.22亚硝酸钠标准使用液(5.0μg/mL):临用前,吸取亚硝酸钠标准溶液5.00mL,置于200mL容量瓶中,加水稀释至刻度。
9.23硝酸钠标准溶液(200μg/mL,以亚硝酸钠计):准确称取0.1232g于110℃~120℃干燥恒重的硝酸钠,加水溶解,移于入500mL容量瓶中,并稀释至刻度。9.24硝酸钠标准使用液(5μg/mL):临用时吸取硝酸钠标准溶液2.50mL,置于100mL容量瓶中,加水稀释至刻度。
仪器和设备
10.1天平:感量为0.1mg和1mg
10.2组织揭碎机。
10.3超声波清洗器。
10.4恒温干燥箱。
10.5分光光度计。
10.6镐柱
GB5009.33—2010
10.6.1海绵状镉的制备:投入足够的锌皮或锌棒于500mL硫酸镉溶液(200g/L)中,经过3h~4h,当其中的镉全部被锌置换后,用玻璃棒轻轻刮下,取出残余锌棒,使镉沉底,倾去上层清液,以水用倾泻法多次洗涤,然后移入组织捣碎机中,加500mL水,捣碎约2S,用水将金属细粒洗至标准筛上,取20目~40目之间的部分。
10.6.2镉柱的装填:如图2。用水装满镉柱玻璃管,并装入2cm高的玻璃棉做垫,将玻璃棉压向柱底时,应将其中所包含的空气全部排出,在轻轻敲击下加入海绵状镉至8cm10cm高,上面用1cm高的玻璃棉覆盖,上置一贮液漏斗,末端要穿过橡皮塞与镉柱玻璃管紧密连接。如无上述镉柱玻璃管时,可以25m酸式滴定管代用,但过柱时要注意始终保持液面在镉层之上,当镉柱填装好后,先用25mL盐酸(0.1mol/L)洗涤,再以水洗两次,每次25mL,镉柱不用时用水封盖,随时都要保持水平面在镐层之上,不得使镉层夹有气泡,6
贮液漏斗,内径35mm,外径37mmS91
进液毛细管,内径0.4mm,外径6mms橡皮塞:
柱豉璃管,内径13mm,外径16mm玻璃棉;
海编状锰:
出液毛细管,内径2mm,外径8mmS8EE
图2镐柱示意图下载标准就来标准下载网
GB5009.33—2010
单位为毫来
10.6.3镉柱每次使用完毕后,应先以25mL盐酸(0.1mol/L)洗涤,再以水洗两次,每次25mL,最后用水覆盖镉柱。
10.6.4镉柱还原效率的测定:吸取20mL硝酸钠标准使用液,加入5mL氨缓冲液的稀释液,混匀后注入贮液漏斗,使流经镐柱还原,以原烧杯收集流出液,当贮液漏斗中的样液流完后,再加5mL水置换柱内留存的样液。取10.0mL还原后的溶液(相当10μg亚硝酸钠)于50mL比色管中,以下按11.4自“吸取0.00mL、0.20mL、0.40mL、0.60mL、0.80mL、1.00mL..”起依法操作,根据标准曲线计算测得结果,与加入量一致,还原效率应大于98%为符合要求。10.6.5还原效率计算
还原效率按式(2)进行计算。
式中:
X—还原效率,%;
A测得亚硝酸钠的含量,单位为微克(ug):测定用溶液相当亚硝酸钠的含量,单位为微克(μg)。10
11分析步骤
11.1试样的预处理
同5.1。
11.2提取
GB5009.33—2010
称取5g(精确至0.01g)制成勾浆的试样(如制备过程中加水,应按加水量折算),置于50mL烧杯中,加12.5mL饱和硼砂溶液(9.15),搅拌均匀,以70℃左右的水约300mL将试样洗入500mL容量瓶中,于沸水浴中加热15min,取出置冷水浴中冷却,并放置至室温。11.3提取液净化
在振荡上述提取液时加入5mL亚铁氰化钾溶液(9.13),摇勾,再加入5mL乙酸锌溶液(9.14),以沉淀蛋白质。加水至刻度,摇匀,放置30min,除去上层脂肪,上清液用滤纸过滤,弃去初滤液30mL,滤液备用。
11.4亚硝酸盐的测定
吸取40.0mL上述滤液于50mL带塞比色管中,另吸取0.00mL、0.20mL、0.40mL、0.60mL、0.80mL、1.00mL、1.50mL、2.00mL、2.50mL亚硝酸钠标准使用液(相当于0.0μg、1.0μg、2.0μg、3.0μg、4.0μg、5.0μg、7.5μg、10.0μg、12.5μg亚硝酸钠),分别置于50mL带塞比色管中。于标准管与试样管中分别加入2mL对氨基苯磺酸溶液(9.19),混匀,静置3min~5min后各加入1mL盐酸萘乙二胺溶液(9.20),加水至刻度,混匀,静置15min,用2cm比色杯,以零管调节零点,于波长538nm处测吸光度,绘制标准曲线比较。同时做试剂空白。11.5硝酸盐的测定
11.5.1镉柱还原
11.5.1.1先以25mL稀氨缓冲液(9.17)冲洗镉柱,流速控制在3mL/min5mL/min(以滴定管代替的可控制在2mL/min~3mL/min)。11.5.1.2吸取20mL滤液于50mL烧杯中,加5mL氨缓冲溶液(9.16),混合后注入液漏斗,使流经镉柱还原,以原烧杯收集流出液,当贮液漏斗中的样液流尽后,再加5m水置换柱内留存的样液。11.5.1.3将全部收集液如前再经镉柱还原一次,第二次流出液收集于100mL容量瓶中,继以水流经镉柱洗涤三次,每次20mL,洗液一并收集于同一容量瓶中,加水至刻度,混匀。11.5.2亚硝酸钠总量的测定
吸取10mL~20mL还原后的样液于50mL比色管中。以下按11.4自*吸取0.00mL、0.20mL、0.40mL、0.60mL、0.80mL、1.00mL...\起依法操作。12分析结果的表述
12.1亚硝酸盐含量计算
亚硝酸盐(以亚硝酸钠计)的含量按式(3)进行计算。Xi=-
Aix1000
≤x1000
式中:
X试样中亚硝酸钠的含量,单位为毫克每千克(mg/kg);Ar—测定用样液中亚硝酸钠的质量,单位为微克(μg);(3)
m试样质量,单位为克(g);
V—测定用样液体积,单位为毫升(mL);Vo—试样处理液总体积,单位为毫升(mL)。GB5009.33—2010
以重复性条件下获得的两次独立测定结果的算术平均值表示,结果保留两位有效数字。12.2硝酸盐含量的计算
硝酸盐(以硝酸钠计)的含量按式(4)进行计算。X2=
式中:
A2x1000
×1000
Xz试样中硝酸钠的含量,单位为毫克每千克(mg/kg);-经镉粉还原后测得总亚硝酸钠的质量,单位为微克(ug);A
-试样的质量,单位为克(g);
-亚硝酸钠换算成硝酸钠的系数:测总亚硝酸钠的测定用样液体积,单位为毫升(mL):V
试样处理液总体积,单位为毫升(mL);Vo
经镉柱还原后样液总体积,单位为毫升(mL);V
-经镉柱还原后样液的测定用体积,单位为毫升(mL):V
Xi一由式(3)计算出的试样中亚硝酸钠的含量,单位为毫克每千克(mg/kg)。(4)
以重复性条件下获得的两次独立测定结果的算术平均值表示,结果保留两位有效数字13精密度
在重复性条件下获得的两次独立测定结果的绝对差值不得超过算术平均值的10%。第三法乳及乳制品中亚硝酸盐与硝酸盐的测定14原理
试样经沉淀蛋白质、除去脂肪后,用镀铜镉粒使部分滤液中的硝酸盐还原为亚硝酸盐。在滤液和已还原的滤液中,加入磺胺和N-1-萘基-乙二胺二盐酸盐,使其显粉红色,然后用分光光度计在538nm波长下测其吸光度。
将测得的吸光度与亚硝酸钠标准系列溶液的吸光度进行比较,就可计算出样品中的亚硝酸盐含量和硝酸盐还原后的亚硝酸总量:从两者之间的差值可以计算出硝酸盐的含量。15试剂和材料
测定用水应是不含硝酸盐和亚硝酸盐的蒸馏水或去离子水。注:为避免镀铜镉柱(16.10)中混入小气泡,柱制备(17.1)、柱还原能力的检查(17.2)和柱再生(17.3)时所用的蒸馏水或去离子水最好是刚沸过并冷却至室温的。15.1亚硝酸钠(NaNO2)。
15.2硝酸钾(KNO3)。
15.3镀铜镐柱
镐粒直径0.3mm~0.8mm。也可按下述方法制备。GB5009.332010
将适量的锌棒放入烧杯中,用40g/L的硫酸镉(CdSO4-8H2O)溶液浸没锌棒。在24h之内,不断将锌棒上的海绵状镉刮下来。取出锌棒,淫出烧杯中多余的溶液,剩下的溶液能浸没镉即可。用蒸馏水冲洗海绵状镉2次~3次,然后把镉移入小型搅拌器中,同时加入400mL0.1mol/L的盐酸。搅拌几秒钟,以得到所需粒度的颗粒。将搅拌器中的镉粒连同溶液一起倒回烧杯中,静置几小时,这期间要搅拌几次以除掉气泡。倾出大部分溶液,立即按17.1.1至17.1.8中叙述的方法镀铜。15.4硫酸铜溶液:溶解20g硫酸铜(CuSO45H2O)于水中,稀释至1000mL。15.5盐酸-氨水缓冲溶液:pH9.60~9.70。用600mL水稀释75mL浓盐酸(质量分数为36%~38%)混匀后,再加入135mL浓氨水(质量分数等于25%的新鲜氨水)。用水稀释至1000mL,混勾。用精密pH计调pH值为9.609.70。
15.6盐酸(2mol/L):160mL的浓盐酸(质量分数为36%~38%)用水稀释至1000mL。15.7盐酸(0.1mol/L):50mL2mol/L的盐酸用水稀释至1000mL。15.8沉淀蛋白和脂肪的溶液:
15.8.1硫酸锌溶液:将53.5g的硫酸锌(ZnSO47H2O)溶于水中,并稀释至100mL。15.8.2亚铁氰化钾溶液:将17.2g的三水亚铁氰化钾[K4Fe(CN)3H2O]溶于水中,稀释至100mL15.9EDTA溶液:用水将33.5g的乙二胺四乙酸二钠(Na2CioHi4N203:2H20)溶解,稀释至1000mL。15.10显色液1:体积比为450:550的盐酸。将450mL浓盐酸(质量分数为36%~38%)加入到550mL水中,冷却后装入试剂瓶中。15.11显色液2:5g/L的磺胺溶液。在75mL水中加入5mL浓盐酸(质量分数为36%~38%),然后在水浴上加热,用其溶解0.5g磺胺(NH2C6H4SO2NH2)。冷却至室温后用水稀释至100mL。必要时进行过滤。
15.12显色液3:1g/L的萘胺盐酸盐溶液。将0.1g的N-1-萘基-乙二胺二盐酸盐(C1oHNHCH2CH2NH22HCI)溶于水,稀释至100mL。必要时过滤。注:此溶液应少量配制,装于密封的棕色瓶中,冰箱中2℃~5℃保存。15.13亚硝酸钠标准溶液:相当于亚硝酸根的浓度为0.001g/L将亚硝酸钠在110℃~120℃的范围内干燥至恒重。冷却后称取0.150g,溶于1000mL容量瓶中,用水定容。在使用的当天配制该溶液。取10mL上述溶液和20mL缓冲溶液(15.5)于1000mL容量瓶中,用水定容。每1mL该标准溶液中含1.00μg的NO2。15.14硝酸钾标准溶液,相当于硝酸根的浓度为0.0045g/L将硝酸钾在110℃~120℃的温度范围内干燥至恒重,冷却后称取1.4580g,溶于1000mL容量瓶中,用水定容。
小提示:此标准内容仅展示完整标准里的部分截取内容,若需要完整标准请到上方自行免费下载完整标准文档。
标准图片预览:




- 热门标准
- 国家标准
- GB/T12949-1991 滑动轴承覆有减摩塑料层的双金属轴套
- GB/T38627-2020 信息技术 实时定位 磁定位数据接口
- GB/T1182-2018 产品几何技术规范(GPS) 几何公差 形状、方向、位置和跳动公差标注
- GB/T15349-1994 化学试剂 溴甲酚绿
- GB175-2023 通用硅酸盐水泥
- GB/T8878—2014 棉针织内衣
- GB/T228.1-2021 金属材料 拉伸试验 第1部分:室温试验方法
- GB/T10125-2021 人造气氛腐蚀试验 盐雾试验
- GB/T97.1-2002 平垫圈A级
- GB/T43802-2024 绿色产品评价 物流周转箱
- GB/T7588.1-2020 电梯制造与安装安全规范第1部分:乘客电梯和载货电梯
- GB31094-2014 防爆电梯制造与安装安全规范
- GB9178-1988 集成电路术语
- GB/T42970-2023 半导体集成电路 视频编解码电路测试方法
- GB/T38987-2020 硬质合金螺旋孔棒材
- 行业新闻
请牢记:“bzxz.net”即是“标准下载”四个汉字汉语拼音首字母与国际顶级域名“.net”的组合。 ©2025 标准下载网 www.bzxz.net 本站邮件:wymp4wang@gmail.com