- 您的位置:
- 标准下载网 >>
- 标准分类 >>
- 国家标准(GB) >>
- GB 28316-2012 食品添加剂 番茄红
标准号:
GB 28316-2012
标准名称:
食品添加剂 番茄红
标准类别:
国家标准(GB)
标准状态:
现行出版语种:
简体中文下载格式:
.rar .pdf下载大小:
手机扫码下载更方便
部分标准内容:
中华人民共和国国家标准
GB283162012
食品安全国家标准
食品添加剂
2012-04-25发布
番茄红
2012-06-25实施
中华人民共和国卫生部
1范围
食品安全国家标准
食品添加剂
番茄红
GB283162012
本标准适用于以番茄(Lycopersicon)或番茄制品为原料,以超临界流体(包括二氧化碳等)或有机溶剂为萃取介质制备的食品添加剂番茄红。2分子式、结构式、相对分子质量2.1分子式
番茄红素:C40H56
2.2结构式
2.3相对分子质量
全反式番茄红素化学结构式
536.87(按2007年国际相对原子质量)3技术要求
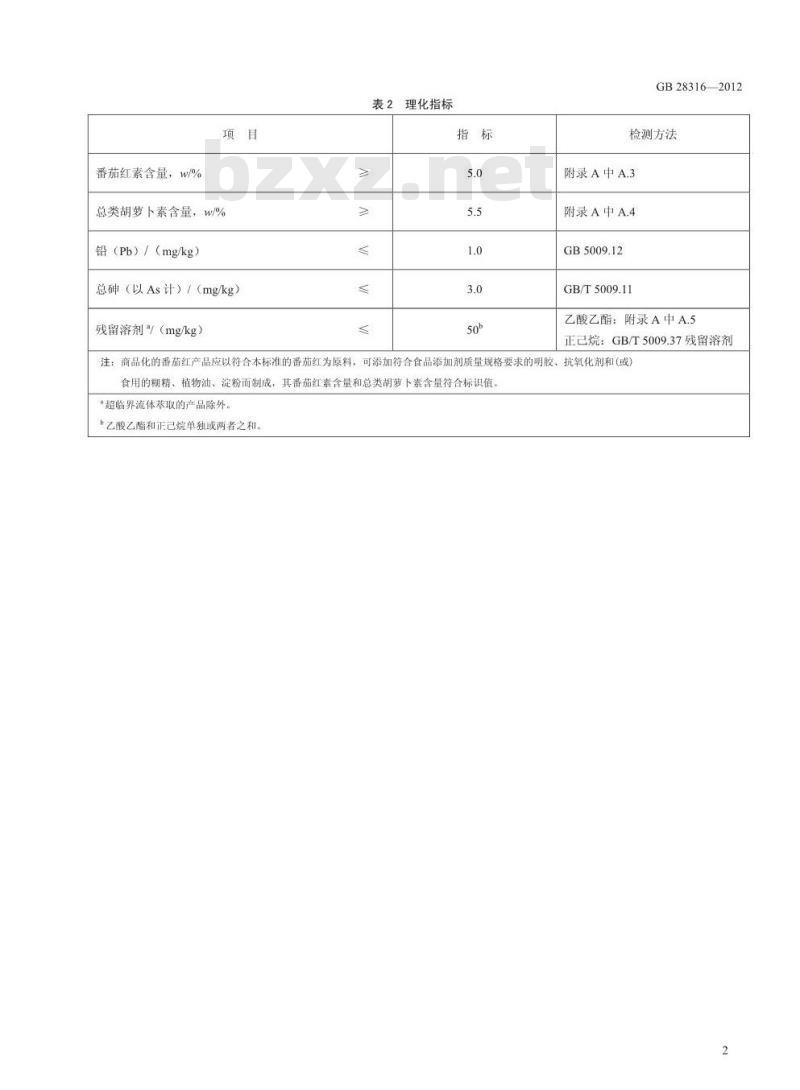
3.1感官要求:应符合表1的规定。表1感官要求
深红色
检验方法
取适量样品置于清洁、干燥的白瓷盘中,在膏状物或油状液体或粉末(晶体)3.2理化指标:应符合表2的规定。自然光线下,观察其色泽和状态1
番茄红素含量,w/%
总类胡萝卜素含量,w/%
铅(Pb)/(mg/kg)
总砷(以As计)/(mg/kg)
残留溶剂(mg/kg)
理化指标
GB283162012
检测方法
附录A中A.3
附录A中A.4
GB5009.12
GB/T5009.11
附录A中A.5
乙酸乙酯:
正已烷:GB/T5009.37残留溶剂
注:商品化的番茄红产品应以符合本标准的番茄红为原料,可添加符合食品添加剂质量规格要求的明胶、抗氧化剂和(或)食用的糊精、植物油、淀粉而制成,其番茄红素含量和总类胡萝卜素含量符合标识值。\超临界流体萃取的产品除外。b乙酸乙酯和正己烷单独或两者之和。2
A.1一般规定
附录A
检验方法
GB283162012
本标准所用试剂和水,在没有注明其他要求时,均指分析纯试剂和GB/T6682一2008中规定的三级水,试验中所用标准滴定溶液、杂质测定用标准溶液、制剂及制品,在没有注明其他要求时,均按GB/T601、GB/T602、GB/T603的规定制备。试验中所用溶液在未注明用何种溶剂配制时,均指水溶液。A.2鉴别试验
A.2.1溶解性
易溶于乙酸乙酯和正己烷,部分溶于乙醇和丙酮,不溶于水。A.2.2颜色反应
称取约0.01g试样,溶于10mL丙酮中,形成橙红色透明溶液,向其中连续滴加等体积的5%硝酸钠溶液(5g溶于100mL水中)和1mol/L硫酸溶液,试样溶液的颜色变浅。A.2.3特征吸收峰
取适量试样,溶于正已烷中,此试样溶液在446nm、472nm、505nm附近波长处有特征吸收峰。A.3番茄红素含量的测定
A.3.1试剂和材料
A.3.1.1二氯甲烷:色谱纯。
A.3.1.2乙睛:色谱纯。
A.3.1.3乙酸乙酯:色谱纯。
A.3.1.4水:一级水。
A.3.1.5乙醇。
A.3.1.6石油醚:沸程60℃~90℃。A.3.1.72,6-二丁基对甲酚(BHT)。A.3.1.8番茄红素对照品:纯度≥90%。A.3.2仪器和设备
A.3.2.1高效液相色谱仪。
A.3.2.2紫外-可见分光光度计。A.3.3参考色谱条件
A.3.3.1色谱柱:固定相为C18,250mm×4.6mm,5μm:或其他等效的色谱柱。A.3.3.2柱温:25℃。
A.3.3.3检测器:紫外/可见光检测器或二极管阵列检测器。A.3.3.4检测波长:472nm。
A.3.3.5流动相:流动相A为乙溶液(9+1),流动相B为乙酸乙酯。洗脱条件为二元线型梯度:流动相B在20min内由0%上升到100%,20min后流动相B保持100%运行5min。A.3.3.6流速:1.0mL/min。
A.3.3.7进样量:10uL。
A.3.4分析步骤
A.3.4.1BHT溶液的配制
GB283162012
准确称量2.5gBHT置于500mL棕色容量瓶中,用二氯甲烷定容,浓度为5000mg/L,密闭避光放置,可稳定储存3个月。
A.3.4.2番茄红素对照品溶液的配制分别称取10mg番茄红素对照品和20mgBHT,精确至0.0001g,取少量二氯甲烷溶解后,转移至100m棕色容量瓶中,用二氯甲烷定容,混合均匀。由于番茄红素不稳定,番茄红素对照品溶液使用前应采用A.3.4.3方法标定其纯度。番茄红素对照品溶液应在-20℃条件下储存,24h内可使用。A.3.4.3番茄红素对照品溶液的标定量取1mL(VA)番茄红素对照品溶液,置于50mL(VB)棕色容量瓶中,加入5mL乙醇和5mLBHT溶液,用石油醚定容,混匀。将此溶液置于1cm比色皿中,以石油醚作空白对照,用紫外-可见光分光光度计在472nm附近的最大吸收波长处测定吸光度。吸光度应控制在0.3~0.7之间,否则应调整溶液浓度,再重新测定吸光度。番茄红素对照品溶液中番茄红素浓度以csT计,单位为毫克每升(mg/L),按公式(A.1)计算:
式中:
Amax×D×10000
番茄红素对照品溶液在472nm附近的最大吸收波长处测得的吸光度值:稀释因子(VB/VA):
浓度换算因子;
番茄红素的吸光系数。
A.3.4.4标准曲线的制备
分别吸取适量番茄红素对照品溶液,用二氯甲烷稀释,并用棕色容量瓶定容,配制成浓度分别为1.0μg/mL、5.0μg/mL、10.0μg/mL、20.0μg/mL、30.0μg/mL、40.0μg/mL、50.0μg/mL系列的番茄红素标准溶液。在A.3.3参考色谱条件下,对系列的番茄红素标准溶液进行色谱分析,得到峰面积值-番茄红素浓度的标准曲线图。
A.3.4.5试样液的配制
取适量试样置于玻璃容器中,于60℃水浴中30min融化。称取融化后的试样1.0g~1.2g,精确至0.0001g,用少量二氯甲烷溶解后转移至100mL棕色容量瓶中,加入10mLBHT溶液,超声混匀,冷却至室温,用二氯甲烷定容。再取1mL置于50mL棕色容量瓶中,用二氯甲烷定容,混匀后用于高效液相色谱分析。
A.3.4.6测定wwW.bzxz.Net
在A.3.3参考色谱条件下,对试样液进行色谱分析,以保留时间和光谱特征定性,以试样中番茄红素组分峰面积与标准曲线比较定量。A.3.5结果计算
番茄红素含量以质量分数wi计,数值以%表示,按公式(A.2)计算:w=
式中:
m×1000×1000
根据标准曲线查得的试样液中番茄红素浓度的数值,单位为微克每毫升(μg/mL):V试样定容体积的数值,单位为毫升(mL):m—试样质量的数值,单位为克(g);1000X1000质量换算因子。
在重复性条件下获得的两次独立测定结果的绝对差值不得超过算术平均值的5%。.(A.2)
A.4总类胡萝卜素含量的测定
A.4.1试剂和材料
A.4.1.1二氯甲烷。
A.4.1.22.6-二叔基对甲酚(BHT)。A.4.1.3乙醇
A.4.1.4石油醚
GB283162012
A.4.1.5BHT溶液:准确称量2.5gBHT置于500mL棕色容量瓶中,用二氯甲烷定容,浓度为5000mg/L,密闭避光放置,可稳定储存3个月。A.4.2仪器和设备
紫外-可见光分光光度计。
A.4.3分析步骤
A.4.3.1试样液的制备
取适量试样置于玻璃容器中,60℃水浴30min融化。称取融化后的试样1.0g~1.2g,精确至0.0001g,取少量二氯甲烷溶解后置于100mL棕色容量瓶中,加入10mLBHT溶液,超声混匀,冷却至室温,二氯甲烷定容(溶液A)。从溶液A中转移5mL(Vc),置于50mL(Vp)棕色容量瓶中,二氯甲烷定容(溶液B)。转移2mL(Ve)溶液B置于100mL棕色容量瓶(Vp)中,添加10mL乙醇,石油醚定容,混合均匀,记作溶液C。
A.4.3.2测定
采用紫外-可见光分光光度计扫描,1cm比色皿,波长范围300nm~550nm,石油醚作空白,记录溶液C的最大吸光度(吸光度应控制在0.2~0.8之间)。A.4.3.3结果计算
总类胡萝卜素含量以番茄红素的质量分数W2计,数值以%表示,按公式(A.3)计算:W=
式中:
溶液C的最大吸光度值
试样质量的数值,单位为克(g);稀释因子[(VeXVp)(Ve×Vc)番茄红素的吸光系数。
ms×3450
.(A.3)
实验结果以平行测定结果的算术平均值为准。在重复性条件下获得的两次独立测定结果的绝对差值不得超过算术平均值的2%。
A.5乙酸乙酯的测定
A.5.1仪器和设备
配备顶空进样器和氢火焰离子检测器(FID)的气相色谱仪。A.5.2参考色谱条件
A.5.2.1色谱柱:交联键合5%二苯基~95%聚二甲基硅氧烷固定液的石英毛细管柱,30m×0.53mm,膜厚3.0um;或其他等效的色谱柱。A.5.2.2载气:氮气。
A.5.2.3载气流量:4.0mL/min。A.5.2.4进样口温度:180℃。
A.5.2.5柱温:73℃,保持5min,以25℃/min的速率升温至160℃,保持1min。A.5.2.6检测器温度:230℃。
A.5.2.7进样体积:1mL定量环。A.5.2.8分流比:1:6。
A.5.3顶空条件
A.5.3.1顶空瓶平衡温度及时间:70℃,120.0min。A.5.3.2定量环温度:100℃。
A.5.3.3传输线温度:110℃。
A.5.3.4混合方式:每30min搅拌1min。A.5.3.5加压时间:0.2min。
A.5.3.6定量环填充时间:0.2min。A.5.3.7定量环平衡时间:0.05min。A.5.3.8进样时间:1.0min
A.5.3.9顶空瓶压力:95.15kPa(13.8psi)。A.5.3.10进样量:1mL。
A.5.4分析步骤
A.5.4.1对照液制备
A.5.4.1.1乙酸乙酯购备液A(10.000mg/kg)GB283162012
在天平上放置一空量瓶,扣除瓶重后精密加入乙酸乙酯500mg,再精密加入邻苯二甲酸二乙酯使得溶剂量达到50.00g,精确至0.1mg,超声混勾。此溶液在室温环境下可稳定存放2个月。A.5.4.1.2乙酸乙酯贮备液B(100mg/kg)在天平上放置一空量瓶,扣除瓶重后精密加入乙酸乙酯贮备液A500mg,再精密加入邻苯二甲酸二乙酯使得溶剂量达到50.00g,精确至0.1mg,超声混匀。此溶液在室温环境下可稳定存放2个月。A.5.4.1.3乙酸乙酯标准溶液C(5mg/kg)在天平上放置一空顶空瓶,扣除瓶重后精密加入乙酸乙酯贮备液B500mg,再精密加入邻苯二甲酸二乙酯使得溶剂量达到10.00g,精确至0.1mg,放入1个12mm~15mm的磁力搅拌棒。密封,混匀。A.5.4.1.4乙酸乙酯标准溶液D(10mg/kg)在天平上放置一空顶空瓶,扣除瓶重后精密加入乙酸乙酯贮备液B1000mg,再精密加入邻苯二甲酸二乙酯使得溶剂量达到10.00g,精确至0.1mg,放入1个12mm~15mm的磁力搅拌棒。密封,混匀。A.5.4.1.5乙酸乙酯标准溶液E(17.5mg/kg)在天平上放置一空顶空瓶,扣除瓶重后精密加入乙酸乙酯贮备液B1750mg,再精密加入邻苯二甲酸二乙酯使得溶剂量达到10.00g,精确至0.1mg,放入1个12mm15mm的磁力搅拌棒。密封,混匀。A.5.4.1.6乙酸乙酯标准溶液F(25mg/kg)在天平上放置一空顶空瓶,扣除瓶重后精密加入乙酸乙酯贮备液B2500mg,再精密加入邻苯二甲酸二乙酯使得溶剂量达到10.00g,精确至0.1mg,放入1个12mm15mm的磁力搅拌棒。密封,混匀。A.5.4.2试样液制备
测定前,取约30g试样,加热至40°℃C~50°C,机械搅拌。趁热精密称取5000mg,置于1个预先称重的顶空瓶中,精密加入邻苯二甲酸二乙酯,使试样和溶剂的总重为10.00g,精确至0.1mg,放入1个12mm~15mm的磁力搅拌棒。密封,混匀。A.5.4.3测定
取乙酸乙酯标准溶液C、D、E、F和试样液,按A.5.3和A.5.2分别进样。A.5.5结果计算
乙酸乙酯含量以质量分数w计,数值以毫克每千克(mg/kg)表示,按公式(A.4)计算:6
式中:
CsT/AsT
试样液中乙酸乙酯色谱峰的峰面积;AsT
GB283162012
..(A.4)
根据乙酸乙酯标准溶液C、D、E、F相应浓度和峰面积计算得到的浓度/峰面积比的平均值试样液的总重,单位为克(g):
试样质量,单位为克(g)。
GB283162012
食品安全国家标准
食品添加剂
2012-04-25发布
番茄红
2012-06-25实施
中华人民共和国卫生部
1范围
食品安全国家标准
食品添加剂
番茄红
GB283162012
本标准适用于以番茄(Lycopersicon)或番茄制品为原料,以超临界流体(包括二氧化碳等)或有机溶剂为萃取介质制备的食品添加剂番茄红。2分子式、结构式、相对分子质量2.1分子式
番茄红素:C40H56
2.2结构式
2.3相对分子质量
全反式番茄红素化学结构式
536.87(按2007年国际相对原子质量)3技术要求
3.1感官要求:应符合表1的规定。表1感官要求
深红色
检验方法
取适量样品置于清洁、干燥的白瓷盘中,在膏状物或油状液体或粉末(晶体)3.2理化指标:应符合表2的规定。自然光线下,观察其色泽和状态1
番茄红素含量,w/%
总类胡萝卜素含量,w/%
铅(Pb)/(mg/kg)
总砷(以As计)/(mg/kg)
残留溶剂(mg/kg)
理化指标
GB283162012
检测方法
附录A中A.3
附录A中A.4
GB5009.12
GB/T5009.11
附录A中A.5
乙酸乙酯:
正已烷:GB/T5009.37残留溶剂
注:商品化的番茄红产品应以符合本标准的番茄红为原料,可添加符合食品添加剂质量规格要求的明胶、抗氧化剂和(或)食用的糊精、植物油、淀粉而制成,其番茄红素含量和总类胡萝卜素含量符合标识值。\超临界流体萃取的产品除外。b乙酸乙酯和正己烷单独或两者之和。2
A.1一般规定
附录A
检验方法
GB283162012
本标准所用试剂和水,在没有注明其他要求时,均指分析纯试剂和GB/T6682一2008中规定的三级水,试验中所用标准滴定溶液、杂质测定用标准溶液、制剂及制品,在没有注明其他要求时,均按GB/T601、GB/T602、GB/T603的规定制备。试验中所用溶液在未注明用何种溶剂配制时,均指水溶液。A.2鉴别试验
A.2.1溶解性
易溶于乙酸乙酯和正己烷,部分溶于乙醇和丙酮,不溶于水。A.2.2颜色反应
称取约0.01g试样,溶于10mL丙酮中,形成橙红色透明溶液,向其中连续滴加等体积的5%硝酸钠溶液(5g溶于100mL水中)和1mol/L硫酸溶液,试样溶液的颜色变浅。A.2.3特征吸收峰
取适量试样,溶于正已烷中,此试样溶液在446nm、472nm、505nm附近波长处有特征吸收峰。A.3番茄红素含量的测定
A.3.1试剂和材料
A.3.1.1二氯甲烷:色谱纯。
A.3.1.2乙睛:色谱纯。
A.3.1.3乙酸乙酯:色谱纯。
A.3.1.4水:一级水。
A.3.1.5乙醇。
A.3.1.6石油醚:沸程60℃~90℃。A.3.1.72,6-二丁基对甲酚(BHT)。A.3.1.8番茄红素对照品:纯度≥90%。A.3.2仪器和设备
A.3.2.1高效液相色谱仪。
A.3.2.2紫外-可见分光光度计。A.3.3参考色谱条件
A.3.3.1色谱柱:固定相为C18,250mm×4.6mm,5μm:或其他等效的色谱柱。A.3.3.2柱温:25℃。
A.3.3.3检测器:紫外/可见光检测器或二极管阵列检测器。A.3.3.4检测波长:472nm。
A.3.3.5流动相:流动相A为乙溶液(9+1),流动相B为乙酸乙酯。洗脱条件为二元线型梯度:流动相B在20min内由0%上升到100%,20min后流动相B保持100%运行5min。A.3.3.6流速:1.0mL/min。
A.3.3.7进样量:10uL。
A.3.4分析步骤
A.3.4.1BHT溶液的配制
GB283162012
准确称量2.5gBHT置于500mL棕色容量瓶中,用二氯甲烷定容,浓度为5000mg/L,密闭避光放置,可稳定储存3个月。
A.3.4.2番茄红素对照品溶液的配制分别称取10mg番茄红素对照品和20mgBHT,精确至0.0001g,取少量二氯甲烷溶解后,转移至100m棕色容量瓶中,用二氯甲烷定容,混合均匀。由于番茄红素不稳定,番茄红素对照品溶液使用前应采用A.3.4.3方法标定其纯度。番茄红素对照品溶液应在-20℃条件下储存,24h内可使用。A.3.4.3番茄红素对照品溶液的标定量取1mL(VA)番茄红素对照品溶液,置于50mL(VB)棕色容量瓶中,加入5mL乙醇和5mLBHT溶液,用石油醚定容,混匀。将此溶液置于1cm比色皿中,以石油醚作空白对照,用紫外-可见光分光光度计在472nm附近的最大吸收波长处测定吸光度。吸光度应控制在0.3~0.7之间,否则应调整溶液浓度,再重新测定吸光度。番茄红素对照品溶液中番茄红素浓度以csT计,单位为毫克每升(mg/L),按公式(A.1)计算:
式中:
Amax×D×10000
番茄红素对照品溶液在472nm附近的最大吸收波长处测得的吸光度值:稀释因子(VB/VA):
浓度换算因子;
番茄红素的吸光系数。
A.3.4.4标准曲线的制备
分别吸取适量番茄红素对照品溶液,用二氯甲烷稀释,并用棕色容量瓶定容,配制成浓度分别为1.0μg/mL、5.0μg/mL、10.0μg/mL、20.0μg/mL、30.0μg/mL、40.0μg/mL、50.0μg/mL系列的番茄红素标准溶液。在A.3.3参考色谱条件下,对系列的番茄红素标准溶液进行色谱分析,得到峰面积值-番茄红素浓度的标准曲线图。
A.3.4.5试样液的配制
取适量试样置于玻璃容器中,于60℃水浴中30min融化。称取融化后的试样1.0g~1.2g,精确至0.0001g,用少量二氯甲烷溶解后转移至100mL棕色容量瓶中,加入10mLBHT溶液,超声混匀,冷却至室温,用二氯甲烷定容。再取1mL置于50mL棕色容量瓶中,用二氯甲烷定容,混匀后用于高效液相色谱分析。
A.3.4.6测定wwW.bzxz.Net
在A.3.3参考色谱条件下,对试样液进行色谱分析,以保留时间和光谱特征定性,以试样中番茄红素组分峰面积与标准曲线比较定量。A.3.5结果计算
番茄红素含量以质量分数wi计,数值以%表示,按公式(A.2)计算:w=
式中:
m×1000×1000
根据标准曲线查得的试样液中番茄红素浓度的数值,单位为微克每毫升(μg/mL):V试样定容体积的数值,单位为毫升(mL):m—试样质量的数值,单位为克(g);1000X1000质量换算因子。
在重复性条件下获得的两次独立测定结果的绝对差值不得超过算术平均值的5%。.(A.2)
A.4总类胡萝卜素含量的测定
A.4.1试剂和材料
A.4.1.1二氯甲烷。
A.4.1.22.6-二叔基对甲酚(BHT)。A.4.1.3乙醇
A.4.1.4石油醚
GB283162012
A.4.1.5BHT溶液:准确称量2.5gBHT置于500mL棕色容量瓶中,用二氯甲烷定容,浓度为5000mg/L,密闭避光放置,可稳定储存3个月。A.4.2仪器和设备
紫外-可见光分光光度计。
A.4.3分析步骤
A.4.3.1试样液的制备
取适量试样置于玻璃容器中,60℃水浴30min融化。称取融化后的试样1.0g~1.2g,精确至0.0001g,取少量二氯甲烷溶解后置于100mL棕色容量瓶中,加入10mLBHT溶液,超声混匀,冷却至室温,二氯甲烷定容(溶液A)。从溶液A中转移5mL(Vc),置于50mL(Vp)棕色容量瓶中,二氯甲烷定容(溶液B)。转移2mL(Ve)溶液B置于100mL棕色容量瓶(Vp)中,添加10mL乙醇,石油醚定容,混合均匀,记作溶液C。
A.4.3.2测定
采用紫外-可见光分光光度计扫描,1cm比色皿,波长范围300nm~550nm,石油醚作空白,记录溶液C的最大吸光度(吸光度应控制在0.2~0.8之间)。A.4.3.3结果计算
总类胡萝卜素含量以番茄红素的质量分数W2计,数值以%表示,按公式(A.3)计算:W=
式中:
溶液C的最大吸光度值
试样质量的数值,单位为克(g);稀释因子[(VeXVp)(Ve×Vc)番茄红素的吸光系数。
ms×3450
.(A.3)
实验结果以平行测定结果的算术平均值为准。在重复性条件下获得的两次独立测定结果的绝对差值不得超过算术平均值的2%。
A.5乙酸乙酯的测定
A.5.1仪器和设备
配备顶空进样器和氢火焰离子检测器(FID)的气相色谱仪。A.5.2参考色谱条件
A.5.2.1色谱柱:交联键合5%二苯基~95%聚二甲基硅氧烷固定液的石英毛细管柱,30m×0.53mm,膜厚3.0um;或其他等效的色谱柱。A.5.2.2载气:氮气。
A.5.2.3载气流量:4.0mL/min。A.5.2.4进样口温度:180℃。
A.5.2.5柱温:73℃,保持5min,以25℃/min的速率升温至160℃,保持1min。A.5.2.6检测器温度:230℃。
A.5.2.7进样体积:1mL定量环。A.5.2.8分流比:1:6。
A.5.3顶空条件
A.5.3.1顶空瓶平衡温度及时间:70℃,120.0min。A.5.3.2定量环温度:100℃。
A.5.3.3传输线温度:110℃。
A.5.3.4混合方式:每30min搅拌1min。A.5.3.5加压时间:0.2min。
A.5.3.6定量环填充时间:0.2min。A.5.3.7定量环平衡时间:0.05min。A.5.3.8进样时间:1.0min
A.5.3.9顶空瓶压力:95.15kPa(13.8psi)。A.5.3.10进样量:1mL。
A.5.4分析步骤
A.5.4.1对照液制备
A.5.4.1.1乙酸乙酯购备液A(10.000mg/kg)GB283162012
在天平上放置一空量瓶,扣除瓶重后精密加入乙酸乙酯500mg,再精密加入邻苯二甲酸二乙酯使得溶剂量达到50.00g,精确至0.1mg,超声混勾。此溶液在室温环境下可稳定存放2个月。A.5.4.1.2乙酸乙酯贮备液B(100mg/kg)在天平上放置一空量瓶,扣除瓶重后精密加入乙酸乙酯贮备液A500mg,再精密加入邻苯二甲酸二乙酯使得溶剂量达到50.00g,精确至0.1mg,超声混匀。此溶液在室温环境下可稳定存放2个月。A.5.4.1.3乙酸乙酯标准溶液C(5mg/kg)在天平上放置一空顶空瓶,扣除瓶重后精密加入乙酸乙酯贮备液B500mg,再精密加入邻苯二甲酸二乙酯使得溶剂量达到10.00g,精确至0.1mg,放入1个12mm~15mm的磁力搅拌棒。密封,混匀。A.5.4.1.4乙酸乙酯标准溶液D(10mg/kg)在天平上放置一空顶空瓶,扣除瓶重后精密加入乙酸乙酯贮备液B1000mg,再精密加入邻苯二甲酸二乙酯使得溶剂量达到10.00g,精确至0.1mg,放入1个12mm~15mm的磁力搅拌棒。密封,混匀。A.5.4.1.5乙酸乙酯标准溶液E(17.5mg/kg)在天平上放置一空顶空瓶,扣除瓶重后精密加入乙酸乙酯贮备液B1750mg,再精密加入邻苯二甲酸二乙酯使得溶剂量达到10.00g,精确至0.1mg,放入1个12mm15mm的磁力搅拌棒。密封,混匀。A.5.4.1.6乙酸乙酯标准溶液F(25mg/kg)在天平上放置一空顶空瓶,扣除瓶重后精密加入乙酸乙酯贮备液B2500mg,再精密加入邻苯二甲酸二乙酯使得溶剂量达到10.00g,精确至0.1mg,放入1个12mm15mm的磁力搅拌棒。密封,混匀。A.5.4.2试样液制备
测定前,取约30g试样,加热至40°℃C~50°C,机械搅拌。趁热精密称取5000mg,置于1个预先称重的顶空瓶中,精密加入邻苯二甲酸二乙酯,使试样和溶剂的总重为10.00g,精确至0.1mg,放入1个12mm~15mm的磁力搅拌棒。密封,混匀。A.5.4.3测定
取乙酸乙酯标准溶液C、D、E、F和试样液,按A.5.3和A.5.2分别进样。A.5.5结果计算
乙酸乙酯含量以质量分数w计,数值以毫克每千克(mg/kg)表示,按公式(A.4)计算:6
式中:
CsT/AsT
试样液中乙酸乙酯色谱峰的峰面积;AsT
GB283162012
..(A.4)
根据乙酸乙酯标准溶液C、D、E、F相应浓度和峰面积计算得到的浓度/峰面积比的平均值试样液的总重,单位为克(g):
试样质量,单位为克(g)。
小提示:此标准内容仅展示完整标准里的部分截取内容,若需要完整标准请到上方自行免费下载完整标准文档。
标准图片预览:




- 其它标准
- 热门标准
- 国家标准
- GB/T38627-2020 信息技术 实时定位 磁定位数据接口
- GB/T8878—2014 棉针织内衣
- GB/T1182-2018 产品几何技术规范(GPS) 几何公差 形状、方向、位置和跳动公差标注
- GB175-2023 通用硅酸盐水泥
- GB/T12949-1991 滑动轴承覆有减摩塑料层的双金属轴套
- GB/T15349-1994 化学试剂 溴甲酚绿
- GB/T97.1-2002 平垫圈A级
- GB/T10125-2021 人造气氛腐蚀试验 盐雾试验
- GB/T228.1-2021 金属材料 拉伸试验 第1部分:室温试验方法
- GB/T43802-2024 绿色产品评价 物流周转箱
- GB/T42970-2023 半导体集成电路 视频编解码电路测试方法
- GB31094-2014 防爆电梯制造与安装安全规范
- GB50300-2013 建筑工程施工质量验收统一标准
- GB/T38987-2020 硬质合金螺旋孔棒材
- GB9178-1988 集成电路术语
- 行业新闻
请牢记:“bzxz.net”即是“标准下载”四个汉字汉语拼音首字母与国际顶级域名“.net”的组合。 ©2025 标准下载网 www.bzxz.net 本站邮件:wymp4wang@gmail.com