- 您的位置:
- 标准下载网 >>
- 标准分类 >>
- 农业行业标准(NY) >>
- NY/T 1026-2006 养蚕用药技术规程
标准号:
NY/T 1026-2006
标准名称:
养蚕用药技术规程
标准类别:
农业行业标准(NY)
标准状态:
现行-
发布日期:
2006-01-26 -
实施日期:
2006-04-01 出版语种:
简体中文下载格式:
.rar.pdf下载大小:
2.84 MB
部分标准内容:
1范围
养蚕用药技术规程
本标准规定了家蚕饲养过程中常用的蚕药种类、使用技术和药效生物检测方法。本标准适用于蚕药管理、使用和药效的生物检测。2规范性引用文件
NY/T1026—2006
下列文件中的条款通过本标准的引用而成为本标准的条款。凡是注明日期的引用文件,其随后所有的修改单(不包括勘误的内容)或修改版均不适用于本标准,然而,鼓励根据本标准达成协议的各方研究是否可使用这些文件的最新版本。凡是不注明日期的引用文件,其最新版本适用于本标准。中华人民共和国兽药典(2000年版)中华人民共和国兽药规范(1992)兽药管理条例(2004)
进口兽药质量标准(1999)
食品动物禁用的兽药及其他化合物清单(中华人民共和国农业部公告第193号)3术语和定义
下列术语和定义适用于本标准。3.1
家蚕silkworm
以桑叶为饲料,通过人工饲养,能分泌蚕丝、生产蚕茧的经济昆虫,行业管理习惯上称为桑蚕。3.2
蚕病silkwormdiseases
家蚕病害的总称。家蚕的病害,有病毒病、细菌病、真菌病、原生动物病、节肢动物病害、中毒症等种类。
蚕药chemicalsforsilkwormrearing养蚕用药的简称,指兽药中专门用于蚕室蚕具消毒、蚕病预防与治疗调节蚕生长发育的各类化学药品及其制剂。
消毒药剂disinfectant
用于杀灭养蚕环境中和附着在蚕体上的病原微生物,防治疾病发生和传染的药物,包括氯制剂、甲醛制剂和表面活性剂及其复配制剂等。3.3.2
5antibacterial drug
抗菌药
能够抑制或杀灭病原菌的药物,包括抗菌素及其制剂。3.3.3
抗寄生虫药antiparasiticdrug
能够杀灭或驱除蚕体内、体外寄生虫的化学药品。1
NY/T1026—2006
昆虫激素类似物insecthormoneanalogue用于调节家蚕生长发育的昆虫激素类似物4蚕药使用基本原则
4.1蚕药管理
4.1.1允许使用的药剂
养蚕过程中使用的药物,应符合中华人民共和国兽药典》、《中华人民共和国兽药规范》、《进口兽药质量标准》等的相关规定,并应来自具有兽药生产许可证和产品批准文号的生产企业,或者具有进口兽药许可证》的供应商。所用药物的标签应符合农业部发布的《兽药标签和说明书管理办法》。使用的药物,在规定条件下,应对家蚕生理无不良影响,其剂量、剂型、有效性和使用方法应达到不同蚕区防治蚕病的要求。此内容来自标准下载网
4.1.2禁止使用的药剂
禁止使用未经国家畜牧兽医行政管理部门批准的兽药或已经淘汰的兽药。严禁使用《食品动物禁用的兽药及其他化合物清单》中的药物及化合物。5蚕药药效的生物检测
在实际使用前,必要时可以参见附录A和附录B的方法对蚕药的药效进行生物检测。6蚕药使用技术方法
依据消毒、预防、治疗对象,选择相应蚕药,按照技术规程或使用说明,确保使用浓度、作用条件与作用时间。建立并保存全部用药纪录,包括蚕药品名、用药方式、用药量以及蚕期发病情况,以备后续参考。
6.1常用蚕药的种类
依据用途蚕药可分为消毒药、抗菌药、抗寄生虫药和昆虫激素类似物等。6.1.1消毒药剂
用于养蚕的消毒药剂主要有含氯消毒剂、醛制剂、石灰、表面活性剂等。含氟消毒剂主要有漂白粉(含氯石灰)、漂粉精、二氟异氰尿酸钠、三氟异氰尿酸和三氰异氰尿酸钠等:醛制剂主要有福尔马林(含甲醛35%40%和多聚甲醛等:表面活性剂主要有十二烷基二甲基苯甲基氯化铵、十二烷基二甲基苯甲基溴化铵、十二烷基三甲基漠化铵和十六烷基二甲基乙基溴化铵等。6.1.2抗菌药
用于养蚕的抗菌药主要有红霉素,硫氰酸红霉素和诺氟沙星等。6.1.3抗寄生虫药
用于养蚕的抗寄生虫药主要有灭蚕蝇等。6.1.4昆虫激素类似物
用于养蚕的昆虫激素类似物主要有蜕皮激素等。6.2蚕药使用技术方法
6.2.1蚕室、蚕具消毒
用于蚕室、蚕具消毒的主要药剂种类有:含氧消毒剂、醛制剂、石灰、表面活性剂及复方制剂等。使用药物消毒前,蚕室及周围环境应先行打扫干净,蚕具要清洗晒干后置于蚕室内,然后再使用消毒药剂进行消毒。养蚕结束后,为了消除养蚕过程中产生的病原体对养蚕环境的污染,应对蚕室、蚕具和养蚕废弃物进行消毒。消毒时,应根据消毒药剂的性质要求,保持一定的作用温度和作用时间,需要密闭消2
NY/T1026—2006
毒的应设法将蚕室密闭。小型用具、器具也可采用蒸煮、日晒等物理消毒方法进行消毒或浸人消毒液中浸渍消毒。
蚕室,蚕具及养蚕环境消毒常用消毒药剂及其使用方法参见附录C6.2.2蚕体蚕座消毒
为了预防养蚕过程中病原体的感染,尤其是蚕座内蚕病的交叉传染,必要时应使用蚕体蚕座消毒药剂进行蚕体蚕座消毒。常用的套体蚕座消毒药剂主要为复方含剥制剂,复方醛制剂和石灰粉等,用粉剂进行撒粉消毒,用熏烟剂进行熏烟消毒。蚕体蚕座消毒常用消毒药剂及其使用方法参见附录C。6.2.3预防和治疗药剂的使用
部分细菌性蚕病,可用抗菌药进行预防或治疗。养蚕生产上常用的抗菌药主要有红霉素、硫氰酸红霉素和诺氟沙星等。使用抗菌药时要严格遵守规定的用法和用量,同时要考虑交替用药,尽可能降低耐药性的产生。
蚕病预防与治疗常用药剂及其便用方法参见附录C。6.2.4寄生虫病的防治
通过使用药物可对养蚕过程中发生的寄生虫病进行防治。防治家蚕寄生虫病常用药物及其常用方法参见附录C。6.2.5调节蚕生长发育的昆虫激素类药物的使用慎用昆虫激素类药物。遇有桑叶出现余缺,以及为了促进上族齐一等目的,应使用昆虫激素类药物调节蚕生长发育时,应参见附录C所示的民虫激素类药物及其使用方法进行。6.2.6桑叶叶面消毒
在养蚕环境已受到微粒子病污染的地区,为防止食下传染,蚕种生产单位可采取桑叶叶面消毒的办法,以提高对微粒子病的防治效果。必要时,丝董育地区在小蚕共育期间,也可进行桑叶叶面消毒。桑叶叶面消毒,使用含氯消毒药剂。1龄~2龄期,使用有效氯含量为0.3%的消毒液,浸消5min左右,用清水漂洗除去残留在桑叶表面的消毒液,再经脱水、晾干后,即可给桑饲蚕;3龄~5龄期,使用有效氯含量为0.3%的消毒液,浸消8min,经清水漂洗、脱水、晾干后备用。7蚕病的综合防治
7.1饲养管理
蚕病防治以药剂消毒杀灭病原为主,实行多种技术措施配合综合防治。在对蚕室蚕具进行严格消毒的前提下,选择饲养体质强健好养、经济性状优良的蚕品种,加强饲养管理,合理喂饲富含营养物质的饲料,增强蚕体自身的抗病能力。做好桑园病虫害防治工作,防止交叉感染。需要应用药物进行预防治疗或使用激素类药物对蚕的生长发育进行调节时,应避免添食大量水剂。7.2病死蚕与养蚕废弃物处理
72、1病死看处理
为减少病原,养蚕全过程中发现的病死蚕应及时淘汰,并经消毒处理,以免蔓延扩散。被病蚕污染的蚕具、蚕网、防干纸等,应消毒清洗后方能使用。7.2.2蚕沙处理
残桑、蚕粪,应经消毒处理或经堆制充分发酵腐熟后,方可作为肥料施用。3
NY/T1026—2006
A.1适用范围
附录A
(资料性附录
蚕用消毒剂消毒效果生物检测方法本方法适用于蚕用消毒剂对各种物体的消毒效果评价。A.2理化指标
将消毒剂置20℃主2℃温度(或推荐使用温度)下,测定在使用浓度下杀灭指示微生物达到消毒或灭菌所需的最短时间(min)。
A.3指示微生物
A.3.1细菌
A.3.1.1细菌繁殖体:黑胸败血病菌(Bacillussp.)、黏质沙雷氏菌(SerratiamarcescensBizio)。A.3.1.2细菌芽孢:苏芸金芽孢杆菌猝倒亚种(Bacillusthuringiensis subsp,sotoIshiwata)芽孢。A.3.2真菌
A.3.2.1球孢白僵菌[Beauveriabassiana(Bals.)Vuill.A.3.2.2菜氏野村菌[Nomuraearilevi(Farlow)Samson]。A.3.2.3黄曲霉(AspergillusflauusLink)。A.3.3病毒
A.3.3.1家蚕核型多角体病毒(Bambyrc moriNuclearPolyhedrosisVirus,BmNPV)多角体(polyhedron)。A.3.3.2家蚕质型多角体病毒(BombyxmoriCytoplasmicPolyhedrosisVirus,BmCPV)多角体。A.3.4原生动物
A.3.4.1家蚕微粒子虫(NosemabombyeisNaegeli)孢子。A.4检测方法
A.4.1中和剂中和效果试验
A.4.1.1中和剂的选择
为了正确评价消毒剂对微生物的杀灭作用,消毒试验中要求选择适当的中和剂。所选中和剂不仅要能及时中止消毒剂杀灭微生物的作用,且中和剂本身及其与消毒剂的反应产物(下称中和产物)应对微生物无抑制或杀灭作用,并对培养基无不良影响。要选用注明生产厂家、批号的中和剂。A.4.1.2培养基与试剂
A.4.1.2.1普通营养琼脂培养基
成分!
蛋白陈
牛肉膏
氰化钠
蒸馏水
1000ml
NY/T1026—2006
制法:除琼脂外,其他成分溶解于蒸馏水中,调pH至7.2~7.4,加入琼脂后加热溶解,过滤分装,经121C压力蒸汽灭菌30min,备用。A.4.1.2.20.03mol/L磷酸盐缓冲液(pH7.2~7.4,下称PBS)成分:
磷酸氢二钠
磷酸二氢钾
蒸馏水
1000ml
制法:将磷酸氢二钠和磷酸二氢钾溶解于蒸馏水中,pH7.2~7.4,分装,经121℃压力蒸汽灭菌30min,备用。
A.4.1.3器材
A.4.1.3.1锥形烧瓶。
A.4.1.3.2
平皿:直径9cm
量筒。
A.4.1.3.3
A.4.1.3.4
A.4.1.3.5
精密pH试纸。
无菌试管。
5无菌刻度吸管:1.0ml,5.0ml,10.0ml。A.4.1.3.6
A.4.1.3.7
恒温培养箱。
A.4.1.3.8
冰箱。
A.4.1.3.9
菌落计数器。
A.4.1.3.10
酒精灯。
A.4.1.4操作方法
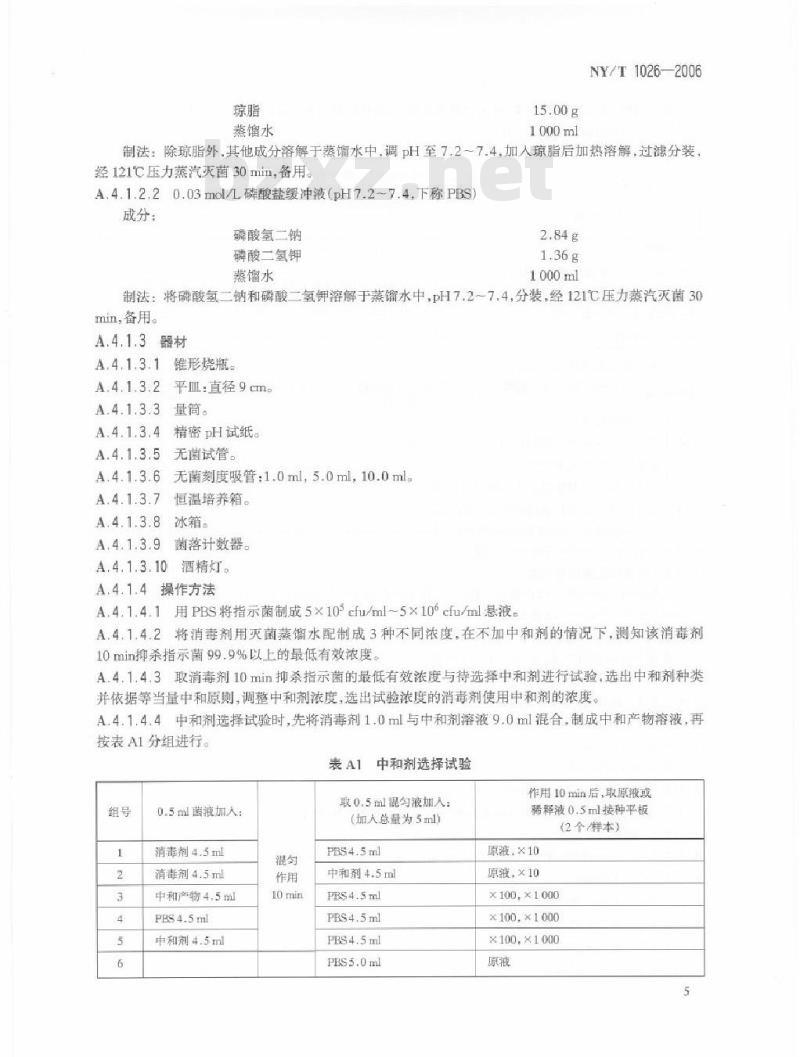
A.4.1.4.1用PBS将指示菌制成5x10°cfu/ml~5x10%cfu/ml悬液。A.4.1.4.2将消毒剂用灭菌蒸馏水配制成3种不同浓度,在不加中和剂的情况下,测知该消毒剂10min抑杀指示菌99.9%以上的最低有效浓度。A.4.1.4.3取消毒剂10min抑杀指示菌的最低有效浓度与待选择中和剂进行试验,选出中和剂种类并依据等当量中和原则,调整中和剂浓度,选出试验浓度的消毒剂使用中和剂的浓度。A.4.1.4.4中和剂选择试验时,先将消毒剂1.0ml与中和剂溶液9.0ml混合,制成中和产物溶液,再按表A1分组进行。
中和剂选择试验
取0.5ml混勾液加人:
0.5ml菌液加人:
消毒剂4.5ml
消毒剂4.5ml
中和产物4.5m
中和剂4.5ml
(加人总量为5ml)
中和剂4.5ml
作用10min后,取原液或
稀释液0.5ml接种平板
(2个/样本)
原液,x10
原液,×10
X100,X1000
x100,×1000
X100,X1000
NY/T1026—2006
然后,倾注平板置37℃培养48h,计数菌落数,按稀释倍数计算出回收菌数(cfu/ml)。A.4.1.5中和试验结果报告方法
按表A2进行。
中和剂
1%卵磷脂
1%卵磷脂+0.1%聚山梨醇-80(吐温80)
1%聚山醇-80(吐温-80)
0.5%硫代硫酸钠
中和试验结果举例
各组回收菌落数,cfu/ml
4.67×1064.83×1004.11×106
794 5.81×106 5.89x106 5.78x1061943.31×10%5.31x105.21×1051323.20×1065.03x105.8×10
第3.4.5组间误差率
3.4.5组误差率按公式(A1)计算
误差率(%)=(三组均数-3组菌数发|+|三组均数-4组菌数|+|三组均数-5组菌数\\)=3×100(A1)三组均数
A.4.1.6判定标准
A.4.1.6.1第3、4、5组菌数相似,其误差率≤10%。A.4.1.6.2第6组无菌生长。
A.4.1.6.3第2组菌数明显少于第3、4.5组。A,4.1.6.4第1组不长菌或明显少于第2组。符合上述标准的中和剂表明可消除消毒剂对指示菌的作用,中和剂及其与消毒剂的中和产物对指示菌无毒害,判定为该消毒剂的中和剂。A.4.2消毒剂定量消毒试验
定量消毒试验是测定受消毒因子作用后,样本残存微生物数量的试验方法。以杀灭率或灭活率表示结果,用于对消毒剂杀灭效果的评价。A.4.2.1培养基
普通营养琼脂培养基,按A.4.1.2.1制备。A.4.2.2试剂
A.4.2.2.1稀释液:含1%蛋白陈的0.03mol/LPBS(pH7.2~7.4)。A.4.2.2.2灭菌蒸馏水。
A.4.2.2.3中和剂
按A.4.1进行选择。
A.4.2.2.40.03mol/LPBS(pH7.2~7.4)。A.4.2.2.5洗脱液:含中和剂、1%蛋白陈、0.1%聚山梨醇-80的PBSA.4.2.3器材
A.4.2.3.1灭菌刻度吸管:1.0ml,5.0ml,10.0ml。A.4.2.3.2无菌试管。
A.4.2.3.3灭菌三角烧瓶。
灭菌平皿(直径9cm)。
A.4.2.3.4
A.4.2.3.5
恒温水浴箱。
A.4.2.3.6恒温培养箱。
A.4.2.3.7酒精灯。
A.4.2.3.8菌落计数器。
A.4.2.3.9微量进样器。
NY/T1026-2006
A.4.2.3.10载体:根据需要及试验目的选用经脱脂处理0.5cm×1.0cm大小的布片、纸片、玻片、橡胶片、塑料片、不锈钢片或铝片。A.4.2.4试验方法
A.4.2.4.1定量悬浮试验
采用定量悬浮试验评价消毒剂杀菌效果及其影响因素。将一定量的细菌悬液加人消毒剂溶液中,作用一定时间,去除残留的消毒剂后,采取消毒液一细菌混合物样本,接种于营养琼脂固体培养基上,经培养后检查其存活菌数,与未经消毒剂作用的对照菌数相比较,计算出杀菌效果。消毒对象为家蚕病毒(BmNPV和BmCPV)多角体和微粒子虫(Nasemabom-bucis)孢子时,将消毒液一多角体或微粒子虫孢子混合物样本,涂抹于定量桑叶后,经口接种于家蚕二龄起蚕,饲养一定时间后,记录统计发病死亡率,计算半数感染剂量IDs0,与未经消毒剂作用的对照组相比较,计算出消毒效果。试验时,根据消毒剂的特性和消毒对象,确定供试指示微生物的种类。A.4.2.4.1.1配制试验菌液:用无菌蒸馏水或磷酸盐缓冲液,将菌液稀释至5×105cfu/ml~5×10gcfu/ml。如消毒对象是病毒多角体或微粒子虫孢子,则将其稀释至10°个/mlA.4.2.4.1.2配制消毒液溶液:将消毒剂用蒸馅水稀释成3个不同浓度,每个浓度4.5ml,放20土2℃水浴中。
A.4.2.4.1.3待试管内液体温度与水浴温度平衡后,吸取试验菌液(或病毒多角体、微粒子虫孢子悬液)0.5ml,加入消毒剂溶液内,混匀,立即计时,此时菌一药混合液含菌量为5×10cfu/ml~5×105cfu/ml,或10°个/ml多角体(或微粒子虫孢子)。A.4.2.4.1.4分别于4个不同间隔时间,各取0.5ml菌一药混合波移入4.5ml中和剂中混勾。A.4.2.4.1.5中和10min,作适当释后进行活菌计数:接种平板,细菌放37C温箱内培养24h~48h后计数菌落;白僵菌25℃、曲霉菌30℃,培养48h后观察初步结果,继续观察一周止。A.4.2.4.1.6如消毒对象是多角体或微粒子虫孢子,则将中和后的混合液逐级稀释后涂抹于桑叶,定量喂于二龄起蚕,每区设3个重复。根据各种蚕病潜伏期的长短,饲养一定时间(核形多角体病3d5d,微粒子病7d~10d,质形多角体病7d~12d),饲养过程中随时注意病蚕的发病情况,做好病蚕的隔离消毒工作,防止交叉感染。根据各种病的发病症状并结合显微镜进行逐条检查,记录阳性率,按式(A2)计算对照组和试验组的ID50gIDs的对数=L-d(S-0.5)
式中:
L为最低稀释倍数的对数;
d为稀释度间差的对数;
S为各稀释列的阳性率(发病蚕数/接种蚕数)之和。+*....(A2)
A.4.2.4.1.7阳性对照,以洗脱液代替消毒液,同时按A.4.2.4.1.2~A.4.2.4.1.6进行。A.4.2.4.1.8按不同稀释度推算出每个样本存活菌数(cfu/ml),按式(A3)计算杀灭率:如消毒对象是病毒多角体或微粒子虫孢子时,按式(A4)计算灭活率。杀灭率(%)=对照组存适菌数在试验组存活菌数×100对照组存活菌数
以上计算必须将对照组生长菌数和消毒组生长菌数换算成相同稀释度后,然后代人公式。灭活:%-对照组照组试验组1..
对照组IDs0
NY/T1026—2006
A.4.2.4.1.9试验重复5次。
A.4.2.4.2定量载体试验
将一定量的病原微生物污染在载体上,然后将染菌载体暴露于消毒剂,作用一定时间后,将载体放人中和液内洗菌,稀释,进行活菌计数或对蚕体感染力测试,并与未经消毒的对照载体比较,计算出杀灭率。
A.4.2.4.2.1将灭菌载体平放于平皿内,每个载体滴注定量菌液(载体回收菌量达5×10cfu/片~5x10°cfu/片),涂匀,放37℃培养箱待干。A.4.2.4.2.2用灭菌蒸馏水将消毒剂稀释成3个不同浓度,各吸取5ml分别加入3个试管内,置于20℃水浴中,或恒温箱内。
A.4.2.4.2.3待试管内液体温度与水浴温度平衡后,加入染菌载体,作用至规定时间,将染菌载体移人含中和剂的5ml洗脱液试管内,中和10min,振荡80次,适当稀释,接种两个平板,放37℃C培养24h~48h,进行活菌计数。球孢白僵菌25℃、曲霉菌30℃,培养48h后观察初步结果,继续观察一周止。A.4.2.4.2.4如消毒对象是多角体或微粒子虫孢子,则按A.4.2.4.1.6进行。A.4.2.4.2.5阳性对照,以洗脱液代替消毒液按A.4.2.4.2.2~A.4.2.4.2.4进行。A.4.2.4.3表面消毒试验
将一定量的特定微生物污染在载体或物体表面,然后将染菌(包括细菌繁殖体和芽孢、微粒子虫孢子、病毒多角体,真菌分生孢子等)载体暴露于消毒因子中,作用一定时间后,用含有中和剂的稀释液回收残留于载体或物体表面上的微生物,与对照组菌数比较,计算杀灭率。如消毒对象为家蚕病原多角体或微粒子虫孢子,则将回收的微生物经口接种于蚕体,调查感染发病率,与对照组比较,计算灭活率。A.4.2.4.3.1染菌样片的制备:试验前将布片、铝片、玻璃片、纸片、竹片等有代表性的材料制成0.5cm×1.0cm或1cm×1cm、1.5cm×1.5cm的样片,用洗衣粉煮沸后用自来水冲洗、晾干、经高压灭菌备用。染菌方法有滴染、浸染和喷染三种。染菌量一般控制在每片5×105个~5×10°个。A.4.2.4.3.1.1滴染法将灭菌后的样片平放于无菌平皿内,每个样片加0.01ml~0.02ml菌液,涂匀。菌片于37℃温箱烘干,备用。繁殖体菌片现用现制备,芽孢菌片在4℃下,有效期不超过6个月。病毒多角体,微粒子虫孢子和真菌分生孢子菌片提前1d~3d制备,自然条件下阴干。A.4.2.4.3.1.2浸染法将灭菌样片平放于灭菌平血内,加人菌液,以样片全部浸湿为度。30min后,用无菌镊子将菌片移至另一垫有灭菌滤纸的平血内,于37℃温箱烘干、备用。A.4.2.4.3.1.3喷雾染菌法用气溶胶喷雾器将预先制备好的菌液在密闭的染菌柜内喷雾数分钟。喷雾完毕后静止1min,待大粒子沉降后,将样片由柜下方的抽屈送人柜内,使细菌微粒均勾沉降在样片上(一般为15min)。
A.4.2.4.3.2将试验菌片放在合适的部位,当测定烟雾熏蒸或喷雾熏蒸等消毒试验时,将菌片放于室内有代表性的地点,例如地面、桌面、窗面、墙壁等。经消毒预定时间后,将菌片放人装有5ml无菌蒸馅水或0.03M磷酸盐缓冲液(如消毒因子为消毒剂,则可根据消毒剂种类加入相应的中和剂)的试管中。将试管用力振荡80次,以洗下菌片上的残留微生物,用吸管吸取原液或适当倍数的稀释液接种平板,作活菌计数。
A.4.2.4.3.3如消毒对象是多角体或微粒子虫孢子,则按A.4.2.4.1.6进行。A.4.2.4.3.4阳性对照,不作消毒处理,按A.4.2.4.3.1~A.4.2.4.3.3进行。A.4.2.4.3.5按式(A5)计算杀灭率,按式(A4)计算灭活率。杀灭率(%)=对照组菌片整菌鳌片遭囊细菌片回收菌数×100对照组菌片回收菌数
O ........ (A5)
如消毒对象为家蚕病原多角体或微粒子虫孢子,消毒效果则用灭活率来表示。灭活率的计算方法8
同“定量悬浮试验”。
A.4.3有机物保护试验
NY/T10262006
通过有机物保护试验,测定消毒剂对有机物保护条件下的微生物的杀灭作用,以杀灭率表示,其结果与该消毒剂定量消毒试验相比较,用于评价有机物对消毒剂的杀菌能力的影响。A.4.3.1培养基与试剂
A.4.3.1.1普通营养琼脂培养基:按A.4.1.2.1制备。A.4.3.1.2试剂
A.4.3.2.2.1稀释液:同A.4.2.2.1。A.4.3.2.2.2灭菌蒸馏水。
A.4.3.2.2.3中和剂:按A.4.1进行选择。A.4.3.2.2.40.03mol/LPBSpH7.2~7.4)。A.4.3.2.2.5洗脱液:含1%蛋白陈、0.1%聚山梨醇-80的生理盐水。A.4.3.2.2.6小牛血清加人菌悬液中,使其最终浓度为10%。A.4.3.2器材
同A.4.2.3。
A.4.3.3试验方法
A.4.3.3.1实验前预先将菌液进行活菌计数,用稀释液稀释,加入小牛血清,使其最终浓度为10%,含菌数为5×105cfu/ml~5×10°cfu/ml,以此作为试验菌悬液。A.4.3.3.2以下步骤同A.4.2.4.1.2~A.4.2.4.1.9。A.4.3.4结果判定
A.4.3.4.15次试验的杀灭率均大于99.9%所需最低浓度和最短时间,判为该消毒剂在有机物存在下,可以达到消毒的有效浓度和时间。A.4.3.4.2此有效浓度和时间与定量消毒试验达到消毒的有效浓度和时间相同或相近,判为有机物对消毒剂杀菌作用无明显影响。达到消毒最低有效浓度增加1倍以上或最短作用时间延长1倍以上者可视为有明显影响。
A.5消毒效果的评价
A.5.1对细菌和真菌的杀灭率≥99.9%,对病毒多角体和家蚕微粒子虫孢子的灭活率≥99.0%,可判为消毒合格。
A.5.2在实际应用中消毒效果的评价以有机物保护试验的最低浓度和最短时间为该消毒剂达到实用消毒所需的浓度和时间。
A.5.3注明采用何种试验方法。
NY/T1026—2006
B.1适用范围
附录B
(资料性附录)
蚕用抗微生物药物生物检测方法本方法适用于蚕用抗微生物药物对家蚕细菌病防治效果评价。B.2理化指标
在25℃土2℃条件下,测定各种抗微生物药物达到有效治疗家蚕细菌病的最低剂量和时间。B.3
3指示微生物
B.3.1细菌
B.3.1.1细菌繁殖体:黑胸败血病菌(Bacillussp.)、黏质沙雷氏菌(SerratiamarcescensBizio)、青头败血病菌(Aeromonassp)肠球菌(Enterococcusfaecalis或Enterocaccusfaecium)。B.3.1.2细菌芽孢:苏芸金芽孢杆菌猝倒亚种(Bacillusthuringiensis subsp.sottoIshiwata)。B.4检测方法
B.4.1抗微生物药物体外抑菌(杀菌)试验抗微生物药物体外抑菌(杀菌)试验是测定受抗微生物药物作用后的样本有无微生物生长的试验方法。该试验适用于对抗微生物药物抑菌(杀菌)效果的初步评价。B.4.1.1培养基
B.4.1.1.1普通营养琼脂培养基:按A.4.1.2.1制备。B.4.1.1.2普通肉汤培养基
B.4.1.2.2.1成分:
蛋白藤
氟化钠
肉浸液
1000ml
B.4.1.2.2.2制法:取蛋白陈、氯化钠加肉浸液内。微温溶解,调pH至弱碱性,煮沸、滤清,调节pH使灭菌后为7.2-7.4压力燕汽灭菌备用。B.4.1.2试剂
B.4.1.2.1稀释液:含1%蛋白陈的0.03mol/LPBS(pH7.2~7.4)。B.4.1.2.2灭菌蒸馏水
B.4.1.3器材
B.4.1.3.1灭菌刻度吸管:1.0ml,5.0ml,10.0ml。B.4.1.3.2
灭菌试管
B.4.1.3.3
3灭菌三角烧瓶。
B.4.1.3.4酒精灯。
B.4.1.3.5恒温水浴箱。
B.4.1.3.6恒温培养箱。
B.4.1.4试验方法
B.4.1.4.1最小抑首浓度(MIC)的测定NY/T10262006
B.4.1.4.1.1将逐步降低浓度的抗微生物药物溶液(通常采用1:2稀释)和等量的双倍浓度的营养肉汤相混合,然后用0.1ml试验菌的培养物接种各试管,使其含菌量为10°cfu/ml左右。B.4.1.4.1.2接种后的试管,在37℃下培养24h,观察有无细菌生长B.4.1.4.2最小杀菌浓度(MBC)的测定B.4.1.4.2.1在MIC试验的基础上进行。将MIC试验中无细菌生长的各管培养液0.1ml转接于不含抗微生物药物的普通营养琼脂培养基平血表面。B.4.1.4.2.2接种后的平血在37℃下培养24h48h,观察有无细菌生长,B.4.1.4.3试验重复3次。
B.4.1.5结果判定
B.4.1.5.1肉汤培养时,以抑制微生物生长的最低药物浓度为MIC值。B.4.1.5.2平血皿培养时以细菌减少99.9%的最低药物浓度为MBC值B.4.2抗微生物药物临床试验
通过抗微生物药物临床试验,测定受抗微生物药物作用后的蚕体有无感染发病。该试验适用于对抗微生物药物实际使用效果的评价。B.4.2.1培养基
B.4.2.1.1普通营养琼脂培养基:按A.4.1.2.1制备。B.4.2.1.2普通肉汤培养基:按B.4.1.1.2制备。B.4.2.2试剂:同B.4.1.2。
B.4.2.3器材
B.4.2.3.1灭菌刻度吸管:1.0ml,5.0ml,10.0mlB.4.2.3.2灭菌试管。
B.4.2.3.3灭菌三角烧瓶。
B.4.2.3.4酒精灯。
B.4.2.3.5接种针。
B.4.2.3.6恒温培养箱。
B.4.2.4试验方法
B.4.2.4.1用稀释液将肉汤培养或平皿培养的菌液稀释计数,使其含菌量为10°cfu/ml左右。B.4.2.4.2药物试验组一般设高、中(推荐剂量)低三个剂量组B.4.2.4.3空白对照组即不感染不给药组。B.4.2.4.4阳性对照组即感染不给药组。B.4.2.4.5药物对照组选择与试验药物具有可比性的同类或同效药物,按常规剂量给药。B.4.2.4.6用经酒精灯火焰灭菌的接种针蘸取少量菌液给四龄或五龄起蚕进行穿刺接种,或将菌液均匀涂抹于定量桑叶叶面给蚕进行经口接种,每个处理40头一50头蚕,重复3区。B.4.2.4.7接种后进行给药处理,按推荐的临床给药途径给药11
NY/T1026—2006
B.4.2.4.8按常规的饲养方法进行饲养观察,调查各处理的发病死亡情况,记录发病死亡率。B.4.2.4.9按式(B1)计算有效率。有效率%)阻性对照组发瘤率药物基验组发病死亡率10(B1)阳性对照组发病死亡率
0试验重复3次,统计平均有效率。B.4.2.4.10
B.4.2.5结果判定
B.4.2.5.1阳性对照组发病死亡率≥95.0%。2以平均有效率≥95.0%判定该抗微生物药物治疗有效。B.4.2.5.2
B.5治疗效果的评价
B.5.1计算有效率,平均有效率≥95.0%判定为该抗微生物药物治疗有效12
小提示:此标准内容仅展示完整标准里的部分截取内容,若需要完整标准请到上方自行免费下载完整标准文档。
养蚕用药技术规程
本标准规定了家蚕饲养过程中常用的蚕药种类、使用技术和药效生物检测方法。本标准适用于蚕药管理、使用和药效的生物检测。2规范性引用文件
NY/T1026—2006
下列文件中的条款通过本标准的引用而成为本标准的条款。凡是注明日期的引用文件,其随后所有的修改单(不包括勘误的内容)或修改版均不适用于本标准,然而,鼓励根据本标准达成协议的各方研究是否可使用这些文件的最新版本。凡是不注明日期的引用文件,其最新版本适用于本标准。中华人民共和国兽药典(2000年版)中华人民共和国兽药规范(1992)兽药管理条例(2004)
进口兽药质量标准(1999)
食品动物禁用的兽药及其他化合物清单(中华人民共和国农业部公告第193号)3术语和定义
下列术语和定义适用于本标准。3.1
家蚕silkworm
以桑叶为饲料,通过人工饲养,能分泌蚕丝、生产蚕茧的经济昆虫,行业管理习惯上称为桑蚕。3.2
蚕病silkwormdiseases
家蚕病害的总称。家蚕的病害,有病毒病、细菌病、真菌病、原生动物病、节肢动物病害、中毒症等种类。
蚕药chemicalsforsilkwormrearing养蚕用药的简称,指兽药中专门用于蚕室蚕具消毒、蚕病预防与治疗调节蚕生长发育的各类化学药品及其制剂。
消毒药剂disinfectant
用于杀灭养蚕环境中和附着在蚕体上的病原微生物,防治疾病发生和传染的药物,包括氯制剂、甲醛制剂和表面活性剂及其复配制剂等。3.3.2
5antibacterial drug
抗菌药
能够抑制或杀灭病原菌的药物,包括抗菌素及其制剂。3.3.3
抗寄生虫药antiparasiticdrug
能够杀灭或驱除蚕体内、体外寄生虫的化学药品。1
NY/T1026—2006
昆虫激素类似物insecthormoneanalogue用于调节家蚕生长发育的昆虫激素类似物4蚕药使用基本原则
4.1蚕药管理
4.1.1允许使用的药剂
养蚕过程中使用的药物,应符合中华人民共和国兽药典》、《中华人民共和国兽药规范》、《进口兽药质量标准》等的相关规定,并应来自具有兽药生产许可证和产品批准文号的生产企业,或者具有进口兽药许可证》的供应商。所用药物的标签应符合农业部发布的《兽药标签和说明书管理办法》。使用的药物,在规定条件下,应对家蚕生理无不良影响,其剂量、剂型、有效性和使用方法应达到不同蚕区防治蚕病的要求。此内容来自标准下载网
4.1.2禁止使用的药剂
禁止使用未经国家畜牧兽医行政管理部门批准的兽药或已经淘汰的兽药。严禁使用《食品动物禁用的兽药及其他化合物清单》中的药物及化合物。5蚕药药效的生物检测
在实际使用前,必要时可以参见附录A和附录B的方法对蚕药的药效进行生物检测。6蚕药使用技术方法
依据消毒、预防、治疗对象,选择相应蚕药,按照技术规程或使用说明,确保使用浓度、作用条件与作用时间。建立并保存全部用药纪录,包括蚕药品名、用药方式、用药量以及蚕期发病情况,以备后续参考。
6.1常用蚕药的种类
依据用途蚕药可分为消毒药、抗菌药、抗寄生虫药和昆虫激素类似物等。6.1.1消毒药剂
用于养蚕的消毒药剂主要有含氯消毒剂、醛制剂、石灰、表面活性剂等。含氟消毒剂主要有漂白粉(含氯石灰)、漂粉精、二氟异氰尿酸钠、三氟异氰尿酸和三氰异氰尿酸钠等:醛制剂主要有福尔马林(含甲醛35%40%和多聚甲醛等:表面活性剂主要有十二烷基二甲基苯甲基氯化铵、十二烷基二甲基苯甲基溴化铵、十二烷基三甲基漠化铵和十六烷基二甲基乙基溴化铵等。6.1.2抗菌药
用于养蚕的抗菌药主要有红霉素,硫氰酸红霉素和诺氟沙星等。6.1.3抗寄生虫药
用于养蚕的抗寄生虫药主要有灭蚕蝇等。6.1.4昆虫激素类似物
用于养蚕的昆虫激素类似物主要有蜕皮激素等。6.2蚕药使用技术方法
6.2.1蚕室、蚕具消毒
用于蚕室、蚕具消毒的主要药剂种类有:含氧消毒剂、醛制剂、石灰、表面活性剂及复方制剂等。使用药物消毒前,蚕室及周围环境应先行打扫干净,蚕具要清洗晒干后置于蚕室内,然后再使用消毒药剂进行消毒。养蚕结束后,为了消除养蚕过程中产生的病原体对养蚕环境的污染,应对蚕室、蚕具和养蚕废弃物进行消毒。消毒时,应根据消毒药剂的性质要求,保持一定的作用温度和作用时间,需要密闭消2
NY/T1026—2006
毒的应设法将蚕室密闭。小型用具、器具也可采用蒸煮、日晒等物理消毒方法进行消毒或浸人消毒液中浸渍消毒。
蚕室,蚕具及养蚕环境消毒常用消毒药剂及其使用方法参见附录C6.2.2蚕体蚕座消毒
为了预防养蚕过程中病原体的感染,尤其是蚕座内蚕病的交叉传染,必要时应使用蚕体蚕座消毒药剂进行蚕体蚕座消毒。常用的套体蚕座消毒药剂主要为复方含剥制剂,复方醛制剂和石灰粉等,用粉剂进行撒粉消毒,用熏烟剂进行熏烟消毒。蚕体蚕座消毒常用消毒药剂及其使用方法参见附录C。6.2.3预防和治疗药剂的使用
部分细菌性蚕病,可用抗菌药进行预防或治疗。养蚕生产上常用的抗菌药主要有红霉素、硫氰酸红霉素和诺氟沙星等。使用抗菌药时要严格遵守规定的用法和用量,同时要考虑交替用药,尽可能降低耐药性的产生。
蚕病预防与治疗常用药剂及其便用方法参见附录C。6.2.4寄生虫病的防治
通过使用药物可对养蚕过程中发生的寄生虫病进行防治。防治家蚕寄生虫病常用药物及其常用方法参见附录C。6.2.5调节蚕生长发育的昆虫激素类药物的使用慎用昆虫激素类药物。遇有桑叶出现余缺,以及为了促进上族齐一等目的,应使用昆虫激素类药物调节蚕生长发育时,应参见附录C所示的民虫激素类药物及其使用方法进行。6.2.6桑叶叶面消毒
在养蚕环境已受到微粒子病污染的地区,为防止食下传染,蚕种生产单位可采取桑叶叶面消毒的办法,以提高对微粒子病的防治效果。必要时,丝董育地区在小蚕共育期间,也可进行桑叶叶面消毒。桑叶叶面消毒,使用含氯消毒药剂。1龄~2龄期,使用有效氯含量为0.3%的消毒液,浸消5min左右,用清水漂洗除去残留在桑叶表面的消毒液,再经脱水、晾干后,即可给桑饲蚕;3龄~5龄期,使用有效氯含量为0.3%的消毒液,浸消8min,经清水漂洗、脱水、晾干后备用。7蚕病的综合防治
7.1饲养管理
蚕病防治以药剂消毒杀灭病原为主,实行多种技术措施配合综合防治。在对蚕室蚕具进行严格消毒的前提下,选择饲养体质强健好养、经济性状优良的蚕品种,加强饲养管理,合理喂饲富含营养物质的饲料,增强蚕体自身的抗病能力。做好桑园病虫害防治工作,防止交叉感染。需要应用药物进行预防治疗或使用激素类药物对蚕的生长发育进行调节时,应避免添食大量水剂。7.2病死蚕与养蚕废弃物处理
72、1病死看处理
为减少病原,养蚕全过程中发现的病死蚕应及时淘汰,并经消毒处理,以免蔓延扩散。被病蚕污染的蚕具、蚕网、防干纸等,应消毒清洗后方能使用。7.2.2蚕沙处理
残桑、蚕粪,应经消毒处理或经堆制充分发酵腐熟后,方可作为肥料施用。3
NY/T1026—2006
A.1适用范围
附录A
(资料性附录
蚕用消毒剂消毒效果生物检测方法本方法适用于蚕用消毒剂对各种物体的消毒效果评价。A.2理化指标
将消毒剂置20℃主2℃温度(或推荐使用温度)下,测定在使用浓度下杀灭指示微生物达到消毒或灭菌所需的最短时间(min)。
A.3指示微生物
A.3.1细菌
A.3.1.1细菌繁殖体:黑胸败血病菌(Bacillussp.)、黏质沙雷氏菌(SerratiamarcescensBizio)。A.3.1.2细菌芽孢:苏芸金芽孢杆菌猝倒亚种(Bacillusthuringiensis subsp,sotoIshiwata)芽孢。A.3.2真菌
A.3.2.1球孢白僵菌[Beauveriabassiana(Bals.)Vuill.A.3.2.2菜氏野村菌[Nomuraearilevi(Farlow)Samson]。A.3.2.3黄曲霉(AspergillusflauusLink)。A.3.3病毒
A.3.3.1家蚕核型多角体病毒(Bambyrc moriNuclearPolyhedrosisVirus,BmNPV)多角体(polyhedron)。A.3.3.2家蚕质型多角体病毒(BombyxmoriCytoplasmicPolyhedrosisVirus,BmCPV)多角体。A.3.4原生动物
A.3.4.1家蚕微粒子虫(NosemabombyeisNaegeli)孢子。A.4检测方法
A.4.1中和剂中和效果试验
A.4.1.1中和剂的选择
为了正确评价消毒剂对微生物的杀灭作用,消毒试验中要求选择适当的中和剂。所选中和剂不仅要能及时中止消毒剂杀灭微生物的作用,且中和剂本身及其与消毒剂的反应产物(下称中和产物)应对微生物无抑制或杀灭作用,并对培养基无不良影响。要选用注明生产厂家、批号的中和剂。A.4.1.2培养基与试剂
A.4.1.2.1普通营养琼脂培养基
成分!
蛋白陈
牛肉膏
氰化钠
蒸馏水
1000ml
NY/T1026—2006
制法:除琼脂外,其他成分溶解于蒸馏水中,调pH至7.2~7.4,加入琼脂后加热溶解,过滤分装,经121C压力蒸汽灭菌30min,备用。A.4.1.2.20.03mol/L磷酸盐缓冲液(pH7.2~7.4,下称PBS)成分:
磷酸氢二钠
磷酸二氢钾
蒸馏水
1000ml
制法:将磷酸氢二钠和磷酸二氢钾溶解于蒸馏水中,pH7.2~7.4,分装,经121℃压力蒸汽灭菌30min,备用。
A.4.1.3器材
A.4.1.3.1锥形烧瓶。
A.4.1.3.2
平皿:直径9cm
量筒。
A.4.1.3.3
A.4.1.3.4
A.4.1.3.5
精密pH试纸。
无菌试管。
5无菌刻度吸管:1.0ml,5.0ml,10.0ml。A.4.1.3.6
A.4.1.3.7
恒温培养箱。
A.4.1.3.8
冰箱。
A.4.1.3.9
菌落计数器。
A.4.1.3.10
酒精灯。
A.4.1.4操作方法
A.4.1.4.1用PBS将指示菌制成5x10°cfu/ml~5x10%cfu/ml悬液。A.4.1.4.2将消毒剂用灭菌蒸馏水配制成3种不同浓度,在不加中和剂的情况下,测知该消毒剂10min抑杀指示菌99.9%以上的最低有效浓度。A.4.1.4.3取消毒剂10min抑杀指示菌的最低有效浓度与待选择中和剂进行试验,选出中和剂种类并依据等当量中和原则,调整中和剂浓度,选出试验浓度的消毒剂使用中和剂的浓度。A.4.1.4.4中和剂选择试验时,先将消毒剂1.0ml与中和剂溶液9.0ml混合,制成中和产物溶液,再按表A1分组进行。
中和剂选择试验
取0.5ml混勾液加人:
0.5ml菌液加人:
消毒剂4.5ml
消毒剂4.5ml
中和产物4.5m
中和剂4.5ml
(加人总量为5ml)
中和剂4.5ml
作用10min后,取原液或
稀释液0.5ml接种平板
(2个/样本)
原液,x10
原液,×10
X100,X1000
x100,×1000
X100,X1000
NY/T1026—2006
然后,倾注平板置37℃培养48h,计数菌落数,按稀释倍数计算出回收菌数(cfu/ml)。A.4.1.5中和试验结果报告方法
按表A2进行。
中和剂
1%卵磷脂
1%卵磷脂+0.1%聚山梨醇-80(吐温80)
1%聚山醇-80(吐温-80)
0.5%硫代硫酸钠
中和试验结果举例
各组回收菌落数,cfu/ml
4.67×1064.83×1004.11×106
794 5.81×106 5.89x106 5.78x1061943.31×10%5.31x105.21×1051323.20×1065.03x105.8×10
第3.4.5组间误差率
3.4.5组误差率按公式(A1)计算
误差率(%)=(三组均数-3组菌数发|+|三组均数-4组菌数|+|三组均数-5组菌数\\)=3×100(A1)三组均数
A.4.1.6判定标准
A.4.1.6.1第3、4、5组菌数相似,其误差率≤10%。A.4.1.6.2第6组无菌生长。
A.4.1.6.3第2组菌数明显少于第3、4.5组。A,4.1.6.4第1组不长菌或明显少于第2组。符合上述标准的中和剂表明可消除消毒剂对指示菌的作用,中和剂及其与消毒剂的中和产物对指示菌无毒害,判定为该消毒剂的中和剂。A.4.2消毒剂定量消毒试验
定量消毒试验是测定受消毒因子作用后,样本残存微生物数量的试验方法。以杀灭率或灭活率表示结果,用于对消毒剂杀灭效果的评价。A.4.2.1培养基
普通营养琼脂培养基,按A.4.1.2.1制备。A.4.2.2试剂
A.4.2.2.1稀释液:含1%蛋白陈的0.03mol/LPBS(pH7.2~7.4)。A.4.2.2.2灭菌蒸馏水。
A.4.2.2.3中和剂
按A.4.1进行选择。
A.4.2.2.40.03mol/LPBS(pH7.2~7.4)。A.4.2.2.5洗脱液:含中和剂、1%蛋白陈、0.1%聚山梨醇-80的PBSA.4.2.3器材
A.4.2.3.1灭菌刻度吸管:1.0ml,5.0ml,10.0ml。A.4.2.3.2无菌试管。
A.4.2.3.3灭菌三角烧瓶。
灭菌平皿(直径9cm)。
A.4.2.3.4
A.4.2.3.5
恒温水浴箱。
A.4.2.3.6恒温培养箱。
A.4.2.3.7酒精灯。
A.4.2.3.8菌落计数器。
A.4.2.3.9微量进样器。
NY/T1026-2006
A.4.2.3.10载体:根据需要及试验目的选用经脱脂处理0.5cm×1.0cm大小的布片、纸片、玻片、橡胶片、塑料片、不锈钢片或铝片。A.4.2.4试验方法
A.4.2.4.1定量悬浮试验
采用定量悬浮试验评价消毒剂杀菌效果及其影响因素。将一定量的细菌悬液加人消毒剂溶液中,作用一定时间,去除残留的消毒剂后,采取消毒液一细菌混合物样本,接种于营养琼脂固体培养基上,经培养后检查其存活菌数,与未经消毒剂作用的对照菌数相比较,计算出杀菌效果。消毒对象为家蚕病毒(BmNPV和BmCPV)多角体和微粒子虫(Nasemabom-bucis)孢子时,将消毒液一多角体或微粒子虫孢子混合物样本,涂抹于定量桑叶后,经口接种于家蚕二龄起蚕,饲养一定时间后,记录统计发病死亡率,计算半数感染剂量IDs0,与未经消毒剂作用的对照组相比较,计算出消毒效果。试验时,根据消毒剂的特性和消毒对象,确定供试指示微生物的种类。A.4.2.4.1.1配制试验菌液:用无菌蒸馏水或磷酸盐缓冲液,将菌液稀释至5×105cfu/ml~5×10gcfu/ml。如消毒对象是病毒多角体或微粒子虫孢子,则将其稀释至10°个/mlA.4.2.4.1.2配制消毒液溶液:将消毒剂用蒸馅水稀释成3个不同浓度,每个浓度4.5ml,放20土2℃水浴中。
A.4.2.4.1.3待试管内液体温度与水浴温度平衡后,吸取试验菌液(或病毒多角体、微粒子虫孢子悬液)0.5ml,加入消毒剂溶液内,混匀,立即计时,此时菌一药混合液含菌量为5×10cfu/ml~5×105cfu/ml,或10°个/ml多角体(或微粒子虫孢子)。A.4.2.4.1.4分别于4个不同间隔时间,各取0.5ml菌一药混合波移入4.5ml中和剂中混勾。A.4.2.4.1.5中和10min,作适当释后进行活菌计数:接种平板,细菌放37C温箱内培养24h~48h后计数菌落;白僵菌25℃、曲霉菌30℃,培养48h后观察初步结果,继续观察一周止。A.4.2.4.1.6如消毒对象是多角体或微粒子虫孢子,则将中和后的混合液逐级稀释后涂抹于桑叶,定量喂于二龄起蚕,每区设3个重复。根据各种蚕病潜伏期的长短,饲养一定时间(核形多角体病3d5d,微粒子病7d~10d,质形多角体病7d~12d),饲养过程中随时注意病蚕的发病情况,做好病蚕的隔离消毒工作,防止交叉感染。根据各种病的发病症状并结合显微镜进行逐条检查,记录阳性率,按式(A2)计算对照组和试验组的ID50gIDs的对数=L-d(S-0.5)
式中:
L为最低稀释倍数的对数;
d为稀释度间差的对数;
S为各稀释列的阳性率(发病蚕数/接种蚕数)之和。+*....(A2)
A.4.2.4.1.7阳性对照,以洗脱液代替消毒液,同时按A.4.2.4.1.2~A.4.2.4.1.6进行。A.4.2.4.1.8按不同稀释度推算出每个样本存活菌数(cfu/ml),按式(A3)计算杀灭率:如消毒对象是病毒多角体或微粒子虫孢子时,按式(A4)计算灭活率。杀灭率(%)=对照组存适菌数在试验组存活菌数×100对照组存活菌数
以上计算必须将对照组生长菌数和消毒组生长菌数换算成相同稀释度后,然后代人公式。灭活:%-对照组照组试验组1..
对照组IDs0
NY/T1026—2006
A.4.2.4.1.9试验重复5次。
A.4.2.4.2定量载体试验
将一定量的病原微生物污染在载体上,然后将染菌载体暴露于消毒剂,作用一定时间后,将载体放人中和液内洗菌,稀释,进行活菌计数或对蚕体感染力测试,并与未经消毒的对照载体比较,计算出杀灭率。
A.4.2.4.2.1将灭菌载体平放于平皿内,每个载体滴注定量菌液(载体回收菌量达5×10cfu/片~5x10°cfu/片),涂匀,放37℃培养箱待干。A.4.2.4.2.2用灭菌蒸馏水将消毒剂稀释成3个不同浓度,各吸取5ml分别加入3个试管内,置于20℃水浴中,或恒温箱内。
A.4.2.4.2.3待试管内液体温度与水浴温度平衡后,加入染菌载体,作用至规定时间,将染菌载体移人含中和剂的5ml洗脱液试管内,中和10min,振荡80次,适当稀释,接种两个平板,放37℃C培养24h~48h,进行活菌计数。球孢白僵菌25℃、曲霉菌30℃,培养48h后观察初步结果,继续观察一周止。A.4.2.4.2.4如消毒对象是多角体或微粒子虫孢子,则按A.4.2.4.1.6进行。A.4.2.4.2.5阳性对照,以洗脱液代替消毒液按A.4.2.4.2.2~A.4.2.4.2.4进行。A.4.2.4.3表面消毒试验
将一定量的特定微生物污染在载体或物体表面,然后将染菌(包括细菌繁殖体和芽孢、微粒子虫孢子、病毒多角体,真菌分生孢子等)载体暴露于消毒因子中,作用一定时间后,用含有中和剂的稀释液回收残留于载体或物体表面上的微生物,与对照组菌数比较,计算杀灭率。如消毒对象为家蚕病原多角体或微粒子虫孢子,则将回收的微生物经口接种于蚕体,调查感染发病率,与对照组比较,计算灭活率。A.4.2.4.3.1染菌样片的制备:试验前将布片、铝片、玻璃片、纸片、竹片等有代表性的材料制成0.5cm×1.0cm或1cm×1cm、1.5cm×1.5cm的样片,用洗衣粉煮沸后用自来水冲洗、晾干、经高压灭菌备用。染菌方法有滴染、浸染和喷染三种。染菌量一般控制在每片5×105个~5×10°个。A.4.2.4.3.1.1滴染法将灭菌后的样片平放于无菌平皿内,每个样片加0.01ml~0.02ml菌液,涂匀。菌片于37℃温箱烘干,备用。繁殖体菌片现用现制备,芽孢菌片在4℃下,有效期不超过6个月。病毒多角体,微粒子虫孢子和真菌分生孢子菌片提前1d~3d制备,自然条件下阴干。A.4.2.4.3.1.2浸染法将灭菌样片平放于灭菌平血内,加人菌液,以样片全部浸湿为度。30min后,用无菌镊子将菌片移至另一垫有灭菌滤纸的平血内,于37℃温箱烘干、备用。A.4.2.4.3.1.3喷雾染菌法用气溶胶喷雾器将预先制备好的菌液在密闭的染菌柜内喷雾数分钟。喷雾完毕后静止1min,待大粒子沉降后,将样片由柜下方的抽屈送人柜内,使细菌微粒均勾沉降在样片上(一般为15min)。
A.4.2.4.3.2将试验菌片放在合适的部位,当测定烟雾熏蒸或喷雾熏蒸等消毒试验时,将菌片放于室内有代表性的地点,例如地面、桌面、窗面、墙壁等。经消毒预定时间后,将菌片放人装有5ml无菌蒸馅水或0.03M磷酸盐缓冲液(如消毒因子为消毒剂,则可根据消毒剂种类加入相应的中和剂)的试管中。将试管用力振荡80次,以洗下菌片上的残留微生物,用吸管吸取原液或适当倍数的稀释液接种平板,作活菌计数。
A.4.2.4.3.3如消毒对象是多角体或微粒子虫孢子,则按A.4.2.4.1.6进行。A.4.2.4.3.4阳性对照,不作消毒处理,按A.4.2.4.3.1~A.4.2.4.3.3进行。A.4.2.4.3.5按式(A5)计算杀灭率,按式(A4)计算灭活率。杀灭率(%)=对照组菌片整菌鳌片遭囊细菌片回收菌数×100对照组菌片回收菌数
O ........ (A5)
如消毒对象为家蚕病原多角体或微粒子虫孢子,消毒效果则用灭活率来表示。灭活率的计算方法8
同“定量悬浮试验”。
A.4.3有机物保护试验
NY/T10262006
通过有机物保护试验,测定消毒剂对有机物保护条件下的微生物的杀灭作用,以杀灭率表示,其结果与该消毒剂定量消毒试验相比较,用于评价有机物对消毒剂的杀菌能力的影响。A.4.3.1培养基与试剂
A.4.3.1.1普通营养琼脂培养基:按A.4.1.2.1制备。A.4.3.1.2试剂
A.4.3.2.2.1稀释液:同A.4.2.2.1。A.4.3.2.2.2灭菌蒸馏水。
A.4.3.2.2.3中和剂:按A.4.1进行选择。A.4.3.2.2.40.03mol/LPBSpH7.2~7.4)。A.4.3.2.2.5洗脱液:含1%蛋白陈、0.1%聚山梨醇-80的生理盐水。A.4.3.2.2.6小牛血清加人菌悬液中,使其最终浓度为10%。A.4.3.2器材
同A.4.2.3。
A.4.3.3试验方法
A.4.3.3.1实验前预先将菌液进行活菌计数,用稀释液稀释,加入小牛血清,使其最终浓度为10%,含菌数为5×105cfu/ml~5×10°cfu/ml,以此作为试验菌悬液。A.4.3.3.2以下步骤同A.4.2.4.1.2~A.4.2.4.1.9。A.4.3.4结果判定
A.4.3.4.15次试验的杀灭率均大于99.9%所需最低浓度和最短时间,判为该消毒剂在有机物存在下,可以达到消毒的有效浓度和时间。A.4.3.4.2此有效浓度和时间与定量消毒试验达到消毒的有效浓度和时间相同或相近,判为有机物对消毒剂杀菌作用无明显影响。达到消毒最低有效浓度增加1倍以上或最短作用时间延长1倍以上者可视为有明显影响。
A.5消毒效果的评价
A.5.1对细菌和真菌的杀灭率≥99.9%,对病毒多角体和家蚕微粒子虫孢子的灭活率≥99.0%,可判为消毒合格。
A.5.2在实际应用中消毒效果的评价以有机物保护试验的最低浓度和最短时间为该消毒剂达到实用消毒所需的浓度和时间。
A.5.3注明采用何种试验方法。
NY/T1026—2006
B.1适用范围
附录B
(资料性附录)
蚕用抗微生物药物生物检测方法本方法适用于蚕用抗微生物药物对家蚕细菌病防治效果评价。B.2理化指标
在25℃土2℃条件下,测定各种抗微生物药物达到有效治疗家蚕细菌病的最低剂量和时间。B.3
3指示微生物
B.3.1细菌
B.3.1.1细菌繁殖体:黑胸败血病菌(Bacillussp.)、黏质沙雷氏菌(SerratiamarcescensBizio)、青头败血病菌(Aeromonassp)肠球菌(Enterococcusfaecalis或Enterocaccusfaecium)。B.3.1.2细菌芽孢:苏芸金芽孢杆菌猝倒亚种(Bacillusthuringiensis subsp.sottoIshiwata)。B.4检测方法
B.4.1抗微生物药物体外抑菌(杀菌)试验抗微生物药物体外抑菌(杀菌)试验是测定受抗微生物药物作用后的样本有无微生物生长的试验方法。该试验适用于对抗微生物药物抑菌(杀菌)效果的初步评价。B.4.1.1培养基
B.4.1.1.1普通营养琼脂培养基:按A.4.1.2.1制备。B.4.1.1.2普通肉汤培养基
B.4.1.2.2.1成分:
蛋白藤
氟化钠
肉浸液
1000ml
B.4.1.2.2.2制法:取蛋白陈、氯化钠加肉浸液内。微温溶解,调pH至弱碱性,煮沸、滤清,调节pH使灭菌后为7.2-7.4压力燕汽灭菌备用。B.4.1.2试剂
B.4.1.2.1稀释液:含1%蛋白陈的0.03mol/LPBS(pH7.2~7.4)。B.4.1.2.2灭菌蒸馏水
B.4.1.3器材
B.4.1.3.1灭菌刻度吸管:1.0ml,5.0ml,10.0ml。B.4.1.3.2
灭菌试管
B.4.1.3.3
3灭菌三角烧瓶。
B.4.1.3.4酒精灯。
B.4.1.3.5恒温水浴箱。
B.4.1.3.6恒温培养箱。
B.4.1.4试验方法
B.4.1.4.1最小抑首浓度(MIC)的测定NY/T10262006
B.4.1.4.1.1将逐步降低浓度的抗微生物药物溶液(通常采用1:2稀释)和等量的双倍浓度的营养肉汤相混合,然后用0.1ml试验菌的培养物接种各试管,使其含菌量为10°cfu/ml左右。B.4.1.4.1.2接种后的试管,在37℃下培养24h,观察有无细菌生长B.4.1.4.2最小杀菌浓度(MBC)的测定B.4.1.4.2.1在MIC试验的基础上进行。将MIC试验中无细菌生长的各管培养液0.1ml转接于不含抗微生物药物的普通营养琼脂培养基平血表面。B.4.1.4.2.2接种后的平血在37℃下培养24h48h,观察有无细菌生长,B.4.1.4.3试验重复3次。
B.4.1.5结果判定
B.4.1.5.1肉汤培养时,以抑制微生物生长的最低药物浓度为MIC值。B.4.1.5.2平血皿培养时以细菌减少99.9%的最低药物浓度为MBC值B.4.2抗微生物药物临床试验
通过抗微生物药物临床试验,测定受抗微生物药物作用后的蚕体有无感染发病。该试验适用于对抗微生物药物实际使用效果的评价。B.4.2.1培养基
B.4.2.1.1普通营养琼脂培养基:按A.4.1.2.1制备。B.4.2.1.2普通肉汤培养基:按B.4.1.1.2制备。B.4.2.2试剂:同B.4.1.2。
B.4.2.3器材
B.4.2.3.1灭菌刻度吸管:1.0ml,5.0ml,10.0mlB.4.2.3.2灭菌试管。
B.4.2.3.3灭菌三角烧瓶。
B.4.2.3.4酒精灯。
B.4.2.3.5接种针。
B.4.2.3.6恒温培养箱。
B.4.2.4试验方法
B.4.2.4.1用稀释液将肉汤培养或平皿培养的菌液稀释计数,使其含菌量为10°cfu/ml左右。B.4.2.4.2药物试验组一般设高、中(推荐剂量)低三个剂量组B.4.2.4.3空白对照组即不感染不给药组。B.4.2.4.4阳性对照组即感染不给药组。B.4.2.4.5药物对照组选择与试验药物具有可比性的同类或同效药物,按常规剂量给药。B.4.2.4.6用经酒精灯火焰灭菌的接种针蘸取少量菌液给四龄或五龄起蚕进行穿刺接种,或将菌液均匀涂抹于定量桑叶叶面给蚕进行经口接种,每个处理40头一50头蚕,重复3区。B.4.2.4.7接种后进行给药处理,按推荐的临床给药途径给药11
NY/T1026—2006
B.4.2.4.8按常规的饲养方法进行饲养观察,调查各处理的发病死亡情况,记录发病死亡率。B.4.2.4.9按式(B1)计算有效率。有效率%)阻性对照组发瘤率药物基验组发病死亡率10(B1)阳性对照组发病死亡率
0试验重复3次,统计平均有效率。B.4.2.4.10
B.4.2.5结果判定
B.4.2.5.1阳性对照组发病死亡率≥95.0%。2以平均有效率≥95.0%判定该抗微生物药物治疗有效。B.4.2.5.2
B.5治疗效果的评价
B.5.1计算有效率,平均有效率≥95.0%判定为该抗微生物药物治疗有效12
小提示:此标准内容仅展示完整标准里的部分截取内容,若需要完整标准请到上方自行免费下载完整标准文档。
标准图片预览:




- 其它标准
- 热门标准
- 农业行业标准(NY)
- NY/T1153.4-2013 农药登记用白蚁防治剂药效试验方法及评价 第4部分农药木材处理预防白蚁
- NY/T5295-2004 无公害食品 产地环境评价准则
- NY/T797-2004 硅肥
- NY/T2501-2013 植物新品种特异性、一致性和稳定性测试指南 丝瓜
- NY/T482-2002 敬亭绿雪茶
- NY/T1121.4-2006 土壤检测 第4部分:土壤容重的测定
- NY/T2024-2011 农作物优异种质资源评价规范 柿
- NY/T5295-2004 无公害食品产地环境评价准则
- NY/T800-2004 生鲜牛乳中体细胞的测定方法
- NY/T5094-2002 无公害食品 蕹菜生产技术规程
- NY/T742-2003 铧式犁作业质量
- NY/T1464.28-2010 农药田间药效试验准则 第28部分:杀虫剂防治阔叶树天牛
- NY/T2669-2014 热带作物品种审定规范 木薯
- NY/T798-2015 复合微生物肥料
- NY/T2516-2013 植物新品种特异性、一致性和稳定性测试指南 椰子
- 行业新闻
请牢记:“bzxz.net”即是“标准下载”四个汉字汉语拼音首字母与国际顶级域名“.net”的组合。 ©2025 标准下载网 www.bzxz.net 本站邮件:bzxznet@163.com
网站备案号:湘ICP备2025141790号-2
网站备案号:湘ICP备2025141790号-2