- 您的位置:
- 标准下载网 >>
- 标准分类 >>
- 医药行业标准(YY) >>
- YY 0290.4-2008 医用光学人工晶状体 第4部分:标签和资料
标准号:
YY 0290.4-2008
标准名称:
医用光学人工晶状体 第4部分:标签和资料
标准类别:
医药行业标准(YY)
标准状态:
现行-
发布日期:
2008-10-17 出版语种:
简体中文下载格式:
.rar.pdf下载大小:
148.80 KB
替代情况:
替代YY 0290.4-1997采标情况:
ISO11979-4:2000 IDT
点击下载
标准简介:
标准下载解压密码:www.bzxz.net
YY 0290《眼科光学 人工晶状体》分为9个部分,本部分为YY 0290的第4部分。本部分代替YY 0290.4-1997《人工晶体 第4部分:标签和资料》。YY0290的本部分规定了标签和包装上或包装内所提供资料内容的要求。本部分与YY 0290.4-1997相比主要变化如下:———规范性引用文件YY0290.1采用2008版;———适用范围进行了适当调整;———YYY 0290.4-1997中第3章给出的术语在本版本的附录A(资料性附录)中列出;———YY 0290.4-1997中表1内容在本标准分拆为表1、表2,并增加了相关项目;———对第5章项目进行了部分调整;———原附录A内容在本版本中调整为标准第6章。 YY 0290.4-2008 医用光学人工晶状体 第4部分:标签和资料 YY0290.4-2008
部分标准内容:
ICS 11.040
中华人民共和国医药行业标准
YY 0290.4—2008/IS0 11979-4:2000代替YY0290.1-1997
眼科光学
人工晶状体
第4部分:标签和资料
Ophthalmic implants-Intraocular lenses-Part 4 Labeling and information(1SO 11979 4:2000,IDT)
2008-10-17发布
国家食品药品监督管理局
2010-06-01实施
YY0290眼科光学人晶状体》分为9个部分:-第 1 部分:术语;
-第2部分:光学性能及测试方法:—一第3部分+机械性能及测试方法;第4部分:标签和资料:
第5部分:件物柜奔性;
第6部分:有效期和运输稳定性;第8部分:基本要求;
第9部分:多焦人工晶忧休:
一第10部分有晶体眼人工品状侠:本部分为YY0290的第1部分,
FKAONiKAca
YY 0290.4—2008/1S0 11979-4:2000全部分等同采用[SO11979-4:2000%服科植人物人上品状体第4部分:标签利资料本部分代替YY0299.4—1997《人工品体第4部分:标签和资料》。本部分与YY0290.4—1997相比主要变化如下:规范性引用文件YY0290.1采用2008版;适月范围进行了适当调整;
YY02.4—1997中第3章给出的术语在本版本的附录A(资料性附录)中列山;—YY0290,4一1997中表1内容在本标准分拆为表1.表2,并增加了相关项日;对第5章项目进行了部分调整:
-原附录A内容在本版本中调整为标准第6章,本部分的附录A为资料性附录,
本标准由全国光学利光学仪器标推化技术委员会医用光学和仪器分技术委员会(SAC/TC103/SC1)提出并归口
本部分起草单位:国家食品药品监督管理局杭州医疗器械质量监督检验中心。本部分主晏起草人:何涛、郑建、贾晓航,文燕、马莉。1
1范围
YY 0290.4—2008/1S0 11979-4,2000眼科光学
人工晶状体
第4部分·标签和资料
YY0290的本部分规定了人工晶状体(IO1.)标签和包装上或包装内所提供资料内容的要求。2
规范性引用文件
下列文件中的条通过YY0290的本部分的引用而成为本部分的条款,凡是注口期的引用文件,其随后的修改单(不包括勘误的内容)或修订版均不适用于本部分,然而,鼓励根据本部分达成协议的各方研究是否可使用这些文件的联新版本。凡是不注日期的引用文件,其最新版本适用于本部分。YY0290.1一2008眼科光学人T.品状体第1部分,术语3术语和定义
YY029C.!确立的术语利定义适月于YY0290的本部分。注;YY 0290. 1中与术部分关的某些术语和定义在附录 A 中作为资料性附录给出。4标签
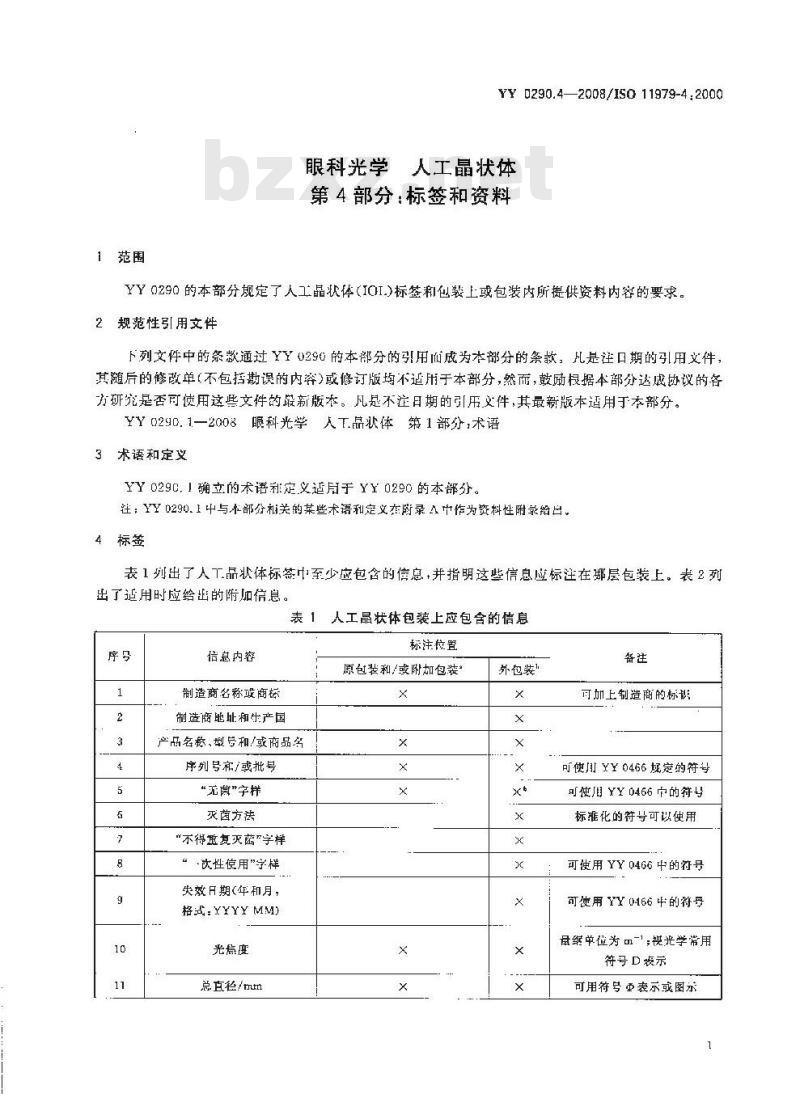
表1列出了人工品状体标签巾至少应包含的信息,并指明这些信息应标注在层包装上。表2列出了适用时应给出的附加信息。表人工晶状体包装上应包含的信息序号
信息内容
制造商名称成商标
制造商地址和生产国
产品名格、型号和/或商品名
序列号和/或批号
“无菌”字样
灭茵方法
\不得重复灭菌\字样
“·次性使用”字样
失效月期(年和月,
格式:YYYY MM)
总直径/tntm
标注位置
原包装和/或附如包装”
外包装”
可加上制造商的标认
可使YY0466规定的符号
可使目YY0466的符号
标准化的符号可认使用
可使用 YY 0466 中的符号
可使用 YY 0166中的符号
母缩单位为-1,视光学常用
符号D表示
可用符号重表示或图示
YY 0290.42008/IS0 11979-4:2000序号
倍息内容
主体直径(若为非团形,
标注最大.最小尺度>/mm
人工晶状体结构外形图
预期植人位置的说明
帮助手术老计样植人光
焦度的信息
a关于原包装和附加包装自
使用和正确处理。
b若在外包装上已经有
人工晶状体”。
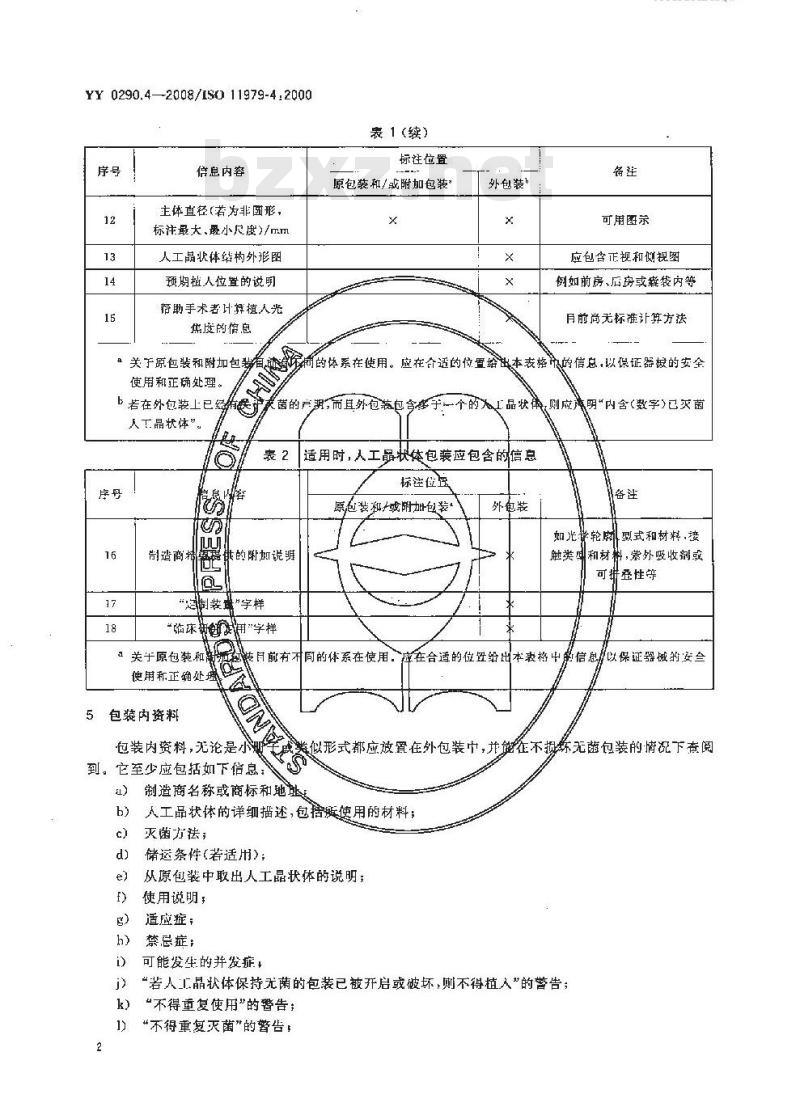
表1(续)
标性位置
原包装和/或附加包装”免费标准下载网bzxz
外包装”
-iiKAONiKAca-
可用图示
应包含正视和侧视图
例如前房、后穷或释袋内等
月前尚无标准让算方法
除周的体系在使用。应在合适的位置给出本表格决的信总以保证器核的安全家菌的产期,而且外包装包含存手一个的人工品状微则应角明“内含(数字)已灭菌表2
适用时,人工品状体包装应包含的信总标注位馆
原包装和+或附包装
律的附加说期
制造商
“烂制装量\字样
“弦床神用\学样
关于原包装和离
便用和正确处理
包装内资料
外包装
经备注
如光骨轮闭型式和材料,接
触类和材,紫外吸收剂或
可拼叠性等
目前有才同的体系在使用,痒在合适的位置给出本表格中前信息/以保证器械的安全包装内资料,无论是小
到。它至少应包括如下信息
似形式都应放罩在外包装巾,并能在不练无萌包装的情说下套阅制造商名称或商标和地盛
人工品状体的详细描述,包括读用的材料;灭菌方法;
储运条件(若适用):
从原包装中取出人工晶状体的说明;使用说明,
适应症;
禁总症:
可能发生的并发症,
“若人工品状体保持无菌的包装已被开启或破坏,则不得植人”的警告;“不得重复使用”的替告;
“不得重复灭菌”的替告!
Ⅱ)其他适用的警告:
6自粘标签
如果制造商提供广自粘标签,至少应包含如下内容:制造商名称或商标;
产品名称,型号和/或商品名:
序列号和/或批号。可使用YY0466中给出的符号;光焦度:
YY0290.4—2008/1SO11979-4.2000总直径,可用符号更或图系表示:主体卓径(芳为非圆形,最小和最动度,可用图示表示。SE
YY 0290.4--2008/[S0 11979-4:2000附录A
(资料性附录)
选用的术语和定义
HiiKAONiKAca-
为方便使用YY0290的本部分,此处将用到的术语和定义再次列出。若有差只,YY0290.1中定义的术语优先于本文给出的术语和定义。A.1
附加包装additionalwrapping
除原包装外,为保持无菌性能的附加包装物A.2
定制装置 cuslom-made device
根据某位具有正式资格的医疗从业者在其责任范用内给出处方要求,指定设计特性而生产的任何独特设让的装置,该装置专门用予某位特殊虑者。往;为满见医疗从业者特殊婴求而大量生产的裳置不认为是定制装骨。A.3
临床研究使用装置device intended for clinical investigation某位具有正式资格的医疗从业者进行临床研究时所使用的任何装置。A.4
manufacturer
制造商
相有自标识的产品,在上市前对该产品设计,生产,包装利标志负有责任的自然人或法人,不管该行为足本人进行或第三方进行。注:制造商所负的贵任同样适用于那些装配.包装,处理、完全改装和/减将其期有的标识站于产品标签工投放市的自然人或法人。
原包装
primary packaging
用物理方法点接保护晶状体维持其无菌的容器。A.6
自粘标签 self-adhesive lahel放于予外包装内用于医疗记录使用的标签。A.7
外包装storage container
在贮存、销售期间起保护作用的包装。参考文献
YY0290.4—2008/1S0 11979-4:2000[1」YY0466一2003医疗器械用于医疗器械标签、标记和提供信息的符号(ISO15233:2000.IDT)
EN980:1986为医疗器械提供的术语、符号和信息在医疗器标签中适用的图示符号[2-
6为医疗器械提供的术语、符号和信息医疗器械制造商提供的信息EN 1041:1996
YY 0290.4-2008
HTKAONIKAca-
中华人民共和国医药
行业标滩
眼科光学人工晶状体
第4部分:标签和资料
YY 0290. 4—2008/ISO 11979-4:2000*
中国标雅出版社出版发行
北京复兴门外三里河北街16号
邮政编码:100045
网址 spc. nct. cn
电话:68523946
68517548
中国标准出版社案皇岛印刷厂印刷各地新华书店经销
开本 880× 1230 1/16
印张 0.75字数10T字
2009 年1月第一版 2009年1月第 次印刷x
书号:155066·2-19327
7定价14.00元
如有印装差错
由本社发行中心调换
版权专有
侵权必究
举报电话:(01068533533
小提示:此标准内容仅展示完整标准里的部分截取内容,若需要完整标准请到上方自行免费下载完整标准文档。
中华人民共和国医药行业标准
YY 0290.4—2008/IS0 11979-4:2000代替YY0290.1-1997
眼科光学
人工晶状体
第4部分:标签和资料
Ophthalmic implants-Intraocular lenses-Part 4 Labeling and information(1SO 11979 4:2000,IDT)
2008-10-17发布
国家食品药品监督管理局
2010-06-01实施
YY0290眼科光学人晶状体》分为9个部分:-第 1 部分:术语;
-第2部分:光学性能及测试方法:—一第3部分+机械性能及测试方法;第4部分:标签和资料:
第5部分:件物柜奔性;
第6部分:有效期和运输稳定性;第8部分:基本要求;
第9部分:多焦人工晶忧休:
一第10部分有晶体眼人工品状侠:本部分为YY0290的第1部分,
FKAONiKAca
YY 0290.4—2008/1S0 11979-4:2000全部分等同采用[SO11979-4:2000%服科植人物人上品状体第4部分:标签利资料本部分代替YY0299.4—1997《人工品体第4部分:标签和资料》。本部分与YY0290.4—1997相比主要变化如下:规范性引用文件YY0290.1采用2008版;适月范围进行了适当调整;
YY02.4—1997中第3章给出的术语在本版本的附录A(资料性附录)中列山;—YY0290,4一1997中表1内容在本标准分拆为表1.表2,并增加了相关项日;对第5章项目进行了部分调整:
-原附录A内容在本版本中调整为标准第6章,本部分的附录A为资料性附录,
本标准由全国光学利光学仪器标推化技术委员会医用光学和仪器分技术委员会(SAC/TC103/SC1)提出并归口
本部分起草单位:国家食品药品监督管理局杭州医疗器械质量监督检验中心。本部分主晏起草人:何涛、郑建、贾晓航,文燕、马莉。1
1范围
YY 0290.4—2008/1S0 11979-4,2000眼科光学
人工晶状体
第4部分·标签和资料
YY0290的本部分规定了人工晶状体(IO1.)标签和包装上或包装内所提供资料内容的要求。2
规范性引用文件
下列文件中的条通过YY0290的本部分的引用而成为本部分的条款,凡是注口期的引用文件,其随后的修改单(不包括勘误的内容)或修订版均不适用于本部分,然而,鼓励根据本部分达成协议的各方研究是否可使用这些文件的联新版本。凡是不注日期的引用文件,其最新版本适用于本部分。YY0290.1一2008眼科光学人T.品状体第1部分,术语3术语和定义
YY029C.!确立的术语利定义适月于YY0290的本部分。注;YY 0290. 1中与术部分关的某些术语和定义在附录 A 中作为资料性附录给出。4标签
表1列出了人工品状体标签巾至少应包含的信息,并指明这些信息应标注在层包装上。表2列出了适用时应给出的附加信息。表人工晶状体包装上应包含的信息序号
信息内容
制造商名称成商标
制造商地址和生产国
产品名格、型号和/或商品名
序列号和/或批号
“无菌”字样
灭茵方法
\不得重复灭菌\字样
“·次性使用”字样
失效月期(年和月,
格式:YYYY MM)
总直径/tntm
标注位置
原包装和/或附如包装”
外包装”
可加上制造商的标认
可使YY0466规定的符号
可使目YY0466的符号
标准化的符号可认使用
可使用 YY 0466 中的符号
可使用 YY 0166中的符号
母缩单位为-1,视光学常用
符号D表示
可用符号重表示或图示
YY 0290.42008/IS0 11979-4:2000序号
倍息内容
主体直径(若为非团形,
标注最大.最小尺度>/mm
人工晶状体结构外形图
预期植人位置的说明
帮助手术老计样植人光
焦度的信息
a关于原包装和附加包装自
使用和正确处理。
b若在外包装上已经有
人工晶状体”。
表1(续)
标性位置
原包装和/或附加包装”免费标准下载网bzxz
外包装”
-iiKAONiKAca-
可用图示
应包含正视和侧视图
例如前房、后穷或释袋内等
月前尚无标准让算方法
除周的体系在使用。应在合适的位置给出本表格决的信总以保证器核的安全家菌的产期,而且外包装包含存手一个的人工品状微则应角明“内含(数字)已灭菌表2
适用时,人工品状体包装应包含的信总标注位馆
原包装和+或附包装
律的附加说期
制造商
“烂制装量\字样
“弦床神用\学样
关于原包装和离
便用和正确处理
包装内资料
外包装
经备注
如光骨轮闭型式和材料,接
触类和材,紫外吸收剂或
可拼叠性等
目前有才同的体系在使用,痒在合适的位置给出本表格中前信息/以保证器械的安全包装内资料,无论是小
到。它至少应包括如下信息
似形式都应放罩在外包装巾,并能在不练无萌包装的情说下套阅制造商名称或商标和地盛
人工品状体的详细描述,包括读用的材料;灭菌方法;
储运条件(若适用):
从原包装中取出人工晶状体的说明;使用说明,
适应症;
禁总症:
可能发生的并发症,
“若人工品状体保持无菌的包装已被开启或破坏,则不得植人”的警告;“不得重复使用”的替告;
“不得重复灭菌”的替告!
Ⅱ)其他适用的警告:
6自粘标签
如果制造商提供广自粘标签,至少应包含如下内容:制造商名称或商标;
产品名称,型号和/或商品名:
序列号和/或批号。可使用YY0466中给出的符号;光焦度:
YY0290.4—2008/1SO11979-4.2000总直径,可用符号更或图系表示:主体卓径(芳为非圆形,最小和最动度,可用图示表示。SE
YY 0290.4--2008/[S0 11979-4:2000附录A
(资料性附录)
选用的术语和定义
HiiKAONiKAca-
为方便使用YY0290的本部分,此处将用到的术语和定义再次列出。若有差只,YY0290.1中定义的术语优先于本文给出的术语和定义。A.1
附加包装additionalwrapping
除原包装外,为保持无菌性能的附加包装物A.2
定制装置 cuslom-made device
根据某位具有正式资格的医疗从业者在其责任范用内给出处方要求,指定设计特性而生产的任何独特设让的装置,该装置专门用予某位特殊虑者。往;为满见医疗从业者特殊婴求而大量生产的裳置不认为是定制装骨。A.3
临床研究使用装置device intended for clinical investigation某位具有正式资格的医疗从业者进行临床研究时所使用的任何装置。A.4
manufacturer
制造商
相有自标识的产品,在上市前对该产品设计,生产,包装利标志负有责任的自然人或法人,不管该行为足本人进行或第三方进行。注:制造商所负的贵任同样适用于那些装配.包装,处理、完全改装和/减将其期有的标识站于产品标签工投放市的自然人或法人。
原包装
primary packaging
用物理方法点接保护晶状体维持其无菌的容器。A.6
自粘标签 self-adhesive lahel放于予外包装内用于医疗记录使用的标签。A.7
外包装storage container
在贮存、销售期间起保护作用的包装。参考文献
YY0290.4—2008/1S0 11979-4:2000[1」YY0466一2003医疗器械用于医疗器械标签、标记和提供信息的符号(ISO15233:2000.IDT)
EN980:1986为医疗器械提供的术语、符号和信息在医疗器标签中适用的图示符号[2-
6为医疗器械提供的术语、符号和信息医疗器械制造商提供的信息EN 1041:1996
YY 0290.4-2008
HTKAONIKAca-
中华人民共和国医药
行业标滩
眼科光学人工晶状体
第4部分:标签和资料
YY 0290. 4—2008/ISO 11979-4:2000*
中国标雅出版社出版发行
北京复兴门外三里河北街16号
邮政编码:100045
网址 spc. nct. cn
电话:68523946
68517548
中国标准出版社案皇岛印刷厂印刷各地新华书店经销
开本 880× 1230 1/16
印张 0.75字数10T字
2009 年1月第一版 2009年1月第 次印刷x
书号:155066·2-19327
7定价14.00元
如有印装差错
由本社发行中心调换
版权专有
侵权必究
举报电话:(01068533533
小提示:此标准内容仅展示完整标准里的部分截取内容,若需要完整标准请到上方自行免费下载完整标准文档。
标准图片预览:


- 热门标准
- 医药行业标准(YY)
- YY/T1096-2007 温度生物反馈仪
- YY/T0915-2015 ISO 27020:2010 牙科学正畸用托槽和颊面管
- YY0165-1994 热垫式治疗仪
- YY/T0890-2013 放射治疗中电子射野成像装置性能和试验方法
- YY0053-2008 心血管植入物和人工器官血液透析器、血液透析滤过器、血液滤过器和血液浓缩器
- YY/T0591-2011 骨接合植入物 金属带锁髓内钉
- YY/T1523-2017 二氧化碳测定试剂盒(PEPC酶法)
- YY/T1145-2003 人工心肺机术语
- YY/T0454-2003 无菌塑柄手术刀
- YY/T0859-2011 均匀径向载荷下金属血管支架有限元分析方法指南
- YY/T0740-2009 医用血管造影X射线机专用技术条件
- YY/T0457.2-2003 IEC 61262-2. 1994 医用电气设备光电X射线影像增强器特性 第2部分:转换系数的测定
- YY0053-2008 心血管植入物和人工器官血液透析器、血液透析滤过器、血液滤过器和血液浓缩器
- YY/T1522-2017 连接到医用气体管道系统终端的流量测量装置
- YY/T1529-2017 酶联免疫分析仪
- 行业新闻
请牢记:“bzxz.net”即是“标准下载”四个汉字汉语拼音首字母与国际顶级域名“.net”的组合。 ©2025 标准下载网 www.bzxz.net 本站邮件:bzxznet@163.com
网站备案号:湘ICP备2025141790号-2
网站备案号:湘ICP备2025141790号-2