中小幼4氧化还原基础同步练习公开课教案教学设计课件 氧化和还原
中小幼4氧化还原基础同步练习公开课教案教学设计课件 氧化和还原 中小幼4氧化还原基础同步练习公开课教案教学设计课件 氧化和还原
- 类型:
- 课件
- 大小:
- 10 KB
- 格式:
- doc
- 评分:
- 9.0
基础同步练习
1.分析反应MnO2+4HCl(^)=^=MnC12+2H2O+Ch,用双线桥法和单线桥法标出电子转移的方向和数目
2.已知以下两个氧化还原反应的化学方程式:
①2KC1O3^^2KC1+302
②2Al+Fe2O3=^=Al2O3+2Fe⑴用单线桥法表示反应
②中的电子转移情况⑵反应
①中每生成1个2,转移电子的量是
1.下列属于氧化还原反应的是()A.2NaHCO3=^=Na2CO3+H20+CO2T B.Na2O+H2O=2NaOH C.2Kl+Br2=2KBr+l2D.MgO+2HCl=MgCl2+H
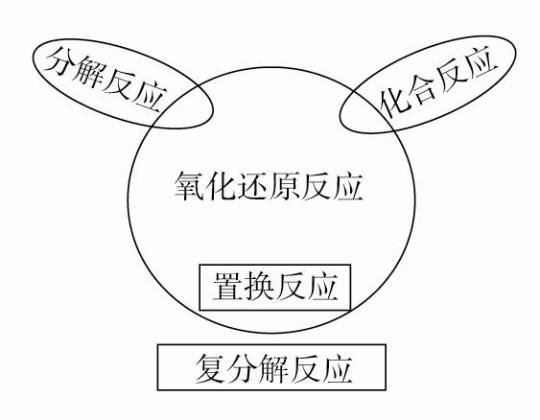
202.下列说法正确的是()A.复分解反应中有的是氧化还原反应,有的不是氧化还原反应B.置换反应有可能是非氧化还原反应C.化合反应一定是氧化还原反应D.分解反应不一定是氧化还原反应
3.氧化还原反应在生产、生活中具有广泛的用途下列生产、生活中的事例不属于氧化还原反应的是()A.金属冶炼B.燃放鞭炮C.食物腐败■用汽油除去油污
4.下列各组物质发生的反应,既是化合反应,又是氧化还原反应的是()2H2s+SO2=3S A.1+2H2O I2NO+O2=2NO2催化剂4NH3+5O2^^4NO+6H2O△C.D.SO2+H2O=H2SO
35.下列变化属于还原反应的是(A.Fe一FeSC)4B.CuNC32一Cu C.CO―CO2D.NaCl-AgCl
6.如图为反应Fe+CuSO4=Cu+FeSO4中电子转移的关系图,则图中的元素甲、乙分别表示()A.Fe、S B.Cu、S C.Fe OD.Fe、Cu
7.我国“四大发明”在人类发展史上起到了非常重要的作用,其中黑火药的爆炸反应为2KNO3+S+3C金丝K2s+N2T+3co2T该反应中被氧化的元素是()?(?C B.N C.N和S D?N和C
8.将燃着的镁条伸入盛有二氧化碳的集气瓶中,镁条继续燃烧,反应的化学方程式为C02+2Mg=^C+2MgO,该反应属于()
①化合反应
②分解反应
③置换反应
④复分解反应
⑤氧化还原反应
⑥离子反应
⑦非氧化还原反应A.
①③⑦B.
②③⑥a
③⑤D.
④⑥
9.下列反应既是离子反应,又是氧化还原反应的是()A.BaCb溶液中滴加稀H2s04B.盐酸和氧化铁反应|.铁片放入盐酸中D.氢气还原CuO
10.自然界中存在的元素大多以化合态存在,而我们在生产生活中需要许多单质如金属铁、单质氯等试想,如果把某元素由化合态变为游离态,则它()A.一定被氧化B一定被还原C.可能被氧化,也可能被还原D.化合价降低为
11.在反应中,元素X的原子将电子转移给元素Y的原子,则下列说法正确的是()
①元素X被氧化
②元素Y被氧化
③元素X发生还原反应
④元素Y发生还原反应A.
①②B.
③④C.
②③D.
①④
12.P单质在反应4P+3KoH+3H2O=3KH2PO2+PH3中的变化是()A.被氧化B.被还原C.既被氧化又被还原D.既未被氧化又未被还原
13.盐酸在不同的反应中,可以分别表现出酸性、氧化性和还原性现在有如下三个反应,有关判断正确的是()
①Zn+2HCl=ZnCl2+H2T
②NaOH+HCl=NaCl+H20由解@2HC1=^=H2T+C12T选项有关判断A反应
①是置换反应,HC1表现还原性B反应
②是复分解反应,HC1表现氧化性C反应
③中HC1既表现氧化性也表现还原性D反应
①中氢原子失去电子
14.下列各反应中,氧化反应与还原反应在同种元素中进行的是()Cl2+2NaOH=NaCl+NaClO+H20MnO)B.2KC1O3=^2KC1+302C.2KMnO4=^=K2MnO4+MnO2+02由解D.2H2O3^2H2T+O2T
15.
(1)分析下列反应的化学方程式,是氧化还原反应的用双线桥法标出电子转移的方向和数目,指出被氧化和被还原的元素c,占燃
①2Na+Cb=^=2NaCl_________________________________________________________________________,
②NaOH+HCl=NaCl+H20
(2)分析下列反应的化学方程式,是氧化还原反应的用单线桥法标出电子转移的方向和数目
①BaCb+Na2so4=BaSO41+2NaCl______________________________________________________________________________________________________________________________________________________________________________________________________________________________9
②Fe+2HCl=FeCl2+H2T___________________________________________________________________________________________________________________________________________________________o
16.氧化还原反应有多种分类方法,其中根据参与电子转移的元素种类不同的分类方法最常见下列反应中电子转移发生在相同价态的同种元素之间的有:电子转移发生在不同价态的同种元素之间的有;电子转移发生在不同元素之间的有(填反应标号)
①Fe+2FeCb=3FeCb2NH4NO3=^=N2OT+2H2O@2KMnO4=^=K2MnO4+MnO2+02LX占燃@S+2KNO3+3C=^=K2S+N2+3co2T
⑤Cb+2Na0H=NaCl+NaC10+H20@HgS+02=^Hg+S
0217.Zn与HNO3反应时,HNC3溶液的浓度不同,产物也不同被氧化的Zn与被还原的HNO3的物质的量的关系如图所示表示还原产物为NH4NO3的是C.C D.D
18.酒后驾车是马路第一大杀手已知酒精C2H5OH能与KzCnCh和H2s04的混合溶液在一定条件下发生如下反应2K2Cr2O7+3C2H5OH+8H2so4=2K2so4+2Cr2SO43+3CH3COOH+IIH2O,且知CrzO厂和C#+在溶液中分别显橙色和绿色,回答下列问题1该反应填“是”或“不是离子反应2写出电离方程式Cr2SO43=03该反应填“是”或“不是”氧化还原反应,判断的依据是_______________________________________________________________________________________________________________________________________________________________________________________________________________O一⑷能否用这一反应来检测司机是否酒后驾车填“能”或否”,理由是
19.将亚硒酸与高锌酸钾共热可制得硒酸H2SeO4,配平该反应方程式,并标出电子转移的方向和数目H2SeO3+KMnO4-K2SeO4+MnSeO4+H2SeO4+
20.1加热搅拌条件下加入NaClCh,将Fe2+氧化成Fe3+,其离子方程式是2CoCO3隔绝空气灼烧可以生成Co2O3,该反应的化学方程式为。